Introducción
La esteatosis hepática metabólica (MASLD, Metabolic dysfunction Associated Steatotic Liver Disease) varía desde la esteatosis simple, la esteatohepatitis (MASH, Metabolic dysfunction Associated Steato Hepatitis) o la cirrosis hasta incluso el carcinoma hepatocelular1.
La fibrosis hepática es el principal determinante de la progresión de la MASLD. La fibrosis avanzada (estadio ≥ 3) se asocia con un mayor riesgo de desarrollar descompensación hepática (ascitis, sangrado variceal y encefalopatía hepática), necesidad de trasplante hepático y aumento de la mortalidad. Además, la relevancia de la fibrosis hepática trasciende el ámbito hepático, ya que también se relaciona con un mayor riesgo de desarrollar enfermedad cardiovascular2–4.
Los estudios más recientes sugieren que la fibrosis hepática clínicamente significativa (estadio ≥ 2) también conlleva consecuencias relevantes, entre ellas un mayor riesgo de progresar a cirrosis. Se estima que hasta un 20% de los pacientes con fibrosis en estadios tempranos desarrollarán fibrosis avanzada en un tiempo aproximado de 5 años5.
La fibrosis hepática en estadios tempranos constituye una fase crítica de la enfermedad, ya que es potencialmente tratable e incluso reversible con intervenciones adecuadas. En este contexto, la evaluación precisa y la correcta estadificación de la fibrosis adquieren un papel central en la monitorización de la progresión de la MASLD, con el fin de identificar oportunamente a los pacientes con fibrosis avanzada o clínicamente significativa (estadio ≥ 2)6.
El abordaje terapéutico, por tanto, no debe limitarse a mejorar la esteatosis hepática, sino que debe orientarse también a prevenir y enlentecer la progresión de la fibrosis. En esta revisión narrativa se puntualizan las principales estrategias farmacológicas actualmente aprobadas para el tratamiento de la MASLD.
Método
Se elaboró la siguiente síntesis de evidencia narrativa en los siguientes pasos:
- – Primer paso: se seleccionaron los temas relativos al tratamiento farmacológico de la MASLD.
- – Segundo paso: dos de los autores (DLP y JAVRV) evaluaron la información, la sintetizaron y codificaron en los diversos temas.
- – Tercer paso: posterior a la codificación se desarrollaron preguntas dirigidas y se realizó una revisión sistemática en las bases de datos DynaMed, Google Scholar y PubMed. Se utilizó la jerarquía de la pirámide de la evidencia preevaluada para la obtención de la información. Se empezó por sumarios de evidencias (guías de práctica clínica, Uptodate y Dynamed), seguidos de síntesis o sinopsis de evidencias (revisiones sistemáticas) y por último estudios originales (estudios controlados aleatorizados y estudios observacionales). La búsqueda de información se realizó en los idiomas español e inglés y se utilizaron las siguientes palabras clave: “esteatosis”, “enfermedad hepática grasa no alcohólica”, “fármacos” “tratamiento”, “fibrosis” “MASH”, “NASH”, “MASLD”, “resmetirom” y “GLP-1”. Se incluyeron las publicaciones desde el año 2010 hasta julio 2025.
Los resultados obtenidos fueron revisados por el equipo de autores, quienes utilizando el formato estandarizado extrajeron la información relevante para la inclusión en esta síntesis de evidencia narrativa. A continuación, se exponen los aspectos más relevantes.
Resultados
Criterios para iniciar el tratamiento farmacológico
El propósito del tratamiento farmacológico es otorgar beneficios clínicos palpables a los pacientes. En la enfermedad hepática crónica, esto podría expresarse a través de la reducción significativa de resultados clínicos como el desarrollo de cirrosis y sus complicaciones (ascitis, encefalopatía hepática, hemorragia gastrointestinal), así como de la mortalidad por cualquier causa7.
La modificación del estilo de vida sigue siendo la base fundamental del tratamiento de la MASLD, y el tratamiento farmacológico se reconoce cada vez más como un apoyo fundamental, principalmente en pacientes con MASH confirmada por biopsia, fibrosis significativa (≥ F2) o comorbilidad cardiometabólica8. Se ha evidenciado que, a pesar de que la MASH impulsa la progresión de la enfermedad, la fibrosis es el predictor más crítico del pronóstico, en términos tanto de enfermedad hepática como de mortalidad general. Se considera indicación de tratamiento para la MASH una puntuación ≥ 4 en el sistema de puntuación histológica para la esteatohepatitis no alcohólica (NASH, Non-Alcoholic Steatohepatitis) de la Clinical Research Network (NASH CRN), o una puntuación de actividad de ≥ 2 según el sistema de puntuación de esteatosis, actividad y fibrosis (SAF Steatosis, Activity, and Fibrosis), junto con una fibrosis significativa9,10.
Fármacos con indicación y evidencia clínica reciente
La fisiopatología de la MASLD y la MASH integra resistencia a la insulina, lipotoxicidad, inflamación y remodelado fibrogénico. Las terapias actuales y emergentes actúan sobre rutas metabólicas clave: 1) activación hepatoespecífica del receptor de la hormona tiroidea (THR) β para aumentar la β-oxidación y reducir la lipogénesis (resmetirom); 2) incretinas (agonistas del receptor del péptido similar al glucagón tipo 1 [GLP-1] y del polipéptido insulinotrópico dependiente de glucosa [GIP]), que inducen pérdida ponderal y mejoran la homeostasis metabólica con efectos hepáticos directos; 3) agonismo del factor de crecimiento de fibroblastos 21 (FGF21), que restaura el metabolismo lipídico y la inflamación; y 4) modulación vía agonistas de los receptores activados por proliferadores de peroxisomas (PPAR) de la esteatosis, la inflamación y la fibrosis. La figura 1 muestra las vías y los mecanismos de los fármacos utilizados en la MASLD.
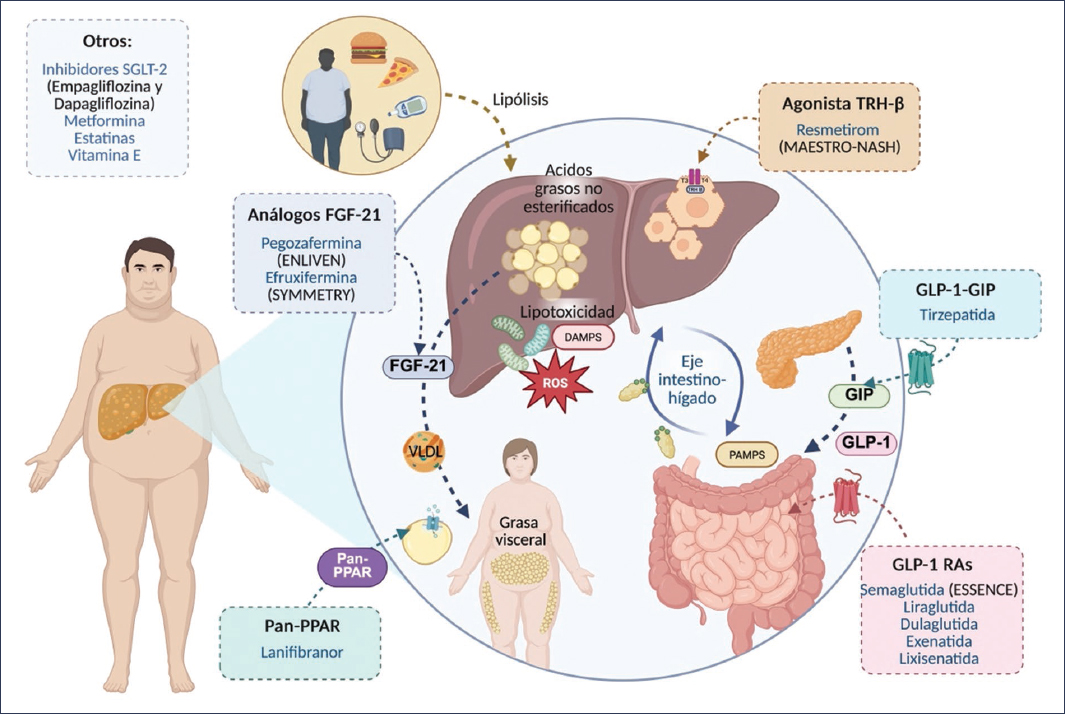
Figura 1. Abordaje farmacológico de la MASLD. Representación esquemática de los principales mecanismos fisiopatológicos (lipotoxicidad, estrés oxidativo, inflamación y eje intestino-hígado) y de las terapias en evaluación dirigidas a estos procesos, incluyendo agonistas de TRH-β, análogos de FGF-21, moduladores pan-PPAR, agonistas de GLP-1 RAs y combinaciones GLP-1/GIP, además de tratamientos convencionales como inhibidores de SGLT-2, metformina, estatinas y vitamina E.
RESMETIROM
Las hormonas tiroideas desempeñan sus funciones uniéndose a dos isoformas del receptor, la THR-α y la THR-β. La THR-β se expresa principalmente en los hepatocitos y cumple un papel fundamental en diversos procesos metabólicos. En particular, la activación de THR-β se vincula con importantes beneficios metabólicos en el hígado, puesto que puede reducir los niveles de colesterol y triglicéridos, estimular la síntesis de ácidos biliares y promover la oxidación de grasas. El resmetirom, un agonista del THR, actúa sobre la acumulación de grasa hepática para reducir la MASH y la fibrosis hepática avanzada11. Cuando el THR-β es estimulado por un agonista (p. ej., resmetirom), mejora la salud hepática al iniciar una cascada de procesos que suelen estar desregulados en los pacientes con MASH y que se asocian con la progresión de la enfermedad y el desarrollo de fibrosis hepática. Hasta el momento es el primer fármaco aprobado por la Food and Drug Administration (FDA) desarrollado específicamente para el tratamiento de la MASH. La determinación de la FDA de aprobar el resmetirom se sustentó en los hallazgos de un ensayo clínico de fase 3 (MAESTRO-NASH) que integró una cohorte de 966 pacientes con NASH12. La resolución de la NASH sin empeoramiento de la fibrosis se alcanzó en el 25.9% de los pacientes en el grupo de resmetirom a dosis de 80 mg y en el 29.9% de aquellos con resmetirom a dosis de 100 mg, en comparación con el 9.7% de los que recibieron placebo (p < 0.001). La mejoría de la fibrosis en al menos un estadio, sin empeoramiento de la puntuación de actividad de NAFLD (Non-Alcoholic Fatty Liver Disease), se logró en el 24.2% de los pacientes en el grupo de resmetirom 80 mg y en el 25.9% en el grupo de resmetirom 100 mg, en comparación con el 14.2% en el grupo placebo (p < 0.001). En este estudio también se documentó una reducción significativa de los niveles de colesterol unido a lipoproteínas de baja densidad desde el inicio hasta la semana 24, en comparación con el grupo placebo (p < 0.001). La diarrea y las náuseas fueron los eventos adversos más frecuentes; sin embargo, estos fueron similares en todos los grupos, lo que confirma la seguridad general del resmetirom13.
Estos hallazgos se confirmaron en un metaanálisis de tres ensayos clínicos aleatorizados (n = 2234) en los que el resmetirom redujo de manera significativa la grasa hepática por fracción de grasa hepática por resonancia magnética (MRI-PDFF) con 80 mg (–27.74% a 36-52 semanas y −30,92% a 12-16 semanas) y con 100 mg (–36.05% y –36.89%; todos p < 0.00001). Respecto a la seguridad, no hubo diferencias globales en cuanto a eventos adversos emergentes en comparación con placebo (para 80 mg, odds ratio [OR]: 1.55, intervalo de confianza del 95% [IC 95%]: 0.84-2.87; para 100 mg, OR: 1.13, IC 95%: 0.78-1.63), aunque fueron más frecuentes la diarrea y la náusea en < 12 semanas14.
SEMAGLUTIDA
El GLP-1 es liberado por las células enteroendocrinas en el tracto gastrointestinal y cumple un papel esencial en la regulación de los niveles de glucosa en sangre posprandiales, al incrementar la secreción de insulina y suprimir la liberación de glucagón15. El GLP-1 también retrasa el vaciamiento gástrico y atenúa la ingesta de alimentos, consiguiendo un equilibrio entre la absorción de nutrientes y la prevención del incremento excesivo de peso. Debido a su importancia en el metabolismo energético, diversos estudios han evaluado los efectos y los posibles beneficios del uso de agonistas del receptor de GLP-1 en el contexto de la salud hepática16. Entre los diversos agonistas del receptor de GLP-1, la semaglutida ha demostrado resultados optimistas en la resolución de la MASH. El ensayo de fase 3 ESSENCE, multicéntrico, aleatorizado, doble ciego y controlado con placebo, incluyó 1197 pacientes con MASH confirmada por biopsia y con fibrosis F2-F3, de los cuales se analizó interinamente a 800 tras 72 semanas de tratamiento con semaglutida en dosis de 2.4 mg por vía subcutánea semanal o placebo (2:1). La semaglutida logró la resolución de la esteatohepatitis sin empeoramiento de la fibrosis en el 62.9% frente al 34.3% (Δ 28.7 pp; p < 0.001) y una reducción de la fibrosis ≥ 1 estadio sin empeoramiento de la esteatohepatitis en el 36.8% frente al 22.4% (Δ 14.4 pp; p < 0.001), con una pérdida de peso media del 10.5% frente al 2.0% y mejoras en índice ELF (Enhanced Liver Fibrosis), la rigidez hepática y los parámetros cardiometabólicos. Respecto al perfil de seguridad, fue consistente con los agonistas GLP-1, predominando los eventos gastrointestinales leves a moderados17. Recientemente, la FDA emitió su aprobación para el tratamiento de la MASH en adultos con fibrosis de moderada a avanzada18.
PEGOZAFERMINA
La pegozafermina es un análogo recombinante del FGF21 de acción prolongada, la cual regula el metabolismo energético, principalmente en situaciones de estrés metabólico19. Los estudios preclínicos han demostrado que FGF21 podría potenciar la señalización de la proteína cinasa activada por AMP (AMPK), favoreciendo la oxidación de ácidos grasos y reduciendo la lipogénesis de novo, lo cual contribuye a la supresión de la fibrosis y a la mejoría del estado metabólico20. El ensayo de fase 2b ENLIVEN, multicéntrico, aleatorizado, doble ciego y controlado con placebo, incluyó 222 pacientes con NASH confirmada por biopsia y con fibrosis F2-F3, asignados a recibir pegozafermina a dosis de 15 mg semanal, 30 mg semanal, 44 mg cada 2 semanas o placebo durante 24 semanas. La mejoría de la fibrosis ≥ 1 estadio sin empeoramiento de la NASH se alcanzó en el 26% con 30 mg y en el 27% con 44 mg, frente al 7% con placebo (p = 0.009 y p = 0.008), y la resolución de la NASH sin empeoramiento de la fibrosis en el 23% con 30 mg, el 26% con 44 mg y el 37% con 15 mg, frente al 2% con placebo. Además, se observó una reducción significativa de la grasa hepática por MRI-PDFF de hasta −48.2%, la normalización de la alanina aminotransferasa (ALT) hasta un 65% y mejoras en el índice ELF, la rigidez hepática, el Pro-C3 y el perfil lipídico. En cuanto a la seguridad, se observaron por eventos gastrointestinales leves a moderados y un caso de pancreatitis aguda21. En otra cohorte única y multicéntrica, que incluyó 20 pacientes con NASH confirmada por biopsia y con fibrosis F2-F3, tras el tratamiento con pegozafermina a dosis de 27 mg semanal durante 20 semanas se observó un mejoría ≥ 2 puntos en puntuación de actividad de la esteatohepatitis (NAS) con ≥ 1 punto en ballooning o inflamación lobulillar, y sin empeoramiento de la fibrosis, en el 63% de los pacientes, con una reducción marcada de la grasa hepática por MRI-PDFF (−64.7%; 100% con ≥ 30% de reducción), la normalización de la ALT en el 79% de quienes la tenían elevada y mejoras en marcadores no invasivos de fibrosis22.
EFRUXIFERMINA
La efruxifermina es un análogo bivalente del FGF21 con acciones directas antifibróticas e indirectas sobre el metabolismo glucídico y lipídico, de administración por vía subcutánea semanalmente. El ensayo de fase 2b SYMMETRY, multicéntrico, aleatorizado, doble ciego y controlado con placebo, incluyó 181 pacientes con cirrosis compensada (Child-Pugh A) por MASH (78% con diagnóstico histológico y 22% con cirrosis criptogénica atribuida a MASH) asignados a recibir efruxifermina en dosis de 28 o 50 mg, o placebo (1:1:1), durante 96 semanas. El objetivo primario (reducción de la fibrosis ≥ 1 estadio sin empeoramiento de la MASH a las 36 semanas) no mostró diferencias significativas: 13% con placebo, 18% con 28 mg y 19% con 50 mg. A las 96 semanas, las tasas fueron del 11%, el 21% y el 29%, respectivamente (Δ vs. placebo: +16 pp para 50 mg; IC 95%: 2-30), con resolución de la MASH en el 42% de los tratados frente al 13% de los que recibieron placebo, y con mejoras en el índice ELF, la rigidez hepática, las enzimas hepáticas y el perfil cardiometabólico. Los eventos adversos fueron principalmente gastrointestinales y reacciones locales, en su mayoría leves o moderados23. En otro estudio previo, el 89% de los pacientes experimentaron al menos un evento adverso relacionado con el tratamiento, siendo los más comunes de grado 1-224. Finalmente, un metaanálisis que incluyó cuatro estudios con un total de 325 pacientes con MASH y fibrosis en etapas F1-F4 mostró que la efruxifermina tiene un riesgo relativo (RR) de 1.97 (IC 95%: 1.21-3.19; p = 0.006) para mejorar la fibrosis ≥ 1 estadio sin empeorar la MASH. Además, la efruxifermina mejoró los biomarcadores no invasivos relacionados con la fibrosis, como el puntaje ELF y el Pro-C325.
LANIFIBRANOR
El lanifibranor es un agonista pan-PPAR que regula las vías metabólicas, inflamatorias y fibróticas. Favorece específicamente la oxidación de ácidos grasos e inhibe la señalización del factor nuclear kappa B26. En un ensayo clínico de fase IIb, 288 pacientes fueron asignados aleatoriamente para recibir 1200 u 800 mg de lanifibranor, o placebo, una vez al día durante 24 semanas. Al finalizar el tratamiento se observó una mejoría significativa de la esteatosis histológica en comparación con el placebo: más del 35% de los pacientes tratados con lanifibranor mostraron una mejoría de al menos 2 grados en la esteatosis, frente a un 5% en el grupo con placebo. El parámetro de atenuación controlada (CAP) disminuyó significativamente: con 1200 mg, la diferencia media ajustada estimada fue de –23 dB/m (IC 95%: –41 a –5; p = 0.012), y con 800 mg fue de –16 dB/m (IC 95%: –33 a 1; p = 0.070), en comparación con el placebo, con el cual no se presentaron cambios. Al final del tratamiento, una proporción significativamente mayor de pacientes alcanzaron un CAP ≤ 302 dB/m (equivalente a esteatosis leve o ausente, ≤ S1): el 50% con 1200 mg (IC 95%: 36-64; p = 0.009), el 46% con 800 mg (IC 95%: 33-60; p = 0.019) y solo el 25% con placebo (IC 95%: 13-37). Se observó una correlación significativa entre el CAP y el grado de esteatosis histológica, tanto al inicio como al final del tratamiento (coeficiente de Spearman Rs = 0.37; p < 0.001). Finalmente, la reducción del CAP se asoció con disminuciones en los niveles de triglicéridos y de hemoglobina glucosilada al finalizar el tratamiento27.
TIRZEPATIDA
La tirzepatida es un coagonista de las hormonas incretinas GLP-1 y GIP que ha sido aprobado por la FDA para el tratamiento de la diabetes mellitus tipo 2 (DM2) y la pérdida de peso28. Es importante señalar que el aumento de la señalización de incretinas no solo beneficia a los pacientes con pérdida de peso prolongada, sino que también mejora la regulación de la glucemia, lo que sugiere su relevancia clínica en el tratamiento de la MASH. Con el fin de determinar la eficacia y la seguridad de la tirzepatida se realizó un ensayo clínico de fase 2 con 190 pacientes, que fueron asignados aleatoriamente a recibir semanalmente dosis de 5, 10 o 15 mg, o placebo, durante 52 semanas. El porcentaje de participantes que cumplieron los criterios de resolución de la MASH sin empeoramiento de la fibrosis fue del 10% en el grupo de placebo, el 44% en el grupo de tirzepatida 5 mg (diferencia frente a placebo 34%; IC 95%: 17-50), el 56% en el grupo de tirzepatida 10 mg (diferencia 46%; IC 95%: 29-62) y el 62% en el grupo de tirzepatida 15 mg (diferencia 53%; IC 95%: 37-69) (p < 0.001 para las tres comparaciones). El porcentaje de participantes que presentaron una mejoría de la fibrosis de ≥ 1 estadio sin empeoramiento de la MASH fue del 30% en el grupo de placebo, el 55% en el grupo de tirzepatida 5 mg (diferencia frente a placebo 25%; IC 95%: 5-46), el 51% en el grupo de tirzepatida 10 mg (diferencia 22%; IC 95%: 1-42) y el 51% en el grupo de tirzepatida 15 mg (diferencia 21%; IC 95%: 1-42). Los eventos adversos más frecuentes en los grupos de tirzepatida fueron gastrointestinales, y la mayoría leves o moderados29.
SURVODUTIDA
La survodutida es un agonista dual de GLP-1 y GIP. Con el fin de evaluar su rendimiento, se realizó un un ensayo clínico de fase II con 293 pacientes con una dosis semanal de 2.4, 4.8 o 6.0 mg, frente a placebo. Se observó una mejoría en la MASH sin empeoramiento de la fibrosis en el 47% de los participantes del grupo de survodutida 2.4 mg, el 62% de los del grupo de 4.8 mg y el 43% de los del grupo de 6.0 mg, en comparación con el 14% de los del grupo de placebo (p < 0.001). Se evidenció una disminución de al menos el 30% del contenido en el 63% de los participantes del grupo de survodutida 2.4 mg, el 67% de los del grupo de 4.8 mg, el 57% de los del grupo de 6.0 mg y el 14% de los del grupo de placebo. Hubo una mejoría de la fibrosis de ≥ 1 estadio en el 34%, el 36%, el 34% y el 22%, respectivamente. Los eventos adversos más frecuentes con survodutida que con placebo fueron náuseas (66% frente al 23%), diarrea (49% frente al 23%) y vómitos (41% frente al 4%)30.
Otros fármacos
VITAMINA E
La vitamina E es un micronutriente esencial y antioxidante liposoluble con funciones proteicas y efectos de modulación génica. Su metabolismo depende de las proteínas de unión hepáticas que retienen selectivamente el alfa-tocoferol de los alimentos para su incorporación a las lipoproteínas de muy baja densidad y su posterior distribución tisular, junto con el colesterol esterificado y los triglicéridos31. Diversos estudios han demostrado que la suplementación con vitamina E puede mejorar significativamente los niveles de enzimas hepáticas, aspartato aminotransferasa (AST) y ALT, reducir la esteatosis hepática y mejorar la inflamación hepática32. En una revisión sistemática se evaluó la eficacia de la suplementación con vitamina E en pacientes adultos con MASLD, con dosis que variaron de 200 UI a 1000 mg diarios, y la duración del tratamiento fue de 12 a 96 semanas. Las dosis más altas mostraron sistemáticamente reducciones significativas en las enzimas hepáticas (AST y ALT), la esteatosis hepática y la inflamación, aunque el efecto sobre la fibrosis fue limitado. Este hallazgo se vio reforzado en el estudio realizado por Pervez et al.33, en el que la administración de δ-tocotrienol y α-tocoferol logró disminuciones significativas (p < 0.001) de ALT y AST, así como del colesterol total y del unido a lipoproteínas de baja densidad (p < 0.05), y un aumento significativo del colesterol unido a lipoproteínas de alta densidad, en comparación con los valores basales, en ambos grupos de estudio. Con respecto a las mejoras histológicas, en este mismo estudio se demostraron mejoras significativas en la esteatosis hepática y en las relaciones de atenuación hígado-bazo en los grupos de tocoferol y tocotrienol, lo que respalda aún más el papel de la vitamina E en la mejora del contenido de grasa hepática33. Abera et al.34 también hallaron mejoras en la esteatosis, lo que indica que dosis más altas de vitamina E (400-800 UI/día) son más efectivas para abordar las características histológicas.
El efecto de la vitamina E sobre la fibrosis es menos concluyente; si bien varios estudios encontraron mejoras en la esteatosis y la inflamación, no mostraron cambios significativos en la fibrosis35. La evidencia general del impacto de la vitamina E sobre la fibrosis sigue siendo limitada, lo que sugiere que su papel principal puede estar en abordar el daño hepático en etapa temprana en lugar de revertir la fibrosis avanzada.
ESTATINAS
Además de su efecto hipolipidemiante, las estatinas presentan propiedades antiinflamatorias, antioxidantes, proapoptóticas y antifibróticas que podrían beneficiar a los pacientes con MASLD y MASH36. En un estudio realizado en individuos con síndrome metabólico sin diabetes ni evento vascular cerebral (EVC), las enzimas hepáticas y la ecografía mejoraron durante el estudio con el uso de estatinas37. Un metaanálisis destacó el efecto de las estatinas en la reducción significativa de los marcadores bioquímicos hepáticos en la MASLD38 y su asociación con menor riesgo de carcinoma hepatocelular39. Ayada et al.40 realizaron un estudio que comprendía una investigación transversal en una cohorte de población general en curso (estudio Rotterdam) y una cohorte de pacientes con MASLD (cohorte PERSONS), un metaanálisis y una exploración experimental. En el análisis de los 4576 participantes del estudio Rotterdam, el uso de estatinas en pacientes con dislipidemia se asoció inversamente con MASLD en comparación con los participantes con dislipidemia no tratada (OR: 0.72; IC 95%: 0.59-0.86). En la cohorte PERSONS, el análisis de 569 pacientes con MASH comprobada por biopsia mostró que el uso de estatinas se asoció inversamente con MASH (OR: 0.55; IC del 95%: 0.32-0.95), pero no con fibrosis (OR: 0.86; IC 95%: 0.44-1.68)40. Actualmente, el ensayo STAT MASH (NCT04679376) evalúa la eficacia y la seguridad de la atorvastatina en la MASH con criterios histológicos. En conjunto, las estatinas son seguras en los pacientes con MASLD, no incrementan el riesgo de hepatotoxicidad y están indicadas para prevenir eventos cardiovasculares. No obstante, su eficacia específica para el tratamiento de la MASH aún requiere confirmación mediante ensayos clínicos de gran escala41.
INHIBIDORES DEL COTRANSPORTADOR DE SODIO-GLUCOSA TIPO 2 (SGLT2)
Son agentes antihiperglucémicos que actúan sobre las proteínas SGLT-2, expresadas en los túbulos contorneados proximales. Estos fármacos ejercen su efecto impidiendo la reabsorción de la glucosa filtrada en el lumen tubular42. Además, a través de la estimulación de la vía de señalización SIRT1/AMPK y la inhibición de Akt/mTOR, ejercen efectos que incluyen reducción del estrés oxidativo, la inflamación y el daño microvascular, beneficiando las funciones cardiaca y renal43. Clínicamente, los inhibidores del SGLT2 han demostrado beneficio cardiovascular en pacientes con enfermedad cardiovascular aterosclerótica y DM2, lo que los convierte en un enfoque terapéutico de primera elección para este grupo de pacientes44. En particular, el ensayo EMPEROR-PRESERVED evidenció que la empagliflozina reduce de manera significativa el riesgo combinado de muerte por causa cardiovascular u hospitalización por insuficiencia cardiaca en pacientes con insuficiencia cardiaca y fracción de eyección preservada, independientemente de la presencia o ausencia de diabetes45. En el caso de la canaglifozina, los ensayos clínicos aleatorizados han demostrado que mejora la sensibilidad hepática a la insulina, así como la secreción y el aclaramiento de insulina en pacientes con DM2. La reducción del contenido de triglicéridos hepáticos se correlaciona proporcionalmente con la magnitud de la pérdida de peso, la cual fue mayor y más frecuente en los pacientes tratados con canaglifozina46. Destacan el ensayo EMPA-REG OUTCOME, que mostró una reducción significativa de las aminotransferasas con empagliflozina47, y un metaanálisis de diez ensayos controlados aleatorizados con 573 participantes que confirmó la superioridad de los inhibidores del SGLT2 frente a otros antihiperglucémicos en cuanto a mejoría de los parámetros hepáticos y metabólicos48. La evidencia en pacientes no diabéticos es escasa; un pequeño estudio comparó la dapagliflozina y la teneligliptina en pacientes con MASLD y encontró mejorías en las transaminasas y en la reducción de la grasa corporal solo en el grupo tratado con dapagliflozina49. A pesar de ello, no existe evidencia contundente que justifique su empleo en el tratamiento de la MASH41.
METFORMINA
La metformina es un agente hipoglucemiante que actúa activando la AMPK en las células y reduciendo la producción de glucosa en el hígado50. En un metaanálisis se demostró una asociación significativa con la reducción de los parámetros bioquímicos en pacientes con MASLD. Con respecto a la ALT, hubo una reducción promedio que alcanzó el umbral de significación estadística (desviación media [DM] = −10.84; IC 95%: −21.85 a 0.16; p = 0.05). Para la AST, el análisis evidenció una disminución estadísticamente significativa (DM = −4.82; IC 95%: −9.33 a −0.30; p = 0.04). Respecto al índice de masa corporal, no se identificó un efecto significativo de la metformina (DM = −0.65; IC 95%: −1.46 a 0.16; p = 0.12). Por el contrario, se observó una reducción significativa en los niveles séricos de triglicéridos (DM = −0.17 mmol/l; IC 95%: −0.26 a −0.08; p = 0.0002) y de colesterol total (DM = −0.29 mmol/l; IC 95%: −0.47 a −0.10; p = 0.003). Adicionalmente, la resistencia a la insulina, evaluada mediante el índice HOMA-IR, mostró una reducción estadísticamente significativa en el grupo tratado con metformina (DM = −0.42; IC 95%: −0.82 a −0.02; p = 0.04). Estos hallazgos sugieren que la metformina podría contribuir a mejorar el perfil hepático y lipídico, así como la sensibilidad a la insulina51. Sin embargo, actualmente no existe evidencia de que la metformina por sí sola pueda mejorar la histología en la enfermedad hepática asociada a la DM2. En cuanto a los resultados clínicos, existen indicios, derivados de estudios observacionales y de casos y controles, que sugieren que en los pacientes con DM2 y fibrosis o cirrosis avanzada asociada a MASLD la metformina puede mejorar la superviviencia libre de trasplante sin afectar el riesgo de descompensación hepática, además de reducir el riesgo de carcinoma hepatocelular y de neoplasias extrahepáticas. En una cohorte de pacientes con cirrosis avanzada, el 85% de los tratados con metformina y el 88% de los no tratados presentaban esta patología. Tras un seguimiento de 6.9 años, el uso de metformina se asoció con menor riesgo de mortalidad por todas las causas y de trasplante (hazard ratio [HR]: 0.42; IC 95%: 0.24-0.74; p = 0.003), y de carcinoma hepatocelular (HR: 0.25; IC 95%: 0.11-0.58; p = 0.001)52. Por lo tanto, se sugiere que en individuos con cirrosis no se debe suspender la metformina, a menos que sea necesario, ya que esto podría aumentar la mortalidad53. No hay evidencia suficiente para recomendar el uso de metformina como terapia dirigida a la MASH, pero es segura en los pacientes con MASLD y debe usarse para sus respectivas indicaciones, es decir, DM2, insuficiencia cardiaca y enfermedad renal crónica54.
Terapias combinadas
En la MASH, la terapia combinada dirigida a distintas vías representa una alternativa llamativa para mejorar la eficacia clínica y reducir los efectos adversos mediante dosis más bajas o fármacos con acciones complementarias55. La terapia combinada constituye un área activa de investigación en la MASH. La principal justificación es que la focalización en múltiples vías mejoraría la eficacia y el índice terapéutico56. Además, el gran número de vías y agentes considerados para la MASH generan dificultades en la elección de dos vías óptimas. Otras consideraciones para los ensayos de terapia combinada son la mayor complejidad de los requisitos regulatorios, el mayor número de pacientes requerido, la selección de la dosis óptima, el posible aumento de los efectos secundarios y el costo57. A pesar de estos desafíos, se han completado varios ensayos de combinación de fase 2. En un ensayo de fase 2b, 392 pacientes con fibrosis en puente o cirrosis compensada (F3-F4) fueron aleatorizados para recibir placebo, selonsertib 18 mg, cilofexor 30 mg o firsocostat 20 mg, solos o en combinaciones de dos fármacos, una vez al día, durante 48 semanas. La mayoría presentaban cirrosis (56%) y una puntuación de actividad de la MASLD ≥ 5 (83%). La combinación de cilofexor y firsocostat logró una disminución significativa en la puntuación de fibrosis ML NASH CRN (p = 0.040) y un cambio en el área de la biopsia de patrones de fibrosis F3-F4 a ≤ F2. En comparación con el placebo, proporciones significativamente mayores de pacientes con cilofexor/firsocostat tuvieron una reducción de NAS ≥ 2 puntos; reducciones en la esteatosis, la inflamación lobulillar y la balonización; y mejoras significativas en ALT, AST, bilirrubina, ácidos biliares, citoqueratina-18, insulina, tasa de filtración glomerular estimada, puntuación ELF y rigidez hepática mediante elastografía transitoria (p ≤ 0.05 en todos los casos). Se observó prurito en el 20-29% de los pacientes tratados con cilofexor, frente al 15% de los que recibieron placebo58. En un ensayo con 108 pacientes se compararon semaglutida con cilofexor (agonista del receptor X farsenoide [FXR]), semaglutida con el inhibidor de la enzima acetil-CoA carboxilasa (ACC) firsocostat y los tres fármacos. Los tratamientos fueron bien tolerados: la incidencia de eventos adversos fue similar entre los grupos (73-90%) y la mayoría de los eventos fueron de naturaleza gastrointestinal. A pesar de la pérdida de peso similar (7-10%), en comparación con la monoterapia con semaglutida, las combinaciones resultaron en mayores mejoras en la esteatosis hepática medida por MRI-PDFF (media de mínimos cuadrados de los cambios absolutos: –9.8 a –11.0% frente a –8.0%), la bioquímica hepática y las pruebas no invasivas de fibrosis. Además, se observó una reducción uniforme y estadísticamente significativa de la ALT, como marcador de daño hepatocítico, en todos los grupos de combinación59.
Es posible que la terapia combinada ofrezca ventajas sobre la monoterapia, lo que abre el debate sobre si debería adoptarse siempre como tratamiento de primera línea, reservarse únicamente para una fase inicial breve seguida de monoterapia de mantenimiento, o aplicarse solo en pacientes que no respondan a la monoterapia. Esta decisión dependerá en gran medida del tipo de beneficios que aporte la combinación terapéutica, los cuales podrían incluir un mayor grado de respuesta, un incremento en la proporción de pacientes que responden, una respuesta más rápida o más duradera, así como un mejor perfil de tolerabilidad y eventos adversos57. Dentro de las opciones de combinación, las terapias basadas en incretinas tendrán un papel relevante, dado que la mayoría de los pacientes con MASH presentan DM2 u obesidad, condiciones en las que estas ya se utilizan de forma habitual. En la práctica clínica, la cuestión más frecuente será determinar qué fármaco añadir a la incretina que ya recibe un paciente con MASH. Por ejemplo, se realizó un estudio de fase IIb, doble ciego y controlado con placebo, en adultos con DM2 y MASH con fibrosis (F1-F3) en tratamiento estable con agonistas del receptor de GLP-1 para recibir efruxifermina 50 mg o placebo, una vez a la semana durante 12 semanas. En total, 31 adultos con DM2 y fibrosis por MASH (F1-F3) en tratamiento con un GLP-1RA estable (semaglutida el 48.4%, dulaglutida el 45.2% y liraglutida el 6.5%) recibieron efruxifermina 50 mg (n = 21) o placebo (n = 10) durante 12 semanas. Los eventos adversos más frecuentes relacionados con la efruxifermina fueron gastrointestinales y de leves a moderados. Después de 12 semanas, la efruxifermina redujo la fracción de grasa hepática (HFF) en un 65% (p < 0.0001 frente a placebo) en comparación con una reducción del 10% con placebo (GLP-1RA solo). La efruxifermina también mejoró los marcadores no invasivos de lesión hepática, fibrosis, glucosa y metabolismo lipídico, al tiempo que mantuvo la pérdida de peso mediada por GLP-1RA60.
En la tabla 1 se muestran los estudios más relevantes sobre los fármacos utilizados en el tratamiento de la MALSD.
Tabla 1. Tratamientos farmacológicos de la MASLD
| Fármaco | Ensayos clínicos | Posología | Población estudiada | Resultados | Potenciales efectos adversos |
|---|---|---|---|---|---|
| Vitamina E |
Sanyal et al.67 | 800 UI/día, 96 sem | MASH sin DM2 o cirrosis | Mejoría de esteatosis, inflamación y balonización, mejoría de transaminasas, ¿Resolución de MASH? | Evento vascular cerebral hemorrágico ¿Riesgo de cáncer de próstata? |
| Semaglutida |
Newsome et al.68 Flint et al.69 |
0.4 mg/día, vía subcutánea, 72 sem | MASH sin cirrosis y MASLD sin fibrosis significativa | Resolución de la MASH, disminución del LFC, disminución de peso, RCV y resistencia a la insulina ¿Disminución de la progresión de la fibrosis? | Náusea, estreñimiento, vómitos, colelitiasis, pancreatitis |
| Dulaglutida | Seko et al.70 Kuchay et al.71 |
0.75-1.5 mg/sem, 12 a 24 sem | MASLD con DM2 | Disminución de la esteatosis, pérdida de peso, mejoría en las transaminasas y GGT | Epigastralgia y diarrea |
| Empagliflozina |
Kuchay et al.72 Kahl et al.73 |
10-25 mg/día, 20-24 sem | MASLD con DM2 | Disminución del LFC y ALT | Poliuria e infecciones genitourinarias fúngicas |
| Dapagliflozina |
Latva-Rasku et al.74 Tobita et al.75 |
5-10 mg/día, 8-12 sem | MASLD con DM2 y solo MASLD | Disminución en el LFC, pérdida de peso y mejoría de las transaminasas | |
| Ipragliflozina | Ito et al.76 Takahashi et al.77 |
50 mg/día, 24-72 sem | MASLD con DM2 | Disminución de peso, grasa abdominal, mejora de fibrosis y control glucémico | |
| Canagliflozina |
Akuta et al.78 | 100 mg/día, 24 sem | MASLD con DM2 | Mejora de parámetros histológicos y de la ET, el IMC y la grasa visceral | |
| Tirzepatida | Gastaldelli et al.79 | 10-15 mg/sem, vía subcutánea, 52 sem | DM2 con sobrepeso y MASLD | Mejoría en el LFC, pérdida de peso y mejora de la resistencia a la insulina | Colelitiasis y pancreatitis |
| Retatrutida | Jastreboff et al.80 | 4-12 mg/sem, 48 semanas | Obesidad | Reducción de peso sustancial | Náusea, diarrea, vómito y estreñimiento |
| Lanifibranor | Francque et al.26 | 800-1200 mg/día, 24 sem | MASH sin cirrosis | Resolución de la MASH, disminución de transaminasas | Diarrea, náusea, edema periférico, anemia, ganancia de peso |
| Elafibranor | Ratziu et al.81 | 80-120 mg/día, 52 sem | MASH sin cirrosis | Resolución de la MASH sin empeoramiento de la fibrosis | Elevación reversible de la creatinina |
| Resmetirom | Harrison et al.12 | 80 o 100 mg/día, 52 sem | MASH sin cirrosis | Resolución de la MASH y mejoría de la fibrosis | Diarrea y náusea |
* Principales estudios publicados con resultados clinicos demostrados en MASLD de acuerdo a caracteristicas de población y efects adversoso observados. Se incluye el primer farmaco aprobado (resmetirom). ALT: alanino aminotransferasa; DM2: diabetes mellitus tipo 2; ET: elastografía de transición; GGT: gamma-glutamil transpeptidasa; IMC: índice de masa corporal; LFC: cuantificación de grasa hepática; RCV: riesgo cardiovascular.
Farmacogenómica
VARIANTE I148M DEL GEN PNPLA3
La mutación I148M del gen PNPLA3 se ha considerado el principal factor genético relacionado con susceptibilidad a la MASH61. PNPLA3 tiene actividad hidrolasa sobre los triglicéridos, y la variante genética I148M se asocia con una pérdida funcional de esta actividad, lo que fomenta la acumulación de triglicéridos en los hepatocitos y favorece el desarrollo de esteatosis hepática62. La mutación en el gen PNPLA3 desempeña un papel fundamental en la progresión de la MASLD. Por ello, orientar el tratamiento hacia la proteína PNPLA3 que porta la mutación I148M representa una prometedora estrategia terapéutica. De hecho, varios estudios han demostrado que el silenciamiento específico de PNPLA3 en el hígado, mediante oligonucleótidos antisentido (ASO), mejora significativamente diversos aspectos de la MASLD, incluyendo disminución de la esteatosis hepática, la inflamación y la fibrosis63. Considerando estos estudios preclínicos, un ASO dirigido a PNPLA3, llamado ION839 (AZD 2693), se encuentra actualmente en fase I de investigación clínica en pacientes con MASH portadores de los alelos de riesgo I148M de PNPLA3 (NCT04483947). Además del ASO, también se está evaluando la eficacia de un ARNi dirigido a PNPLA3, conocido como LY3849891, en ensayos clínicos para pacientes con MASH con variantes de PNPLA3 (NCT05395481)64. La modulación específica de la actividad PNPLA3 a través de ARNi integra un enfoque terapéutico potencialmente eficaz para el tratamiento de la MASH. Sin embargo, estas intervenciones basadas en ARNi se encuentran en una etapa preliminar y se requieren investigaciones exhaustivas para esclarecer los beneficios terapéuticos y la seguridad de estos enfoques innovadores antes de su aplicación clínica20.
VARIANTE RS72613567 EN HSD17B13
La proteína HSD17B13 es una retinol deshidrogenasa hepática que se localiza principalmente en la superficie de las gotas lipídicas de los hepatocitos. La inhibición de la expresión HSD17B13 suprime la fibrosis hepática al reducir el catabolismo de las pirimidinas65. Aunque los mecanismos precisos de las variantes de HSD17B13 en la MASH siguen sin estar claros, los estudios han identificado que la fosforilación de HSD17B13 mediada por la proteína cinasa A interactúa con la lipasa de triglicéridos adiposos para promover la lipólisis y suprimir la MASH66. Por lo tanto, estos hallazgos indican que HSD17B13 es una posible diana farmacológica contra la MASH.
Se realizó un ensayo clínico de fase I/II de prueba de concepto para evaluar la eficacia de una intervención de 71 días con ARO-HSD. El tratamiento fue bien tolerado y los cambios medios en el ARNm hepático de HSD17β13 desde el inicio hasta el día 71 fueron –56.9% con 25 mg, –85.5% con 100 mg y –93.4% con 200 mg. Los niveles de proteína hepática HSD17β13 se redujeron de forma similar con todas las dosis. En los pacientes, los cambios en la ALT desde el inicio hasta el día 71 fueron –7.7% con 25 mg, –39.3% con 100 mg y –42.3% con 200 mg (p < 0.001 para las cohortes agrupadas). No hubo eventos adversos graves relacionados con el tratamiento ni interrupciones del fármaco. Los eventos adversos emergentes del tratamiento notificados con mayor frecuencia fueron reacciones leves en el lugar de la inyección, de corta duración. La ARO-HSD fue bien tolerada en dosis ≤ 200 mg. Este estudio demostró que el tratamiento a corto plazo con ARO-HSD reduce la expresión hepática del ARNm y la proteína HSD17β13, lo que se acompaña de reducciones en la ALT.
Conclusiones
La modificación intensiva del estilo de vida sigue siendo el pilar del manejo de la MASLD. Sin embargo, en la MASH con fibrosis significativa (≥ F2), la terapia farmacológica aporta beneficios clínicos medibles y debería considerarse con prioridad, especialmente si coexisten obesidad o DM2 (Fig. 2). La fibrosis es el predictor más sólido de desenlaces hepáticos y de mortalidad global, por encima de la actividad inflamatoria, por lo que el objetivo terapéutico debe centrarse en frenar y revertir la fibrosis.
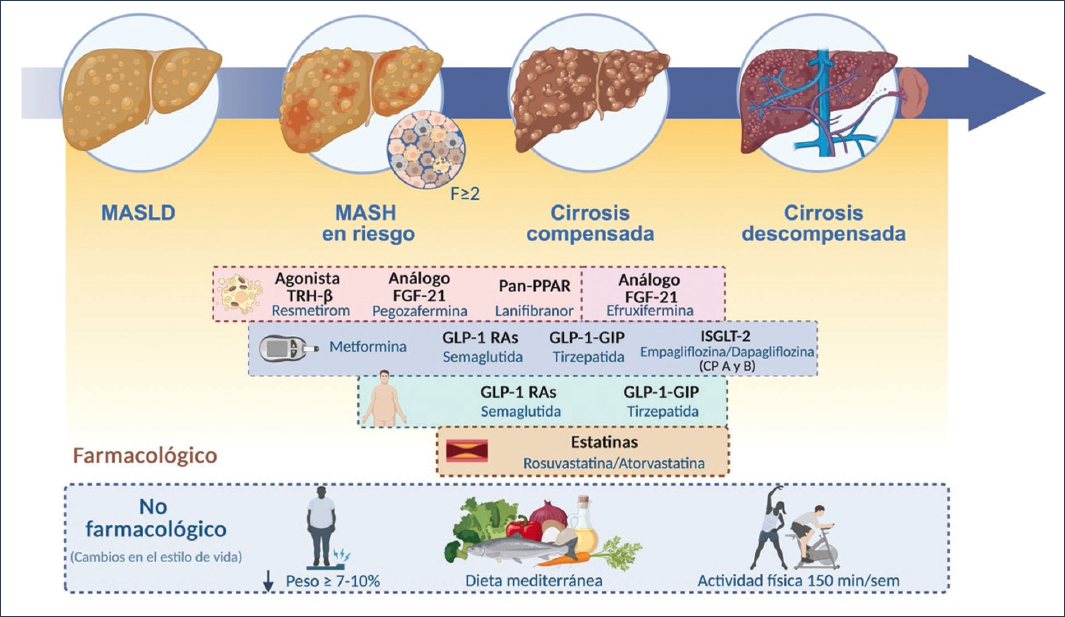
Figura 2. Tratamiento de la MASLD a lo largo de la progresión de la enfermedad, desde el estadio inicial hasta la cirrosis descompensada. Se representan las intervenciones no farmacológicas (pérdida de peso ≥ 7-10%, dieta mediterránea y actividad física) como base terapéutica, junto a las estrategias farmacológicas en investigación o uso clínico (agonistas de TRH-β, análogos de FGF-21, moduladores pan-PPAR, agonistas GLP-1 RAs, GLP-1/GIP, inhibidores de SGLT-2, metformina y estatinas).
Financiamiento
Los autores declaran no haber recibido financiamiento para este estudio.
Conflicto de intereses
J.A. Velarde-Ruiz Velasco ha participado en advisory board de Novo Nordisk México.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. El estudio no involucra datos personales de pacientes ni requiere aprobación ética. No se aplican las guías SAGER.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no utilizaron ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.
