Introducción
La enfermedad hepática esteatósica asociada a disfunción metabólica (MASLD, Metabolic dysfunction Associated Steatotic Liver Disease) constituye actualmente la primera causa de hepatopatía crónica en el mundo. Su prevalencia global se estima entre el 25% y el 30% de la población adulta, con cifras que superan el 40% en regiones con elevada incidencia de obesidad y diabetes mellitus tipo 21. El reciente cambio en la nomenclatura, de NAFLD (Non-Alcoholic Fatty Liver Disease) a MASLD, refleja mejor la íntima asociación con la disfunción metabólica y subraya que esta enfermedad no es un epifenómeno aislado, sino una manifestación hepática de un síndrome multisistémico2,3. La relevancia clínica de la MASLD trasciende claramente la progresión hepática hacia fibrosis avanzada, cirrosis o carcinoma hepatocelular4–6. De hecho, la principal causa de morbimortalidad en estos pacientes es de origen cardiovascular, y no hepática7–9.
Los mecanismos que sustentan esta asociación son múltiples y complejos, en consonancia con la teoría de los «múltiples impactos», que integra resistencia a la insulina, lipotoxicidad, inflamación sistémica, disfunción endotelial, alteraciones de la coagulación, regulación neurohormonal, microbiota intestinal y determinantes genéticos10–13 y condicionantes sociales y comerciales (nuestro LAncet). De forma destacada, emergen nuevos mediadores, como el imidazol-propionato, metabolito derivado del catabolismo microbiano de la histidina, que se perfila como un marcador patogénico clave y posible diana terapéutica en un futuro inmediato14–16.
Pese a la magnitud de la evidencia, la práctica clínica continúa centrada casi en exclusiva en la detección y la monitorización de la fibrosis hepática, mientras que la valoración del riesgo cardiovascular (RCV) es escasa o inexistente en la mayoría de las consultas. Una encuesta nacional en hospitales españoles mostró que menos del 17% realizan una exploración física básica orientada al riesgo, solo un 10% utiliza calculadoras, más de la mitad no solicitan pruebas complementarias y apenas el 46% dedican un tiempo significativo al consejo de estilo de vida; únicamente uno de cada cuatro dispone de circuitos multidisciplinarios17. Este déficit asistencial, sumado al bajo rendimiento de las puntuaciones de riesgo clásicas, refuerza la necesidad de integrar de manera sistemática la valoración vascular en nuestras consultas, apoyada en biomarcadores, técnicas de imagen y un abordaje multidisciplinario. A esta infraevaluación se añade que los algoritmos clásicos de predicción, como el Framingham Risk Score o las Pooled Cohort Equations, presentan un rendimiento limitado en esta población, con pobre discriminación y mala calibración, como ha demostrado el estudio TARGET-NASH18.
El creciente reconocimiento de la MASLD como determinante independiente de riesgo vascular obliga a replantear la aproximación de los hepatólogos a esta patología. La magnitud del problema exige no solo comprender los mecanismos fisiopatológicos que explican su asociación con la enfermedad cardiovascular (ECV), sino también identificar con claridad los distintos desenlaces clínicos implicados y disponer de herramientas adecuadas para su estratificación. Este marco de actuación se alinea con las guías recientes de la European Association for the Study of the Liver (EASL), la European Association for the Study of Diabetes (EASD) y la European Association for the Study of Obesity (EASO), y con las guías de hipertensión de la European Society of Cardiology (ESC) y la European Society of Hypertension (ESH) de 2024 y del American College of Cardiology (ACC) y la American Heart Association (AHA) de 2025, que consolidan una aproximación global basada en el riesgo y ofrecen al hepatólogo una referencia actualizada para integrar la valoración cardiovascular en la práctica asistencial19–22.
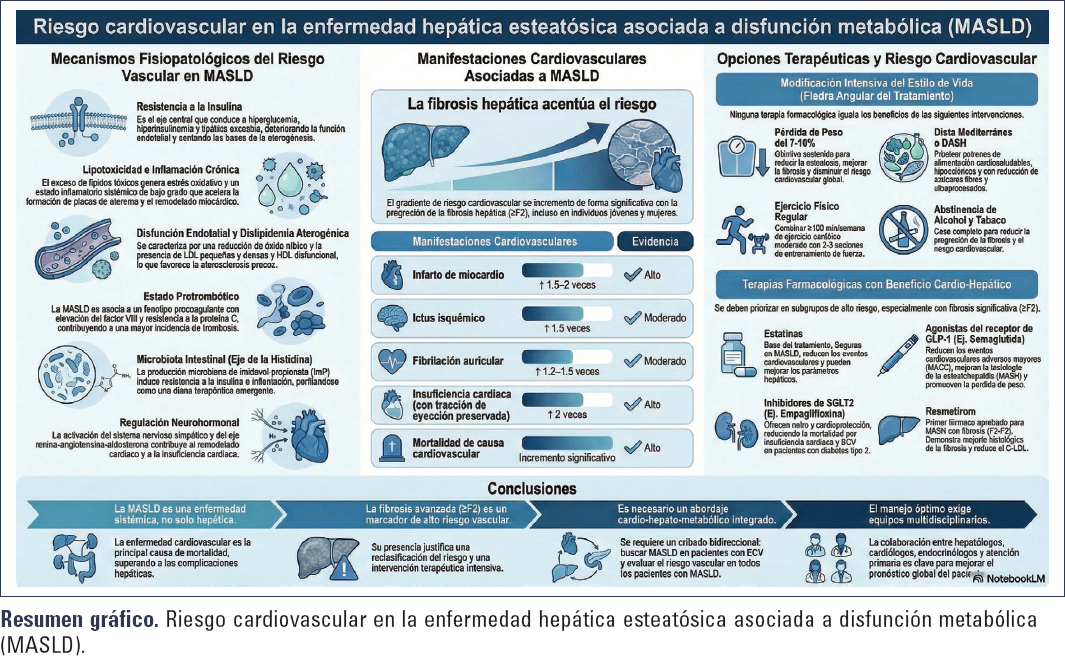
Con este objetivo, el presente artículo ofrece una revisión crítica y estructurada del vínculo entre la MASLD y el RCV, dirigida a hepatólogos expertos, pero no necesariamente familiarizados con los aspectos técnicos del riesgo vascular. El manuscrito propone un recorrido deliberado y progresivo que transita desde los mecanismos fisiopatológicos hasta la descripción sistemática de los RCV asociados a la MASLD, para posteriormente analizar las herramientas de evaluación disponibles y concluir con una reflexión crítica sobre la brecha existente en la práctica clínica hepatológica y las estrategias multidisciplinarias necesarias, incluyendo el abordaje del manejo clínico del RCV en esta población. Nuestra esperanza es poder contribuir a un cambio de paradigma en la práctica clínica, que contemple de forma conjunta el cuidado del hígado y la protección cardiovascular.
Fisiopatología del incremento del riesgo vascular en la MASLD
La fisiopatología de la MASLD es extraordinariamente compleja y responde a la teoría de los múltiples impactos simultáneos, que integran factores metabólicos, inflamatorios, genéticos, ambientales y de la microbiota10–13. Sin embargo, para comprender el aumento del RCV en estos pacientes, resulta más apropiado centrarse en los mecanismos que, de forma directa o indirecta, vinculan al hígado con la patología cardiovascular (Tabla 1 y Fig. 1).
Tabla 1. Mecanismos fisiopatológicos del incremento del riesgo vascular en la MASLD
| Mecanismo | Efectos cardiovasculares principales |
|---|---|
| Resistencia a la insulina | Hiperglucemia, hiperinsulinemia, disfunción endotelial, aterogénesis acelerada |
| Lipotoxicidad e inflamación crónica | Estrés oxidativo, producción de interleucina 6 y factor de necrosis tumoral alfa, remodelado vascular y miocárdico |
| Disfunción endotelial y dislipidemia aterogénica | Reducción de óxido nítrico, LDL pequeñas y densas, HDL disfuncional → aterosclerosis precoz |
| Fibrosis hepática | Marcador de mortalidad de causa cardiovascular, daño multiorgánico, progresión de aterosclerosis |
| Estado protrombótico | Elevación del factor VIII, resistencia a proteína C → trombosis arterial y venosa |
| Microbiota intestinal (eje de la histidina) | Producción de imidazol-propionato por urdA → resistencia a la insulina, inflamación endotelial, rigidez arterial. Potencial diana terapéutica emergente |
| Regulación neurohormonal | Activación simpática y RAAS → remodelado cardiaco, insuficiencia cardiaca con fracción de eyección preservada |
| Genética y heterogeneidad causal | Variantes como PNPLA3/TM6SF2 promueven esteatosis, pero reducen VLDL; otras variantes aumentan el riesgo coronario |
HDL: lipoproteínas de alta densidad; LDL: lipoproteínas de baja densidad; RAAS: sistema renina-angiotensina-aldosterona; VLDL: lipoproteínas de muy baja densidad.
La fisiopatología de la MASLD conecta el hígado, el sistema cardiovascular y el metabolismo, justificando el abordaje integrado cardio-hepato-metabólico.
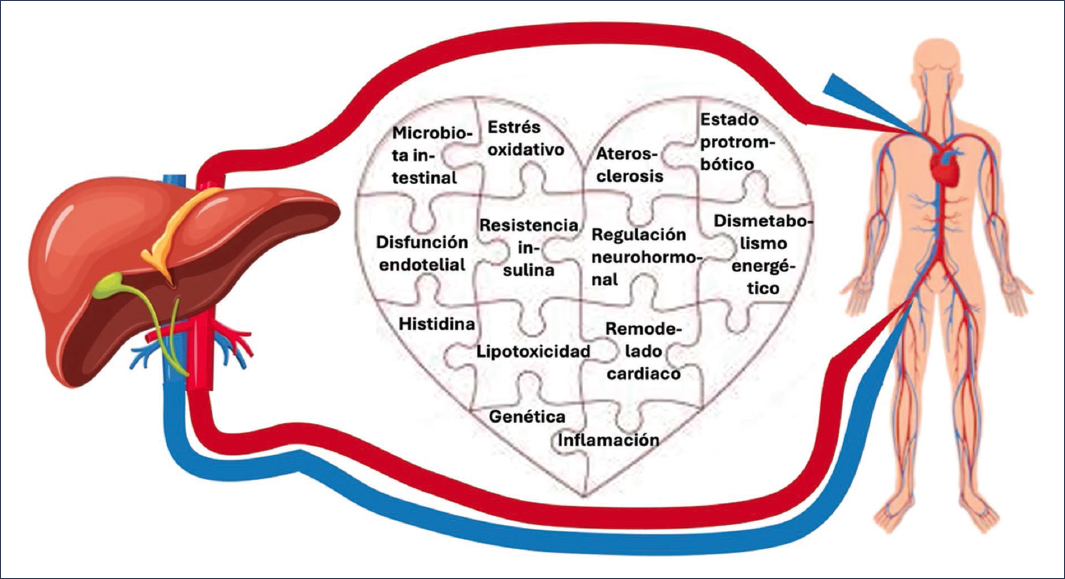
Figura 1. Mecanismos asociados con la fisiopatología del incremento del riesgo vascular en la MASLD.
Resistencia a la insulina y dismetabolismo energético
La resistencia a la insulina es el eje central. Conduce a hiperglucemia, hiperinsulinemia y lipólisis excesiva, con aflujo de ácidos grasos libres al hígado y sobrecarga lipídica en múltiples tejidos. Esta situación no solo promueve la esteatosis hepática, sino que deteriora la función endotelial al reducir la biodisponibilidad de óxido nítrico y activar vías proinflamatorias, sentando la base de la aterogénesis23.
Lipotoxicidad, inflamación y estrés oxidativo
El exceso de lípidos tóxicos (diacilglicéridos, ceramidas) induce disfunción mitocondrial y estrés oxidativo, activando la respuesta del retículo endoplásmico y la liberación de citocinas como el factor de necrosis tumoral alfa y la interleucina 6. El resultado es un estado inflamatorio sistémico de bajo grado que acelera la formación y la progresión de placas ateroscleróticas, y contribuye al remodelado miocárdico24.
Disfunción endotelial y aterosclerosis
La disfunción endotelial, caracterizada por una reducción del óxido nítrico y un aumento del estrés oxidativo, junto con la expresión de moléculas de adhesión, favorece la infiltración leucocitaria y la formación de placas. La dislipidemia típica de la MASLD (lipoproteínas de baja densidad [LDL] pequeñas y densas, lipoproteínas de alta densidad [HDL] disfuncionales, hipertrigliceridemia) es altamente aterogénica y refuerza este proceso25,26.
Estado protrombótico
La MASLD se asocia a un fenotipo procoagulante con elevación del factor VIII y resistencia a la proteína C activada. Esta condición contribuye a la mayor incidencia de trombosis arterial y venosa en esta población27.
Microbiota intestinal: el eje emergente de la histidina
La microbiota intestinal representa un puente entre el hígado y el aparato cardiovascular. De particular relevancia es el metabolismo microbiano de la histidina, capaz de generar imidazol-propionato (ImP) a través de bacterias portadoras del gen urdA. Este metabolito, descrito inicialmente en la diabetes y la obesidad, induce resistencia a la insulina, inflamación endotelial y rigidez arterial, y aparece con frecuencia en condiciones íntimamente ligadas a la MASLD. Se ha propuesto el concepto de biotipo ImP+/urdA^high, que confiere un fenotipo de resistencia a la insulina, esteatosis y riesgo vascular inflamatorio. El ImP se perfila como un marcador funcional emergente y una posible diana terapéutica de primer orden para el abordaje del riesgo vascular en la MASLD14–16,28–30.
Regulación neurohormonal y remodelado cardiaco
La activación del sistema nervioso simpático y del eje renina-angiotensina-aldosterona, favorecida por la inflamación y la resistencia a la insulina, contribuye al desarrollo de insuficiencia cardiaca, particularmente con fracción de eyección preservada31.
Genética y heterogeneidad causal
Los estudios de aleatorización mendeliana sugieren que la relación entre esteatosis hepática y enfermedad coronaria depende del mecanismo biológico. Variantes como PNPLA3 o TM6SF2 promueven la esteatosis al tiempo que reducen la secreción de lipoproteínas de muy baja densidad (VLDL), confiriendo un perfil lipídico paradójicamente menos aterogénico. En cambio, otras variantes asociadas a dislipidemia favorecen un RCV neto más alto32.
En conclusión, el incremento del RCV en la MASLD resulta de la convergencia de múltiples vías fisiopatológicas: resistencia a la insulina, lipotoxicidad e inflamación sistémica, disfunción endotelial, fibrosis avanzada, estado protrombótico y remodelado cardiaco33,34. Entre ellas, el metabolismo microbiano de la histidina y la producción de ImP se pueden consolidar como un mecanismo emergente de máxima relevancia, que podría redefinir en el futuro próximo el abordaje terapéutico del riesgo vascular en esta enfermedad.
Conceptos fundamentales en riesgo vascular y eventos cardiovasculares adversos mayores
La comprensión del riesgo vascular es imprescindible para interpretar el pronóstico de los pacientes con MASLD. Aunque la hepatología ha centrado tradicionalmente su atención en los desenlaces hepáticos, la carga de ECV asociada a esta patología obliga a manejar con precisión conceptos y herramientas habitualmente empleados en cardiología y medicina interna.
Definición de riesgo vascular
El término «riesgo vascular» hace referencia a la probabilidad de desarrollar, en un horizonte temporal definido, un evento cardiovascular o cerebrovascular clínicamente relevante. Tradicionalmente se ha limitado al ámbito aterosclerótico, pero en sentido amplio incluye eventos tanto arteriales como venosos. Su magnitud depende de la suma de factores de riesgo clásicos, como hipertensión arterial, diabetes, dislipidemia, tabaquismo y obesidad central, y de determinantes emergentes como la resistencia a la insulina, la inflamación sistémica de bajo grado, la disfunción endotelial y la disbiosis intestinal, cuya relevancia fisiopatológica y pronóstica está cada vez mejor documentada8,35.
Eventos cardiovasculares adversos mayores
Los eventos cardiovasculares adversos mayores (MACE, major adverse cardiovascular events) son los desenlaces clínicos de mayor impacto en la práctica clínica y en la investigación. Su definición estricta, empleada en la mayoría de los ensayos de registro, incluye el infarto de miocardio e ictus isquémico no mortales y la muerte de causa cardiovascular (Fig. 2). En sentido más amplio, el término se extiende para abarcar la hospitalización por angina inestable o insuficiencia cardiaca, las revascularizaciones coronarias, las arritmias graves con compromiso vital y la resucitación tras la muerte súbita. La heterogeneidad en el uso del concepto obliga a interpretar críticamente los resultados de la literatura y dificulta las comparaciones entre estudios36.
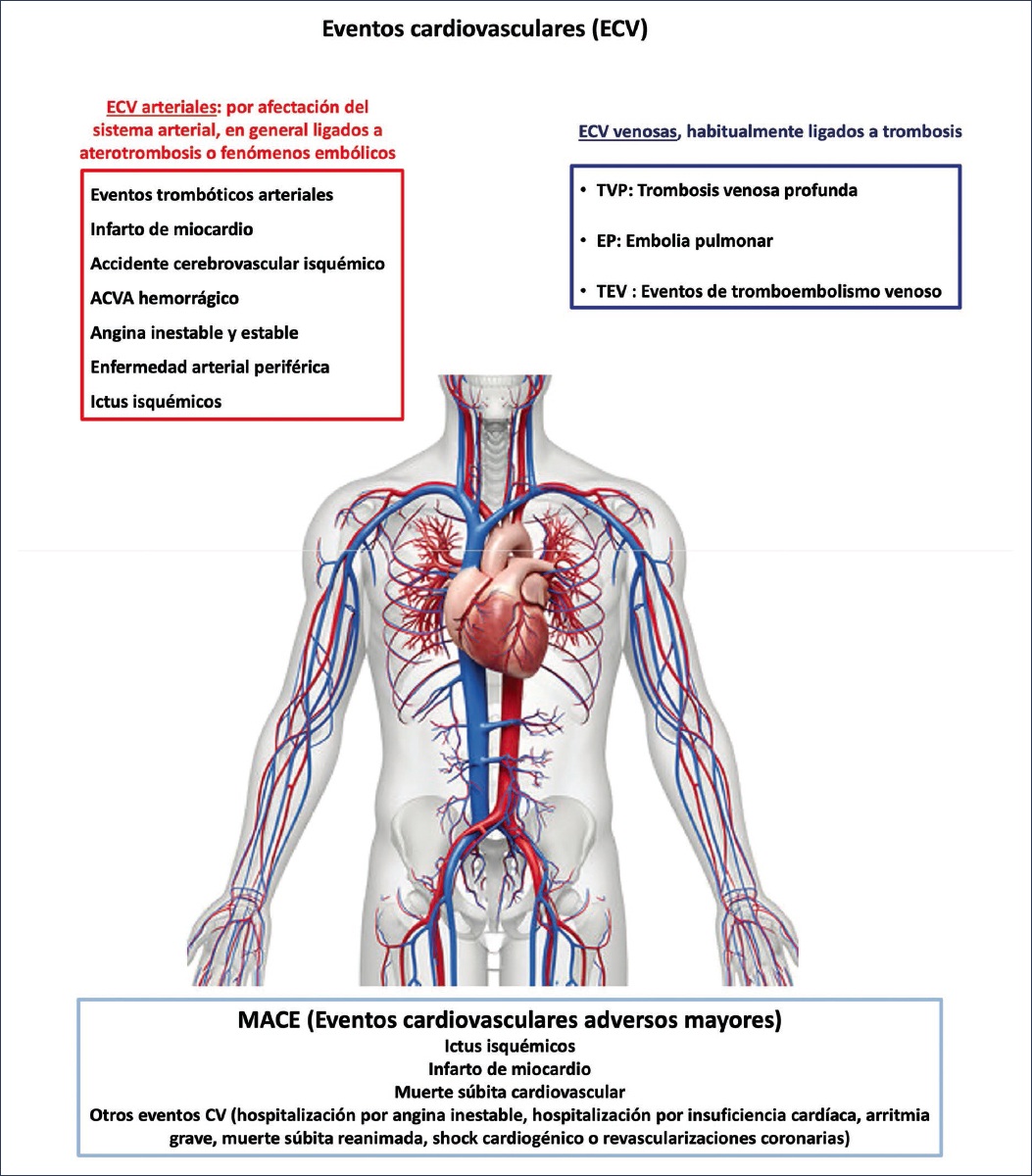
Figura 2. Eventos cardiovasculares asociados que pueden presentarse en los pacientes con MASLD.
Medición clínica del riesgo vascular
La correcta estimación de este riesgo requiere una recogida sistemática de parámetros clínicos y analíticos. La presión arterial debe medirse en condiciones estandarizadas, con dispositivos validados, tras un periodo de reposo y evitando interpretaciones a partir de valores aislados. El perfil lipídico completo (colesterol total, colesterol unido a LDL [C-LDL], colesterol unido a HDL [C-HDL], triglicéridos, colesterol No-HDL y, cuando sea posible, apolipoproteína B) constituye la base de cualquier mod- elo de predicción. No se debe olvidar medir, al menos una vez en la vida, la lipoproteína (a). (Mencionar resistencia a insulina HOMA-IR, inflamcación sistémica PCR-us, congestión NT-ProBNP y daño miocáridco Tropo I). La glucemia en ayunas y la hemoglobina glucosilada (HbA1c) son imprescindibles para detectar diabetes o prediabetes. La cuantificación del índice de masa corporal (IMC) y del perímetro de la cintura permite valorar la adiposidad global y central (y si es posible la determinación de la composición corporal con medición del tejido adiposo visceral mediante BIA, DEXA, BOD-POD, TAC, RMN o PET), y la historia detallada de tabaquismo debe recogerse de manera sistemática. Finalmente, la determinación del cociente albúmina/creatinina en orina añade información crítica: la microalbuminuria refleja daño microvascular no solo renal sino sistémico y se asocia con un incremento independiente del RCV y del riesgo renal, incluso en individuos con filtrado glomerular preservado37.
Herramientas de estratificación del riesgo
La predicción del RCV en población general se apoya en algoritmos validados que combinan la edad, el sexo y los factores de riesgo convencionales. Estas herramientas las analizaremos más adelante.
Daño cardiovascular subclínico
Más allá de los factores de riesgo y los algoritmos clínicos, la detección de daño subclínico aporta una dimensión complementaria38,39. Estos aspectos los abordaremos más adelante.
En conclusión, el hepatólogo debe familiarizarse con los fundamentos del riesgo vascular y del concepto de MACE, así como con las métricas y los parámetros necesarios para su medición. Este marco conceptual es esencial para interpretar el impacto de la MASLD en el pronóstico cardiovascular y para integrar la perspectiva hepática en la prevención vascular contemporánea.
Riesgos cardiovasculares asociados a la MASLD
La MASLD se configura hoy como un determinante cardiovascular sistémico. Su asociación con desenlaces clínicos mayores trasciende el acompañamiento de factores de riesgo clásicos y abarca un espectro amplio que incluye eventos aterotrombóticos, arritmias, insuficiencia cardiaca de predominio diastólico, disfunción microvascular y riesgos específicos en subgrupos seleccionados (Tabla 2). La magnitud del riesgo se incrementa con la progresión de la fibrosis hepática, persiste tras ajustar por confusión cardiometabólica y alcanza incluso a poblaciones tradicionalmente consideradas de menor riesgo, como las mujeres y los adultos jóvenes40.
Tabla 2. Manifestaciones cardiovasculares asociadas a MASLD y nivel de evidencia
| Manifestación cardiovascular | Evidencia epidemiológica | Magnitud del riesgo | Nivel de evidencia (EASL/AASLD) |
|---|---|---|---|
| Infarto de miocardio | Cohortes y metaanálisis | ↑ 1.5-2 veces | Alto |
| Ictus isquémico | Cohortes poblacionales | ↑ 1.5 veces | Moderado |
| Fibrilación auricular | Estudios poblacionales | ↑ 1.2-1.5 veces | Moderado |
| Insuficiencia cardiaca (con fracción de eyección preservada) | Cohortes y metaanálisis | ↑ 2 veces | Alto |
| Mortalidad de causa cardiovascular | Metaanálisis (> 10,000 casos) | Incremento significativo | Alto |
AASLD: American Association for the Study of Liver Diseases; EASL: European Association for the Study of the Liver.
La MASLD se asocia a un incremento independiente del riesgo cardiovascular, con mayor magnitud en presencia de fibrosis avanzada. La insuficiencia cardiaca con fracción de eyección preservada y la mortalidad de causa cardiovascular global destacan como manifestaciones con evidencia más sólida.
Eventos aterotrombóticos (MACE): infarto de miocardio, ictus y muerte de causa cardiovascular
La evidencia contemporánea confirma un exceso de riesgo de MACE que persiste tras ajustar por los factores clásicos y se acentúa cuando coexiste fibrosis hepática significativa40. En términos cuantitativos, el riesgo de cardiopatía isquémica y de infarto de miocardio está aumentado en torno a un 25-30% en los pacientes con MASLD, con independencia de la edad, el sexo y la comorbilidad cardiometabólica, según un metaanálisis que integró aproximadamente 1.2 millones de individuos41. Alon et al.42 confirman este hecho y documentan incrementos significativos del riesgo de infarto, ictus, fibrilación auricular (FA) e insuficiencia cardiaca en estos pacientes. Un metaanálisis posterior demostró mayores morbilidad y mortalidad de causa cardiovascular, incluyendo el fenotipo lean NAFLD43. En el ictus, la relación es igualmente consistente y presenta un gradiente con la fibrosis hepática. Un metaanálisis publicado en Stroke mostró que el riesgo de eventos cerebrovasculares fatales y no fatales aumenta con la gravedad de la MASLD44. En menores de 40 años, una revisión sistemática y metaanálisis de 10.6 millones de personas estimó una hazard ratio (HR) global de 1.63 para eventos cardiovasculares, con incrementos significativos en cardiopatía coronaria, ictus, FA e insuficiencia cardiaca, lo que obliga a anticipar la evaluación vascular cuando coexiste MASLD en edades tempranas45,46. Esta «señal hepática» se traduce clínicamente en una mayor carga de MACE conforme progresa la enfermedad, lo que justifica integrar la estratificación de la fibrosis en la valoración del riesgo vascular40. La evidencia de la práctica real corrobora estos hallazgos. En una cohorte del UK Biobank, la MASLD emergió como un factor independiente de mortalidad por todas las causas y de eventos cardiovasculares adversos; además, añadir la MASLD a los modelos tradicionales mejoró la capacidad de predicción de desenlaces47. Tras un infarto de miocardio, un Fatty Liver Index (FLI) > 60 se asoció con mayor mortalidad de causa cardiovascular a 12 años, independientemente de la obesidad y la diabetes, en la cohorte Alpha Omega48. En una cohorte longitudinal, tanto la persistencia como el desarrollo de esteatosis se vincularon a mayor riesgo de infarto, ictus, insuficiencia cardiaca y mortalidad, frente a quienes no presentaban MASLD; la regresión de la esteatosis se asoció con un perfil de riesgo más favorable, lo que apunta a un componente potencialmente reversible del exceso de riesgo vascular49. En subpoblaciones de alto riesgo, la magnitud del problema es aún mayor, tal como ya hemos señalado. En la diabetes tipo 2 se ha demostrado que la MASLD se asocia con un incremento significativo de ECV y de mortalidad por cualquier causa, con diferencias absolutas de riesgo clínicamente relevantes50. Respecto a la mortalidad de causa cardiovascular y la muerte súbita, la literatura muestra señales heterogéneas. Mientras algunos estudios han observado un aumento claro de la mortalidad de causa cardiovascular, otros detectan un exceso de eventos que no siempre se traducen en mortalidad específica, posiblemente por competencia de riesgos y diferencias metodológicas43. La asociación con la muerte súbita cardiaca es emergente y requiere confirmación prospectiva; en pacientes portadores de un desfibrilador, la presencia de MASLD se ha vinculado a mayor carga de arritmias ventriculares y eventos adversos51. La MASLD constituye un determinante independiente de MACE, con un gradiente de riesgo relacionado con la fibrosis, expresividad alta en la diabetes tipo 2 y presencia significativa en adultos jóvenes. Esta realidad obliga a integrar de manera sistemática la dimensión cardiovascular en la valoración clínica, especialmente cuando la fibrosis o el fenotipo cardiometabólico son relevantes40,47,52 (Tabla 3).
Tabla 3. Evidencia procedente de cohortes y de estudios sobre riesgo cardiovascular en la MASLD
| Estudio/cohorte | Población | Hallazgos principales | Implicaciones en MASLD |
|---|---|---|---|
| MESA77 | Cohorte poblacional multiétnica | PCE mostró estadístico c ≈ 0.69 en esteatosis moderada-grave; subestimación marcada en mujeres | Los modelos clásicos infraestiman el riesgo, en especial en mujeres y en enfermedad avanzada |
| UK Biobank47 | Cohorte poblacional del Reino Unido | MASLD asociada con incremento de MACE y mortalidad de causa cardiovascular | MASLD aporta riesgo adicional no captado por algoritmos convencionales |
| TARGET-NASH18 | Cohorte multicéntrica de práctica clínica | Framingham, PCE y PREVENT con estadístico c 0.58-0.60; mala calibración (sobrestimación en alto riesgo, subestimación en bajo riesgo) | Limitaciones serias de los modelos clásicos en MASLD |
| HEPAMET/ETHON78 | Cohorte clínica vs. poblacional | Pacientes con MASLD mayor prevalencia de eventos cardiovasculares y más categorías elevadas de SCORE; MASH y fibrosis avanzada = predictores independientes de alto riesgo | La fibrosis hepática añade poder pronóstico en la estratificación del riesgo |
| Cohorte cardiometabólica de Atenas79 | Pacientes con factores cardiometabólicos | FIB-4 asociado de forma consistente con lesión arterial subclínica y eventos cardiovasculares; mejora modesta de discriminación | El FIB-4 puede integrarse en modelos de predicción cardiovascular en MASLD |
| NAFLD CV-risk score80 | Modelo específico (edad, volumen plaquetario medio, diabetes) | AUROC ≈ 0.83-0.84 para predecir MACE a 1 año; mejor que Framingham y QRISK2 | Prometedor, pero pendiente de validación externa amplia |
| Metaanálisis en mujeres82 | Mujeres con MASLD | Mayor RCV que en hombres, con amplificación a mayor gravedad hepática | La estratificación debe considerar el sexo como modificador clave |
| Diabetes tipo 1 y MASLD83 | Pacientes con diabetes tipo 1 y MASLD | OR ajustada 4.26 para ASCVD | La coexistencia de MASLD multiplica el riesgo en subgrupos vulnerables |
| Metaanálisis en Jóvenes45 | Población ≤ 40 años | HR agrupada 1.63 para eventos cardiovasculares en MASLD | Justifica la integración temprana de variables hepáticas en los modelos de predicción |
| MASLD vs. MAFLD41,84,85 | Estudios poblacionales | RCV mayor en MAFLD (51.1%) vs. MASLD (35.0%); diferencias en rigidez hepática y gravedad metabólica | MAFLD podría captar mejor el gradiente de riesgo aterosclerótico |
| Grasa pericárdica/periaórtica86 | Estudios de imagen | Mayor volumen asociado con gravedad de MASLD; mejora la predicción al añadirse a factores clásicos | Posible marcador adicional en predicción del riesgo |
ASCVD: enfermedad cardiovascular aterosclerótica; AUROC: área balo la curva ROC; FIB-4: índice de fibrosis basado en 4 factores; HR: hazard ratio; MACE: eventos cardiovasculares adversos mayores; OR: odds ratio; RCV: riesgo cardiovascular.
La evidencia de cohortes muestra que los modelos clásicos infraestiman el riesgo cardiovascular en la MASLD, con especial impacto en las mujeres, los jóvenes y los pacientes con fibrosis avanzada. Los modelos específicos, como el NAFLD CV-risk score, ofrecen mejor discriminación, pero requieren validación externa antes de su aplicación generalizada.
Arritmias: fibrilación auricular y otras
La FA es la arritmia más sólidamente vinculada a la MASLD. Se ha observado un incremento significativo del riesgo de FA en los pacientes con MASLD, asociación que persiste tras ajustar por confusores cardiometabólicos. Un metaanálisis de cohortes confirmó el aumento del riesgo de FA (junto con infarto, ictus e insuficiencia cardiaca)42. En una gran cohorte nacional, la incidencia de FA fue mayor en los pacientes con MASLD y aumentó de forma progresiva con la fibrosis hepática; el exceso fue patente incluso en adultos jóvenes, y se acentuó con la fibrosis avanzada53. Además, un estudio efectuado mediante aleatorización mendeliana sugiere que los fenotipos más graves (p. ej., MASH [Metabolic dysfunction Associated Steato Hepatitis]) podrían relacionarse causalmente con FA, mientras que para la MASLD global la evidencia es menos concluyente54. En conjunto, los hallazgos apoyan considerar la vigilancia de FA en los pacientes con MASLD y fibrosis significativa. Además, se han descrito alteraciones de la repolarización (prolongación y dispersión del QTc) y un posible aumento de las arritmias ventriculares, probablemente mediadas por inflamación sistémica, disfunción autonómica y fibrosis miocárdica difusa55. La asociación entre fibrosis hepática y FA refuerza el papel del daño estructural hepático como marcador de riesgo arrítmico56. En la MASLD con fibrosis significativa o fenotipos de alto riesgo, resulta aconsejable incorporar un cribado oportunista de FA (pulsos/electrocardiograma) y revisar los factores proarrítmicos (electrolitos, prolongadores de QT).
«Cardiomiopatía de la MASLD»: disfunción diastólica e insuficiencia cardiaca con fracción de eyección preservada
La cardiomiopatía asociada a la MASLD se manifiesta por remodelado auricular y ventricular izquierdo, disfunción diastólica y elevación de las presiones de llenado. Un metaanálisis de 31 estudios demostró un mayor volumen auricular izquierdo, masa ventricular izquierda y, sobre todo, deterioro de la función diastólica en la MASLD57. Esta alteración estructural-funcional se traduce en mayor riesgo de insuficiencia cardiaca incidente, con un exceso más marcado para insuficiencia cardiaca con fracción de eyección preservada frente a fracción de eyección reducida en análisis poblacionales58. Una revisión realizada por Mantovani et al.59 sintetiza la evidencia clínica y traslacional que vincula la MASLD con la insuficiencia cardiaca con fracción de eyección preservada, proponiendo a la MASLD como fenotipo de cardiometabolismo adverso con afectación miocárdica y vascular difusa. En pacientes con MASLD y disnea de esfuerzo, edema o elevación del propéptido natriurético cerebral N-terminal (NT-proBNP), la sospecha de insuficiencia cardiaca con fracción de eyección preservada debe plantearse de manera temprana; la coexistencia de obesidad, diabetes tipo 2, hipertensión arterial y fibrosis hepática incrementa la probabilidad pretest y justifica una evaluación cardiológica estructurada.
Enfermedad microvascular y subclínica
Los marcadores de daño vascular silencioso están aumentados en la MASLD. En una revisión que incluyó 59 estudios (16,179 casos y 26,120 controles), la MASLD se asoció a un incremento absoluto de 0.123 mm en el grosor íntima-media carotídeo (≈20.6%)60. La rigidez de la pared arterial está aumentada tanto en la MASLD como en la MAFLD (Metabolic-Associated Fatty Liver Disease), con asociaciones más intensas en la MAFLD y en las mujeres61. En cuanto a la microcirculación coronaria, la MASLD se asocia a disfunción microvascular (reducción de la reserva de flujo), lo que sugiere una base funcional para la mayor propensión a isquemias significativas62. En personas con diabetes tipo 2 y MASLD, la fibrosis evaluada por el índice de fibrosis basado en 4 factores (FIB-4) o por la NAFLD Fibrosis Score (NFS) se asocia de forma independiente con el calcio coronario (CAC) y mejora, modestamente, la estratificación coronaria25. En paralelo, la regresión de la esteatosis se ha asociado a menor progresión del CAC, apoyando la modificabilidad del riesgo vascular63. La afectación microvascular renal (albuminuria, filtrado glomerular) es más prevalente en la MASLD, con aproximadamente 1.45 veces más riesgo de enfermedad renal crónica incidente en el largo plazo64. La presencia de daño vascular subclínico refuerza la indicación de intensificar la prevención cardiovascular. En hepatología, su utilidad es mayor cuando esta evaluación puede cambiar decisiones (p. ej., reclasificar un riesgo dudoso o priorizar terapias cardiometabólicas).
Otros riesgos específicos
DIABETES TIPO 1
En los adultos con diabetes tipo 1, la coexistencia de esteatosis y fibrosis significativa se asocia a un incremento muy sustancial del RCV estimado a 10 años, frente a la diabetes tipo 1 sin esteatosis o con esteatosis sin fibrosis. Este hallazgo se mantuvo en todos los subgrupos por sexo, edad, HbA1c y función renal65.
HIPERTENSIÓN
La MASLD incrementa un 66% el riesgo de hipertensión arterial incidente, con mayores prevalencias a medida que aumentan los estratos de presión arterial; además, la coexistencia de MASLD se asocia a mayor mortalidad total y por causa cardiovascular en los sujetos hipertensos, lo que puede traducirse en más casos de hipertensión arterial resistente66,67.
DETERIORO COGNITIVO Y DEMENCIA
La relación entre integridad hepática y función cognitiva es un tema en evaluación. Un estudio nacional mostró que un FIB-4 alto se asocia con un 18% más de riesgo de demencia incidente, incluso tras ajustes amplios68. Sin embargo, otros análisis poblacionales (UK Biobank) no han confirmado un exceso global cuando se usa el FLI como proxy de MASLD, por lo que la causalidad permanece abierta69.
TROMBOEMBOLIA VENOSA
Los estudios poblacionales recientes sugieren un mayor riesgo de tromboembolia venosa en los pacientes con MASLD. En Corea, la presencia de MASLD se asoció a más eventos de tromboembolia venosa en seguimiento, mientras que en el Tromsø Study los valores elevados de FLI se relacionaron con tromboembolia venosa incidente, si bien parte de la asociación se explicó por adiposidad general70,71. La señal es emergente y requiere confirmación con medidas directas de hígado graso y ajuste fino por obesidad central.
Desempeño de puntuaciones de riesgo generales e incorporación de la «señal hepática»
Los algoritmos clásicos (PCE/SCORE2/Framingham) muestran limitaciones de calibración y discriminación en la MASLD, con subestimación del riesgo en las mujeres y en esteatosis moderada-grave. La incorporación de marcadores hepáticos no invasivos, en especial el FIB-4, aporta valor incremental sobre los sistemas convencionales y parece mediar parte de su efecto a través de lesión vascular, según análisis contemporáneos del Athens Cardiometabolic Registry y de cohortes integradas72. Adicionalmente, el Steatosis-associated Fibrosis Estimator score (SAFE) muestra utilidad para estratificar la fibrosis y facilitar circuitos asistenciales que conectan decisiones hepáticas y cardiovasculares73.
Genética y causalidad
Los estudios de aleatorización mendeliana indican que el vínculo entre esteatosis y cardiopatía coronaria depende del mecanismo lipídico subyacente: cuando se excluyen variantes que reducen la secreción hepática de VLDL (p. ej., PNPLA3, TM6SF2, APOB y MTTP), la asociación con enfermedad de las arterias coronarias emerge con mayor claridad; en cambio, agregarlas diluye o invierte la señal, al acompañarse de perfiles de lipoproteínas «aparentemente favorables»74,75. Esta biología divergente ayuda a explicar por qué no toda «grasa hepática» confiere el mismo RCV, y refuerza el énfasis clínico en fenotipificar más allá de la esteatosis (fibrosis, dislipidemia aterogénica, resistencia a la insulina, inflamación).
La evidencia disponible sitúa a la MASLD como un determinante cardiovascular sistémico: incrementa los MACE, favorece la FA, se asocia a un fenotipo de insuficiencia cardiaca con fracción de eyección preservada, presenta una huella microvascular/subclínica amplia y agrava los riesgos en escenarios específicos (diabetes tipo 1, hipertensión, posible deterioro cognitivo, tromboembolia venosa). El gradiente por fibrosis es un elemento transversal. En hepatología, esto implica documentar sistemáticamente la dimensión cardiovascular, reconocer subgrupos de alto riesgo y considerar la derivación temprana a unidades de riesgo vascular cuando la carga de riesgo o el daño de órgano diana lo aconsejen.
Evaluación del riesgo cardiovascular en la MASLD
Importancia de la clasificación del riesgo
La estratificación del RCV constituye un pilar esencial en la atención a los pacientes con MASLD, ya que la ECV es su principal causa de mortalidad. Su adecuada clasificación permite identificar a individuos sin ECV manifiesta, pero con riesgo elevado, lo que posibilita la implementación precoz de medidas preventivas, además de orientar la intensidad de las intervenciones y fijar objetivos terapéuticos concretos de presión arterial, C-LDL o HbA1c.
Medición clínica de los factores de riesgo
El primer paso consiste en la medición clínica sistemática de los factores de riesgo clásicos: presión arterial, perfil lipídico completo, glucemia y HbA1c, IMC, perímetro abdominal, tabaquismo y antecedentes familiares de ECV prematura. Esta aproximación básica constituye el pilar sobre el que se construye la estratificación pronóstica en la MASLD (Fig. 3).
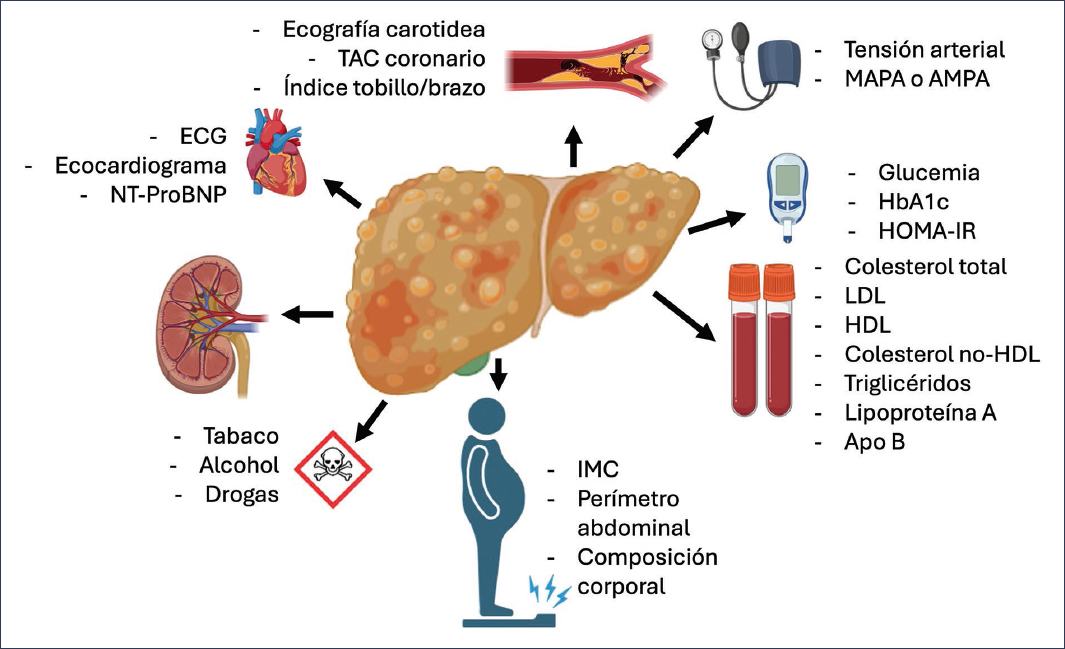
Figura 3. Evaluación del riesgo cardiovascular en el paciente con MASLD. AMPA: automedición de la presión arterial; ECG: electrocardiograma; HbA1c: hemoglobina glucosilada; HDL: lipoproteínas de alta densidad; IMC: índice de masa corporal; LDL: lipoproteínas de baja densidad; MAPA: monitorización ambulatoria de la presión arterial; TAC: tomografía computarizada.
Calculadoras de riesgo cardiovascular y clasificación (Tabla 4)
Tabla 4. Modelos de determinación del riesgo cardiovascular y su aplicabilidad en los pacientes con MASLD
| Modelo | Variables principales incluidas | Limitaciones en MASLD | Posibles ajustes o consideraciones prácticas |
|---|---|---|---|
| Framingham Risk Score (FRS) | Edad, sexo, tabaquismo, presión arterial, colesterol total, HDL, glucemia | Tiende a infravalorar el riesgo cardiovascular en MASLD (estadístico c ≈ 0.58 en cohortes específicas) | Puede complementarse con marcadores hepáticos (p. ej., FIB-4). |
| Pooled Cohort Equations (PCE) | Edad, sexo, lípidos, hipertensión arterial, diabetes, tabaquismo | Desempeño similar a FRS; infravalora el riesgo residual en MASLD | Ajustar con fibrosis hepática o imagen vascular. |
| SCORE2/SCORE2-OP | Edad, sexo, presión arterial, lípidos, tabaquismo, región europea de riesgo | Diseñado para población europea; en MASLD también tiende a infravalorar el riesgo | Posible recalibración incorporando fibrosis o biomarcadores hepáticos |
| PREVENT (AHA, 2023) | Factores clásicos + renales (TFGe, albúmina/creatinina), HbA1c, indicadores sociales | No validado específicamente en MASLD; desempeño ligeramente mejor que FRS/PCE (estadístico c ≈ 0.60 en algunas cohortes) | Potencialmente útil en MASLD con comorbilidad metabólica y renal, aún sin validación formal |
| Submodelos PREVENT | PREVENT–CVD (enfermedad cardiovascular global), PREVENT–ASCVD (enfermedad aterosclerótica), PREVENT–HF (insuficiencia cardiaca) | Aumenta granularidad del riesgo, pero no validado en MASLD | Puede ayudar a identificar riesgo de insuficiencia cardiaca con fracción de eyección preservada) relevante en MASLD |
| SAFE score | Riesgo cardiovascular integrado con biomarcadores hepáticos (ej. FIB-4, ELF) | Validación inicial en cohortes MASLD, aún limitada | Muy prometedor como herramienta cardio-hepato-metabólica |
ELF: enhanced liver fibrosis; FIB-4: índice de fibrosis basado en 4 factores; HbA1c: hemoglobina glucosilada; HDL: lipoproteínas de alta densidad; TFGe: tasa de filtrado glomerular estimada.
Los modelos clásicos de riesgo cardiovascular han sido validados en población general y se utilizan ampliamente en la práctica clínica, pero muestran un rendimiento limitado en los pacientes con MASLD, ya que tienden a infraestimar el riesgo residual debido a que no incluyen variables hepáticas ni metabólicas propias de esta enfermedad. El modelo PREVENT, desarrollado por la American Heart Association en 2023, supone un avance respecto a las ecuaciones tradicionales porque incorpora parámetros renales (filtrado glomerular, albuminuria), glucémicos (HbA1c) y sociales (índice de privación), además de ofrecer distintos submodelos (PREVENT-CVD, PREVENT-ASCVD, PREVENT-HF). Aunque mejora modestamente la discriminación, aún no ha sido validado específicamente en la MASLD y debe usarse con cautela en este contexto. La plataforma U-Prevent no es un modelo en sí mismo, sino una herramienta digital que permite calcular distintos modelos (incluidos FRS, SCORE2, PREVENT) y compararlos en la práctica clínica. Puede ser útil para hepatólogos como recurso práctico. El SAFE score, que integra factores cardiovasculares y hepáticos (p. ej., FIB-4, ELF), surge como un modelo adaptado a la MASLD y podría convertirse en la herramienta más apropiada para la estratificación cardio-hepato-metabólica, aunque su validación aún es preliminar. En la práctica, la mejor estrategia es combinar modelos tradicionales con información hepática adicional (fibrosis, biomarcadores o imagen no invasiva), hasta disponer de modelos validados específicamente para la MASLD.
La predicción del RCV en la población general se fundamenta en algoritmos validados que combinan edad, sexo y factores de riesgo convencionales, entre los que destacan las Pooled Cohort Equations (PCE) recomendadas en los Estados Unidos de América, el SCORE2 de uso extendido en Europa, y el algoritmo de Framingham, considerado el estándar de referencia77,78. Estos modelos estiman la probabilidad de presentar un evento cardiovascular mayor a 10 años y permiten clasificar a los individuos en categorías de riesgo (bajo, moderado, alto o muy alto), constituyendo la base para la toma de decisiones preventivas19 y terapeúticas. No obstante, presentan limitaciones en determinados subgrupos, como las mujeres jóvenes y los pacientes con hepatopatía metabólica, en quienes tienden a subestimar el riesgo real19,38. En este contexto, las guías ESC 2021 recomiendan el SCORE2 como herramienta de referencia19, mientras que la guía ACC/AHA 2025 introduce una aproximación basada en el riesgo global mediante la calculadora PREVENT, enfatiza la necesidad de instaurar tratamiento precoz y adapta las recomendaciones a subpoblaciones específicas como mujeres embarazadas y pacientes con enfermedad renal, hipertensión resistente o deterioro cognitivo, configurándose así como una herramienta práctica y accesible para la estratificación del riesgo en la práctica clínica22. Finalmente, el SAFE, concebido inicialmente para la estratificación de la fibrosis en atención primaria, se ha planteado también como una estrategia de priorización cardiovascular20.
Limitaciones de los sistemas de predicción del riesgo en los pacientes con MASLD
Los modelos tradicionales no fueron diseñados para poblaciones con hepatopatía y presentan defectos de discriminación y calibración. En el estudio MESA, las PCE mostraron una capacidad discriminativa modesta (estadístico c: ≈0.69), que descendía hasta casi 0.65 en pacientes con esteatosis moderada-grave, con una marcada subestimación del riesgo en las mujeres77. De manera concordante, en el UK Biobank, la presencia de MASLD se asoció con un incremento de los MACE y de la mortalidad por causa cardiovascular, pero la inclusión de esta variable en los modelos tradicionales apenas mejoró la predicción47.
El estudio multicéntrico TARGET-NASH confirmó que Framingham, PCE y PREVENT rendían pobremente en la MASLD, con un estadístico centre 0.58 y 0.60, y mala calibración18. Estos defectos se traducen en una infraestimación del riesgo en las mujeres, los adultos jóvenes y el fenotipo metabólicamente sano.
Un aspecto adicional es la influencia de los eventos competitivos (cirrosis, hepatocarcinoma), que pueden sesgar las estimaciones de riesgo si se aplican modelos de Cox estándar. En este contexto, es preferible emplear funciones de incidencia acumulada o modelos de subdistribución de Fine-Gray para analizar de forma más precisa el RCV y el riesgo no cardiovascular en los pacientes con MASLD80,81.
Evidencia de cohortes clínicas y biomarcadores
En el registro HEPAMET, comparado con la cohorte poblacional ETHON, los pacientes con MASLD presentaban mayor prevalencia de eventos cardiovasculares y alcanzaban con más frecuencia categorías elevadas de SCORE, incluso tras excluir la ECV previa. La presencia de MASH y, sobre todo, de fibrosis avanzada, se asoció de manera independiente con alto riesgo, lo que subraya la relevancia pronóstica de la señal hepática78. Entre los biomarcadores, el FIB-4 ha demostrado una asociación consistente con lesión arterial subclínica y con eventos cardiovasculares, mejorando modestamente la discriminación de los modelos y asociándose a mayor mortalidad con puntos de corte elevados79. Asimismo, se han desarrollado modelos específicos, como el NAFLD CV-risk score, que combina la edad, el volumen plaquetario medio y la diabetes, con un área bajo la curva ROC (Receiver Operating Characteristic) de 0.83-0.84 para predecir MACE a 1 año, superando a Framingham y QRISK2, aunque todavía requiere validación externa80. El SAFE, inicialmente concebido para estratificar la fibrosis hepática, se ha validado también como herramienta útil para identificar individuos con mayor vulnerabilidad vascular20,79. Estos hallazgos ilustran un aspecto fundamental: los biomarcadores y los índices diseñados para la estratificación hepática aportan, con un cambio de perspectiva, valor pronóstico cardiovascular.
Subgrupos clínicos y fenotipos diagnósticos
Determinados subgrupos clínicos presentan vulnerabilidades específicas. En un metaanálisis, las mujeres con MASLD mostraron mayor RCV que los hombres, con amplificación cuanto mayor era la gravedad hepática82. En la diabetes tipo 1, la coexistencia de MASLD se asocia con un incremento marcado del riesgo aterosclerótico (odds ratio ajustada: 4.26 para enfermedad cardiovascular aterosclerótica [ASCVD])83. En población joven (≤ 40 años), un metaanálisis informó una HR agrupada de 1.63 para eventos cardiovasculares en la MASLD45.
Los fenotipos diagnósticos también influyen. El constructo MAFLD (no mencionado previamente ni definido), al integrar criterios metabólicos, capta mejor el gradiente aterosclerótico que la MASLD. Los estudios han mostrado mayor riesgo en la MAFLD (51.1%) que en la MASLD (35.0%), con diferencias en rigidez hepática y gravedad metabólica41,84,85. Por otra parte, el volumen de grasa pericárdica y periaórtica se asocia a mayor gravedad de las MASLD y mejora la predicción cuando se añade a los factores clásicos del síndrome metabólico86.
Evaluación no invasiva de la enfermedad cardiovascular subclínica (Tabla 5)
Tabla 5. Biomarcadores y técnicas de imagen para la evaluación subclínica del riesgo cardiovascular en pacientes con MASLD
| Parámetro | Descripción | Hallazgos en MASLD | Implicaciones clínicas |
|---|---|---|---|
| Microalbuminuria87 | Marcador clásico de disfunción endotelial y daño renal precoz | Asociada con mayor rigidez arterial y mortalidad de causa cardiovascular, incluso sin enfermedad renal establecida | Identifica disfunción vascular precoz; cribado sencillo y coste-efectivo |
| PCR ultrasensible/IL-624 | Biomarcadores inflamatorios | Elevadas en MASLD; se correlacionan con progresión de aterosclerosis y mayor incidencia de eventos | Indican inflamación sistémica; potencial para estratificación adicional del riesgo |
| Troponina ultrasensible88 | Marcador de daño miocárdico subclínico | Niveles más altos en MASLD con fibrosis avanzada, incluso sin cardiopatía clínica | Detecta disfunción ventricular temprana; útil en alto riesgo |
| NT-proBNP88 | Marcador de estrés parietal cardiaco | Elevado en MASLD; se asocia con fibrosis avanzada y riesgo de insuficiencia cardiaca | Ayuda a identificar riesgo de insuficiencia cardiaca con fracción de eyección preservada |
| FIB-4/MASLD fibrosis score25,79 | Índices séricos de fibrosis hepática | Asociados con aterosclerosis coronaria, progresión de CAC y eventos cardiovasculares | Biomarcadores hepáticos que aportan valor pronóstico cardiovascular |
| SAFE score79 | Sistema diseñado para fibrosis en atención primaria | Útil para identificar individuos con mayor vulnerabilidad vascular | Herramienta de priorización práctica en estratificación integrada |
| CAC63 | Tomografía computarizada para cuantificación de calcificación coronaria | Predictor más robusto de aterosclerosis subclínica; progresión más rápida en MASLD; enlentecimiento con regresión de esteatosis | Justifica reclasificación a riesgo alto; marcador independiente de eventos |
| Ecografía carotídea89 | Valoración de placas y de grosor íntima-media | Mayor prevalencia de ateromatosis en MASLD, independiente de factores clásicos | Técnica accesible; útil para detección precoz en riesgo intermedio |
| Velocidad de onda de pulso90 | Medida de rigidez arterial | Aumentada en MASLD; se correlaciona con el grado de fibrosis hepática | Refuerza el concepto de remodelado vascular paralelo al hepático |
| Resonancia magnética cardiaca91 | Técnica avanzada para estructura y función miocárdica | Detecta disfunción ventricular y fibrosis difusa en MASLD sin cardiopatía previa | Herramienta de investigación; anticipa riesgo de insuficiencia cardiaca con fracción de eyección preservada |
CAC: calcio coronario; FIB-4: índice de fibrosis basado en 4 factores; NT-proBNP: propéptido natriurético cerebral N-terminal; PCR: proteína C reactiva.
Los biomarcadores analíticos y las técnicas de imagen aportan información complementaria a los modelos clásicos, permitiendo detectar daño vascular o miocárdico subclínico en los pacientes con MASLD. El CAC y la ecografía carotídea son las herramientas más validadas para la reclasificación del riesgo, mientras que biomarcadores como la troponina, el NT-proBNP y el FIB-4 ofrecen perspectivas innovadoras para la integración cardio-hepato-metabólica.
La aproximación clínica puede ser insuficiente para captar la magnitud real del riesgo. En este contexto, la evaluación no invasiva adquiere un papel crucial.
BIOMARCADORES ANALÍTICOS
La microalbuminuria, marcador de disfunción endotelial, se asocia en la MASLD con rigidez arterial y mortalidad de causa cardiovascular, incluso sin enfermedad renal establecida87. La proteína C reactiva ultrasensible y citocinas como la interleucina 6 se correlacionan con progresión aterosclerótica y mayor incidencia de eventos24. La troponina ultrasensible y el NT-proBNP detectan disfunción miocárdica subclínica, con niveles más altos en los pacientes con fibrosis avanzada aun sin cardiopatía conocida88. HOMA IR. Además, índices séricos de fibrosis hepática como el FIB-4 y el MASLD fibrosis score se han vinculado con mayor prevalencia de aterosclerosis coronaria y progresión del CAC, incluso en pacientes diabéticos25.
TÉCNICAS DE IMAGEN
El CAC es el marcador más robusto de aterosclerosis subclínica y predice la incidencia de eventos en los pacientes con MASLD, con progresión más acelerada que en los controles y enlentecimiento si se logra la regresión de la esteatosis63. La ecografía carotídea muestra mayor prevalencia de placas y grosor íntima-media aumentado (técnica en desuso) en la MASLD, independientemente de los factores clásicos89. La rigidez arterial evaluada por la velocidad de onda de pulso se correlaciona con fibrosis hepática90 ECG y ecocardio. Finalmente, la resonancia magnética cardiaca ha permitido detectar disfunción ventricular y fibrosis difusa en pacientes con MASLD sin cardiopatía conocida, anticipando un riesgo de insuficiencia cardiaca con fracción de eyección preservada91.
Guías clínicas y aplicabilidad práctica
Las guías recientes refuerzan la necesidad de integrar estos hallazgos. La guía ESC/ESH 2024 de hipertensión arterial destaca la importancia de medir la presión arterial de manera estandarizada e identificar daño de órgano diana21. Las guías EASL-EASD-EASO 2024 reconocen a la MASLD como un factor de riesgo independiente y a la fibrosis avanzada como un determinante pronóstico20. Por su parte, la guía ACC/AHA 2025 recomienda PREVENT como modelo global, con apartados específicos para mujeres embarazadas y pacientes con enfermedad renal, hipertensión resistente o deterioro cognitivo22.
La aplicabilidad de estas herramientas en la práctica clínica no debe entenderse como un mandato universal. Su mayor utilidad se observa en pacientes con riesgo intermedio, en aquellos con resultados discordantes entre la clínica y los sistemas de puntuación tradicionales, o cuando existe sospecha de daño vascular no explicado por los factores habituales. En la mayoría de los casos, la evaluación avanzada y la interpretación de estos hallazgos deben corresponder a especialistas en RCV, idealmente en unidades multidisciplinarias que integren hepatología, cardiología, endocrinología y nefrología. El cometido del hepatólogo consiste en identificar a los pacientes candidatos a esta valoración y propiciar su derivación, asegurando así una atención verdaderamente integral en una enfermedad cuya principal amenaza pronóstica trasciende al hígado.
Mensajes clave para la práctica
- −La estratificación del RCV debe realizarse en todos los pacientes con MASLD, incluso sin enfermedad cardiovascular conocida.
- −La fibrosis significativa (≥ F2) justifica reclasificar el riesgo hacia categorías más altas.
- −Los sistemas clásicos de determinación del riesgo pueden complementarse con biomarcadores hepáticos, metabólicos, cardiovasculares o pruebas de imagen vascular.
- −La detección de ECV subclínica exige medidas preventivas intensivas.
- −La derivación a unidades multidisciplinarias mejora la integración asistencial y la prevención cardiovascular en los pacientes con MASLD.
Manejo del riesgo cardiovascular en la MASLD
Recomendaciones basadas en la evidencia para dieta, ejercicio y pérdida ponderal
El tratamiento de la MASLD se basa principalmente en una modificación intensiva del estilo de vida, ya que es la estrategia más efectiva para mejorar tanto las complicaciones hepáticas como el RCV. Actualmente no existe ninguna terapia farmacológica que iguale los beneficios de la pérdida de peso, la mejora de la dieta y el aumento de la actividad física20,92,93.
Las guías clínicas recomiendan una pérdida de peso sostenida del 7-10%, con metas intermedias del 3-5% en los primeros meses para favorecer la adherencia20. La dieta debe ser personalizada según las preferencias, la cultura y el estilo de vida del paciente, priorizando patrones alimentarios saludables94. La dieta mediterránea es la más respaldada, especialmente en su variante rica en polifenoles95–97, pero la dieta DASH (Dietary Approaches to Stop Hypertension) y los patrones vegetarianos saludables también son opciones válidas98–100. La clave es una alimentación hipocalórica que el paciente pueda mantener a largo plazo, con reducción de azúcares libres, en especial de la fructosa y las bebidas azucaradas101–103. También pueden considerarse estrategias como el ayuno intermitente o la alimentación con restricción horaria, siempre bajo supervisión profesional104,105.
En relación con el consumo de sustancias, se recomienda la abstinencia total de alcohol, incluso en pequeñas cantidades, debido a su efecto negativo sobre la fibrosis hepática y el RCV106. En contraste, el consumo habitual de café (2-3 tazas al día) se asocia a beneficios hepáticos y metabólicos, gracias a sus compuestos antioxidantes107,108.
La actividad física es fundamental en el manejo de la MASLD, incluso sin una pérdida de peso significativa. Se recomienda combinar ejercicio aeróbico y de fuerza, con un mínimo de 150 minutos semanales de actividad aeróbica moderada o 75 minutos vigorosa, además de dos o tres sesiones semanales de entrenamiento de fuerza109,110. El ejercicio de alta intensidad por intervalos también es una opción eficaz111,112. Es importante reducir el tiempo de sedentarismo, incorporando pausas activas durante el día y fomentando movimientos cotidianos como caminar, subir escaleras o realizar estiramientos breves, lo que favorece la adherencia a largo plazo113.
Otras recomendaciones
El sueño debe ser evaluado como parte del abordaje integral de la MASLD, ya que la apnea obstructiva del sueño es frecuente en estos pacientes y se asocia a mayor riesgo de fibrosis hepática114. Se recomienda realizar cribado sistemático (escala Stop-Bang o escala de somnolencia de Epworth) y, si se detecta riesgo, derivar a una unidad del sueño. El tratamiento con presión positiva continua en la vía respiratoria, junto con la pérdida de peso, puede mejorar la evolución hepática y el RCV115.
El tabaquismo también contribuye a la progresión de la MASLD, por lo que debe recomendarse su abandono total19,116,117. De forma complementaria, se ha identificado que el exposoma, es decir, la exposición a contaminantes ambientales, como partículas finas y dióxido de nitrógeno, aumenta el riesgo de desarrollar o empeorar la enfermedad, por lo que debe considerarse dentro del enfoque preventivo118,119.
Finalmente, el éxito de cualquier intervención en la MASLD depende en gran medida del acompañamiento conductual20. Es fundamental establecer objetivos realistas, realizar un seguimiento estructurado, identificar barreras individuales y ofrecer apoyo continuo. Herramientas como el autorregistro, la retroalimentación frecuente, el uso de tecnologías móviles y el soporte de equipos multidisciplinarios, incluyendo psicólogos o coaches de salud, son clave para mantener los cambios a largo plazo y mejorar los resultados clínicos113,120.
Uso racional de las terapias farmacológicas en la MASLD: un marco integrado cardio-RENO-hepato-metabólico (Tabla 6)
Tabla 6. Opciones terapéuticas en la MASLD y riesgo cardiovascular
| Intervención | Efecto hepático | Efecto cardiovascular | Coste y disponibilidad |
|---|---|---|---|
| Pérdida de peso (7-10%) | ↓ Esteatosis, mejora fibrosis | ↓ Riesgo global | Muy coste-efectiva |
| Dieta mediterránea o DASH | Mejora esteatosis | ↓ Eventos cardiovasculares | Alta disponibilidad |
| Ejercicio regular | ↓ Esteatosis, mejora sensibilidad a insulina | ↓ Riesgo cardiovascular, mejora VO2máx | Muy coste-efectiva |
| Estatinas | Seguras, ↓ esteatosis leve | ↓ Mortalidad de causa cardiovascular | Bajo coste |
| Agonistas del receptor de GLP-1 | ↓ Grasa hepática, mejora NASH | ↓ MACE (en diabetes tipo 2) | Alto coste |
| Inhibidores del SGLT2 | ↓ Esteatosis hepática | ↓ Insuficiencia cardiaca y mortalidad de causa cardiovascular | Alto coste |
| Resmetirom | ↓ Fibrosis histológica | Aún sin datos cardiovasculares robustos | Coste elevado, disponibilidad restringida |
DASH: Dietary Approaches to Stop Hypertension; GLP-1: péptido similar al glucagón tipo 1; MACE: eventos cardiovasculares adversos mayores; SGLT2: cotransportador de sodio y glucosa tipo 2; VO2máx: consumo máximo de oxígeno.
Las intervenciones más coste-efectivas siguen siendo la modificación del estilo de vida y el uso de estatinas. Los fármacos innovadores (agonistas de GLP-1, inhibidores de SGLT2, resmetirom) deben priorizarse en subgrupos de alto riesgo, por su disponibilidad limitada y elevado coste.
La farmacoterapia en la MASLD debe entenderse como parte de una estrategia global que no se limita al hígado, sino que integra la prevención y el tratamiento del RCV y del riesgo metabólico. Tanto las guías europeas conjuntas EASL-EASD-EASO de 202420 como la guía de la American Association for the Study of Liver Diseases (AASLD) de 2023121 coinciden en que la fibrosis hepática, más que la inflamación, es el determinante pronóstico más robusto de mortalidad global y por causa cardiovascular. Ello implica que la intensidad de la intervención farmacológica debe graduarse según la presencia de fibrosis significativa (≥ F2), que marca un fenotipo de riesgo vascular avanzado y exige una estrategia intensiva de control de lípidos, presión arterial, glucemia y peso corporal.
ESTATINAS Y OTROS HIPOLIPIDEMIANTES: LA BASE OLVIDADA
Las estatinas constituyen una piedra angular del manejo farmacológico en la MASLD. Son capaces de reducir el C-LDL y la apoB, y consecuentemente el riesgo vascular de forma segura. Un análisis post hoc del estudio GREACE demostró que su uso en pacientes con enfermedad coronaria y alteraciones hepáticas leves no solo redujo los eventos cardiovasculares, sino que incluso mejoró los parámetros hepáticos122. Sin embargo, siguen infraprescribiéndose en la práctica clínica. En pacientes de alto o muy alto riesgo, los objetivos lipídicos deben ser estrictos, definidos en términos de C-LDL C-No-HDL y apoB, siguiendo las recomenda- ciones de la ESC de 202119. Cuando no se alcanza la meta con estatinas de alta intensidad, se debe añadir ezetimiba, y ante la persistencia del riesgo, recurrir a la asociación con ácido bempedoico, inhibidores de la proproteína convertasa subtilisina/ kexina tipo 9 (PCSK9) O inclisirán123. La lipoproteína (a) constituye un factor hereditario de riesgo residual y puede justificar en el futuro el uso de terapias específicas, como pelacarsen u olpasirán124.
INCRETINAS Y AGONISTAS DEL RECEPTOR DEL PÉPTIDO SIMILAR AL GLUCAGÓN TIPO 1 (GLP-1): UN CAMBIO DE PARADIGMA
Los agonistas del receptor del GLP-1 han pasado de ser agentes hipoglucemiantes para convertirse en terapias de modulación multiorgánica. En marzo de 2025, la Food and Drug Administration (FDA) aprobó la semaglutida para la MASH con fibrosis significativa al producir la resolución histológica de NASH (Non-Alcoholic Steatohepatitis) en un 62.9% de los pacientes125 y mejoría de fibrosis. Además, el ensayo SELECT, con más de 17,600 pacientes con obesidad y ECV sin diabetes, documentó una reducción del 20% en los MACE126. La liraglutida mostró también resolución de la NASH en el ensayo LEAN (39% vs. 9% con placebo)127 y reducción de los eventos cardiovasculares en el estudio LEADER128. La semaglutida, por su parte, redujo los MACE en el ensayo SUSTAIN-6129.
El futuro inmediato es aún más ambicioso. Los agonistas dobles del GLP-1 y del polipéptido insulinotrópico dependiente de glucosa (GIP), como la tirzepatida, han demostrado pérdidas de peso superiores al 20% y mejoras hepáticas significativas130. Los agonistas del GLP-1 y del glucagón, como la cotadutida, han mostrado reducciones de la grasa hepática y de los triglicéridos131. Y los agonistas triples, como la retatrutida, han logrado reducciones de peso del 24 % y descensos notables de la grasa hepática en estudios de fase II132. Así, los fármacos incretínicos han dejado de ser «antidiabéticos» para situarse en el centro de un arsenal cardio-hepato-metabólico.
INHIBIDORES DEL COTRANSPORTADOR DE SODIO Y GLUCOSA TIPO 2 (SGLT2): NEFRO- Y CARDIOPROTECCIÓN EN UN SOLO PASO
Los inhibidores del SGLT2 han demostrado de forma consistente su impacto en la insuficiencia cardiaca y en la enfermedad renal crónica. En el estudio EMPA-REG OUTCOME, la empagliflozina redujo la mortalidad por causa cardiovascular en pacientes con diabetes tipo 2 de alto riesgo133. Su utilidad en la MASLD se potencia cuando coexisten albuminuria, tasa de filtrado glomerular reducida o insuficiencia cardiaca134. La combinación de un inhibidor de SGLT2 y un agonista de GLP-1 RA ofrece complementariedad metabólica y hemodinámica, sumando para el control del peso, la glucemia y la rigidez arterial.
PIOGLITAZONA: EFICACIA HISTOLÓGICA, USO SELECTIVO
La pioglitazona mantiene un lugar en el tratamiento de los pacientes con NASH y diabetes tipo 2. En un ensayo a largo plazo mejoró la necroinflamación y la fibrosis, aunque con efectos adversos de ganancia ponderal y edema135. Por ello, su uso se recomienda solo en perfiles seleccionados, cuando la resistencia a la insulina sea prominente y el balance beneficio-riesgo resulte favorable.
RESMETIROM: EL PRIMER ANTIFIBRÓTICO APROBADO
En 2024, la FDA aprobó el resmetirom como primer antifibrótico para la MASH con fibrosis F2-F3, por demostrar mejoría de la fibrosis y resolución de la MASH, además de reducir el C-LDL, la apoB y los triglicéridos136.
Secuenciación clínica y adherencia
En la fibrosis ≥ F2 o con RCV muy alto, la secuencia debe comenzar con estatinas de alta intensidad, añadir ezetimiba y un inhibidor de PCSK9 si es necesario, introducir un agonista de GLP-1 (semaglutida, liraglutida), considerar un inhibidor de SGLT2 en presencia de insuficiencia cardiaca, albuminuria o tasa de filtrado glomerular reducida, añadir resmetirom en la MASH con fibrosis F2-F3 y reservar la pioglitazona para pacientes con NASH y diabetes tipo 2.
A ello se suma un aspecto frecuentemente olvidado: la adherencia terapéutica. Los estudios en hipertensión y prevención secundaria muestran que hasta un 40% de los pacientes abandonan los tratamientos preventivos de forma crónica, lo que se asocia a un aumento de eventos y de mortalidad137. La entrevista motivacional, la simplificación de los esquemas posológicos y el uso de recordatorios digitales son herramientas que deben integrarse en el seguimiento clínico. En definitiva, la farmacoterapia en la MASLD debe dejar atrás la visión hepatocéntrica y asumirla como una estrategia integrada cardio-RENO-hepato-metabólica.
Seguimiento longitudinal del riesgo cardiovascular en pacientes con MASLD: marco práctico e integrado
El RCV en los pacientes con MASLD no es una fotografía estática, sino un proceso dinámico que debe abordarse en el marco de un continuo cardio-hepato-renal-metabólico. La fibrosis ≥ F2 debe considerarse un umbral de RCV avanzado20,46,138.
EVALUACIÓN BASAL: TRAZAR EL MAPA DE RIESGO
El primer acto clínico debe ser exhaustivo e integrar una historia cardiometabólica completa (antecedentes, hábitos de vida, consumo de tabaco y alcohol, dieta, actividad física y sueño), una exploración dirigida (IMC, perímetro de la cintura, presión arterial protocolizada) y pruebas de laboratorio con perfil lipídico, incluyendo apoB, HbA1c, creatinina con estimación del filtrado glomerular y cociente albúmina/creatinina. La determinación de la lipoproteína (a) al menos una vez en la vida añade valor pronóstico. De forma paralela, la fibrosis debe estratificarse mediante el FIB-4, y cuando el resultado sea intermedio o elevado, o exista discordancia con el fenotipo clínico, complementarse con elastografía para evaluar la rigidez hepática. Este núcleo debe completarse con una métrica de salud cardiovascular global, como el Life’s Essential 8 (LE8), que evalúa la dieta, la actividad física, el tabaquismo, el sueño, el IMC, el colesterol no HDL, la glucemia y la presión arterial. Un LE8 alto se asocia a menor incidencia de MASLD y mejor pronóstico139,140. La albuminuria merece especial atención, pues constituye un marcador de daño de órgano diana y de RCV aumentado, condiciona tanto los objetivos tensionales como la selección de fármacos (inhibidores de la enzima convertidora de angiotensina [IECA], antagonistas de los receptores de la angiotensina II [ARA-II], inhibidores de SGLT2, finerenona en nefropatía DM), y su persistencia debe confirmarse en al menos dos de tres determinaciones37.
SEGUIMIENTO DINÁMICO Y ESTRATIFICADO
El ritmo de reevaluación debe adaptarse al riesgo. En los pacientes sin fibrosis ni comorbilidad mayor, es suficiente una revisión anual con presión arterial, perímetro de cintura, LE8, lípidos/apoB, HbA1c, cociente albúmina/creatinina, transaminasas y FIB-4. En los pacientes con diabetes, hipertensión o dislipidemia, el intervalo se acorta a 6-12 meses. En aquellos con fibrosis ≥ F2 o ECV establecida, se recomienda un control estrecho cada 3-6 meses durante el primer año de intervención intensiva, con repetición del FIB-4 a los 6-12 meses y elastografía anual (o antes en caso de progresión clínica o bioquímica). La revisión a corto plazo (3-6 meses tras la primera visita) debe centrarse en verificar la adherencia a la dieta, el ejercicio y la medicación, identificar las posibles barreras y ajustar el plan. En este periodo bastan los parámetros básicos en los pacientes de bajo riesgo, mientras que en aquellos con fibrosis significativa conviene añadir el perfil lipídico y las transaminasas.
IMAGEN VASCULAR Y RECLASIFICACIÓN
En escenarios de riesgo intermedio o en caso de discordancia entre las puntuaciones de riesgo tradicionales y el fenotipo clínico, la imagen vascular resulta determinante. La puntuación del CAC es la prueba más validada: unos valores ≥ 100 unidades Agatson obligan a intensificar la prevención cardiovascular. En la MASLD, la prevalencia de CAC ≥ 300 es elevada, y un FIB-4 intermedio o alto predice progresión acelerada del CAC39,77. Si la determinación del CAC no está disponible, la medición del grosor íntima-media carotídeo o la detección de placas carotídeas añade valor, y en la MASLD con biopsia la fibrosis se asocia a un grosor íntima-media elevado y una mayor carga de placas89. La velocidad de la onda de pulso ofrece una fenotipificación adicional de la rigidez arterial con valor pronóstico90.
INTERVENCIÓN Y AJUSTES SEGÚN LOS RESULTADOS
El seguimiento no debe limitarse a monitorizar, sino que exige una optimización intensiva de los factores de riesgo:
- −Lípidos: estatinas de alta intensidad como primera línea, con objetivos < 40 en riesgo extremo, < 55 mg/dl de C-LDL en muy alto riesgo y < 70 mg/dl en alto riesgo, y apoB < 65 mg/dl como diana complementaria139. Si no se alcanzan, añadir ezetimiba, bempedoico y considerar un inhibidor de PCSK9 o inclisirán.
- −Presión arterial: objetivo < 130/80 mmHg si se tolera; iniciar IECA/ARA-II en presencia de albuminuria, añadir Antagonista del calcio y/o diurético tiazídico o similar, y espinolactona si persiste fuera de objetivos140.
- −Glucemia y peso/adiposidad: la semaglutida reduce los eventos cardiovasculares en pacientes con obesidad sin diabetes126 y con diabetes con/sin obesidad, mejora la histología hepática125; los inhibidores de SGLT2 reducen las hospitalizaciones por insuficiencia cardiaca, los eventos renales y la mortalidad de causa cardiovascular133; el resmetirom ha demostrado beneficio histológico y un perfil lipídico cardioprotector136.
- −Fibrosis ≥ F2 confirmada: seguimiento más estrecho, considerar resmetirom y priorizar agonistas de GLP-1 o inhibidores de SGLT2 según el fenotipo metabólico.
- −Ateroesclerosis subclínica significativa (CAC ≥ 100 o grosor íntima-media carotídeo elevado o placa carot´dea o índice tobillo-brazo): aplicar estrategias de prevención intensiva como en pacientes de muy alto riesgo, incluso sin eventos.
ADHERENCIA Y METAS A LARGO PLAZO
El éxito del seguimiento exige estructurar objetivos SMART (Specific, Measurable, Achievable, Relevant, Time-bound): pérdida ponderal del 7-10% en 6-12 meses, ≥ 150-300 min/semana de ejercicio aeróbico moderado o 75-150 min de ejercicio vigoroso más 2-3 sesiones de fuerza, 7-8 h de sueño regular, abandono del tabaco y logro de metas lipídicas, tensionales y glucémicas personalizadas. El LE8 debe recalcularse cada 6-12 meses para dirigir la intervención hacia los dominios peor puntuados. La adherencia terapéutica es crítica: cerca del 50% de los pacientes abandona los tratamientos preventivos crónicos al cabo de 1 año, con aumento de la mortalidad total y de causa cardiovascular137. En la MASLD, en la que la prevención es multimodal y prolongada, este fenómeno resulta especialmente dañino. El seguimiento debe incorporar evaluación de la adherencia, herramientas digitales (recordatorios, telemonitorización, telecoaching), entrevista motivacional y cribado de determinantes sociales (inseguridad alimentaria, entornos obesogénicos), con derivación a recursos comunitarios cuando sea posible. Finalmente, el análisis de desenlaces debe contemplar tanto los eventos cardiovasculares como la progresión hepática y la mortalidad de causa no cardiovascular. Para minimizar los sesgos, en contextos de riesgos competitivos deben emplearse modelos de subdistribución de Fine-Gray81.
En síntesis, el seguimiento longitudinal en la MASLD exige un modelo de atención que combine estratificación inicial precisa, reevaluación periódica ajustada al riesgo, integración de biomarcadores hepáticos, cardiovasculares y renales, realización de imagen vascular cuando sea pertinente, intensificación terapéutica basada en el fenotipo y estrategias robustas de adherencia. El hepatólogo debe asumir que cuidar el hígado en la MASLD es inseparable de prevenir la aterotrombosis, proteger el riñón y preservar el corazón.
Conclusiones (Tabla 7)
Tabla 7. Decálogo de consejos prácticos en la consulta del paciente con MASLD
| N.º | Consejo práctico (qué hacer en la consulta) | Referencias |
|---|---|---|
| 1 | Peso: fijar objetivo de pérdida ≥ 7-10% en 6-12 meses; diseñar plan de mantenimiento y seguimiento periódico; evitar metas poco realistas que desmotiven | 92,93 |
| 2 | Dieta: priorizar dieta mediterránea (incluyendo variantes como green-Med); alternativas DASH o plant-based; reducir azúcares libres, fructosa y ultraprocesados; adaptar al contexto del paciente | 94,97,99,103 |
| 3 | Ejercicio: prescribir ≥ 150 min/sem moderado o ≥ 75 min/sem vigoroso; combinar aeróbico + fuerza; considerar ejercicio de alta intensidad por intervalos en pacientes motivados; romper sedentarismo con pausas activas | 109,111,113 |
| 4 | Sueño y apnea obstructiva del sueño: cribar apnea con STOP-Bang en pacientes de riesgo (ronquidos, hipertensión arterial resistente, somnolencia); derivar a estudio y tratamiento | 114,115 |
| 5 | Alcohol y café: reforzar abstinencia absoluta de alcohol; recomendar consumo de café (2-3 tazas/día) salvo contraindicaciones, por su asociación con menor riesgo de fibrosis | 106,107,108 |
| 6 | Conductual y organizativo: acompañar todas las recomendaciones con fijación de objetivos, autorregistro, retroalimentación periódica y soporte digital; derivar a programas multidisciplinarios si fracaso en 3-6 meses | 20 |
| 7 | Tabaco: indagar en cada consulta; dar consejo breve; derivar a programas especializados de cesación, dada su asociación con progresión de fibrosis y riesgo cardiovascular | 116,117 |
| 8 | Exposoma ambiental: sensibilizar sobre contaminación (PM2.5, PM10, NO2); recomendar reducir exposición (p. ej., evitar ejercicio en picos de polución) | 118,119 |
| 9 | Motivación: utilizar entrevista motivacional; centrar la comunicación en logros alcanzables; evitar mensajes contraproducentes sobre pérdidas rápidas de peso | 113 |
| 10 | Personalización y red asistencial: adaptar el plan a la edad, la comorbilidad, la situación social y las preferencias; fomentar un abordaje multidisciplinario (nutrición, psicología, rehabilitación, riesgo cardiovascular) | 20 |
Este decálogo sintetiza las medidas prácticas basadas en la evidencia para la consulta hepatológica en pacientes con MASLD. Integra intervenciones sobre estilo de vida con énfasis en la personalización y el trabajo multidisciplinario, orientado a mejorar la adherencia y el pronóstico cardiovascular y hepático.
La MASLD constituye una de las enfermedades crónicas de mayor prevalencia, pues afecta a más de una cuarta parte de la población adulta mundial, con tendencia creciente y especial impacto en individuos en edad laboral141. Su carácter no es exclusivamente hepático; se trata de una condición sistémica, estrechamente vinculada al riesgo vascular, hasta el punto de que la ECV constituye la principal causa de mortalidad en estos pacientes142. La fibrosis avanzada debe asumirse como el principal marcador pronóstico, integrando prevención hepática y cardiovascular143. Este conocimiento obliga a superar la dicotomía entre hepatología y cardiología, entendiendo el riesgo en un continuo cardio-hepato-renal-metabólico. En la práctica, esto implica dos acciones simultáneas: cribar la MASLD en los pacientes con ECV, y viceversa, cribar la ECV en todos los pacientes con MASLD, independientemente de que presenten o no factores de riesgo clásicos144. La valoración del riesgo vascular debe apoyarse en escalas validadas, pruebas no invasivas de fibrosis (FIB-4, elastografía) y, cuando exista riesgo intermedio o discordancia, implementación de técnicas complementarias para reclasificar el riesgo CV145.
En términos de tratamiento, la MASLD presenta dos vertientes críticas: la hepática y la cardiovascular. La modificación intensiva del estilo de vida sigue siendo la piedra angular: pérdida de peso, patrón dietético cardiosaludable (dieta mediterránea como referencia), ejercicio aeróbico y de fuerza, higiene del sueño y abandono del tabaco146 y del alcohol. En paralelo, el desarrollo de fármacos con eficacia dual (GLP-1, SGLT2, resmetirom) abre una nueva etapa de intervención cardio-hepática cardio-RENO-hepática-metabólica147. El abordaje óptimo requiere equipos multidisciplinarios, que integren hepatólogos, cardiólogos, endocrinólogos, internistas, nefrólogos y profesionales de atención primaria, garantizando los circuitos de cribado, prevención e intervención coordinada148. Esta visión ha quedado reflejada en las guías europeas multidisciplinarias, que recalcan la necesidad de una integración plena en los sistemas de salud149.
En conclusión, la MASLD es una enfermedad prevalente, multisistémica y de alta carga sanitaria, cuyo impacto trasciende el hígado. Incrementa de forma significativa la mortalidad, especialmente por causa cardiovascular, y exige una valoración rigurosa y periódica del riesgo vascular, así como un cribado bidireccional entre hepatología y cardiología. El tratamiento debe combinar cambios de estilo de vida y terapias con beneficio dual, bajo el liderazgo de equipos multidisciplinarios capaces de abordar el continuo cardio-RENO-hepática-metabólica. Solo así será posible reducir la carga clínica y social de la MASLD, y mejorar el pronóstico global de estos pacientes150.
Financiamiento
Este proyecto ha recibido financiamiento del European Horizon’s Research and Innovation Programme HORIZON-HLTH-2022-STAYHLTH-02 (agreement No 101095679) y del Fondo de Investigaciones Sanitarias, Instituto de Salud Carlos III, España (PI22/01853).
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. El estudio no involucra datos personales de pacientes ni requiere aprobación ética. No se aplican las guías SAGER.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que utilizaron inteligencia artificial para la redacción de este manuscrito, en concreto ChatGPT5 Thinking para la edición final del capítulo y la configuración de las tablas.
