Introducción
En 2023 se redefinió la enfermedad hepática grasa no alcohólica (NAFLD, Non-Alcoholic Fatty Liver Disease) como esteatosis hepática metabólica (MASLD, Metabolic dysfunction Associated Steatotic Liver Disease), y así mismo la esteatohepatitis no alcohólica (NASH, Non-Alcoholic Steatohepatitis) fue redefinida como esteatohepatitis de origen metabólico (MASH, Metabolic dysfunction Associated Steato Hepatitis). Dentro de esta nueva clasificación se propuso una nueva categoría, actualmente denominada MetALD (Metabolic dysfunction and Alcohol-related Liver Disease), en la que convergen pacientes que cumplen criterios para MASLD y que además tienen consumo riesgoso de alcohol1, considerado este como 140-350 g/semana (20-50 g/día) en las mujeres y 210-420 g/semana (30-60 g/día) en los hombres2. La propuesta, de acuerdo con esta nueva nomenclatura, para establecer los criterios de MetALD se muestra en la figura 1.
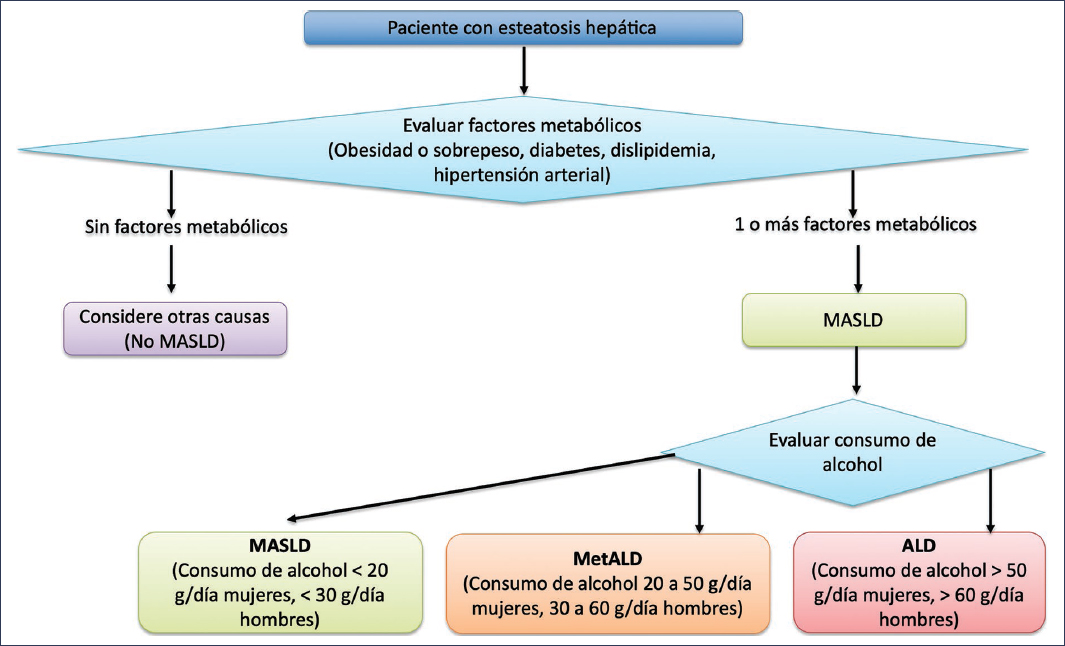
Figura 1. Criterios para considerar MetALD dentro de la nueva nomenclatura de esteatosis hepática.
Controversias de la nueva nomenclatura y definición de MetALD
Existe ambigüedad en los umbrales de consumo alcohólico, ya que los límites propuestos en la actualidad para definir un consumo de riesgo de alcohol carecen de solidez científica, han sido mayormente definidos sobre una base empírica y son variables entre distintas publicaciones3. Por otro lado, el término MetALD representa una superposición conceptualmente imprecisa entre MASLD y enfermedad hepática relacionada con el alcohol (ALD, Alcohol-associated Liver Disease). La distinción diagnóstica entre predominio metabólico o alcohólico no siempre es clara y puede depender en exceso del juicio clínico subjetivo4. Además, aunque se reconoce que el consumo de alcohol potencia la progresión de la fibrosis, la cirrosis y el carcinoma hepatocelular, aún faltan estudios prospectivos robustos que permitan diferenciar de forma clara los riesgos del individuo con MetALD respecto a la MASLD o la ALD por sí mismas5.
En el campo de la investigación, otro gran reto es que esta nueva clasificación implica reevaluar bases de datos históricas y ensayos clínicos en curso, lo cual puede dificultar la realización de comparaciones longitudinales y cuestionar la validez de resultados previos6.
Epidemiología de la MetALD
Existe un subregistro importante en cuanto al consumo de alcohol, toda vez que generalmente, para evaluarlo, se aplican cuestionarios autoinformados, que subestiman la ingesta real en un 20-40%, lo que puede infravalorar la verdadera carga de MetALD7.
La prevalencia de la MetALD es más alta en poblaciones hispanas y del Este de Europa, mientras que es menor en Asia, pero con una tendencia creciente en jóvenes en centros urbanos8.
Los estudios en población general llevados a cabo en los Estados Unidos de América y en Europa sugieren que la MetALD afecta aproximadamente al 3-5% de la población adulta9,10. En Asia, las cifras se reportan entre el 1% y el 3%, probablemente en relación con diferencias culturales en el consumo de alcohol11. En América Latina, donde coexisten una alta prevalencia de obesidad y un consumo elevado de alcohol, las prevalencias oscilan entre el 8 y el 10%12. Sin embargo, la prevalencia de la MetALD se incrementa cuando se evalúa en pacientes con un diagnóstico ya preestablecido de MASLD, en los que se ha reportado que entre el 15% y el 30% cumplen criterios de MetALD13.
El riesgo de padecer MetALD es particularmente elevado en varones de mediana edad con obesidad visceral y diabetes mellitus tipo 214. Se sabe también que los pacientes con MetALD tienen mayor riesgo de fibrosis avanzada comparados con quienes solo cumplen criterios de MASLD15. Finalmente, los estudios han demostrado que el riesgo de carcinoma hepatocelular es sustancialmente más alto (tasa de incidencia de 1.847 por 1000 personas-año) en pacientes con MetALD e índice de fibrosis-4 (FIB-4) ≥ 1.3, en comparación con otras etiologías o con solo MASLD16.
Patogénesis de la ALD y la MASLD: diferencias y similitudes
Aunque la ALD y la MASLD difieren en sus factores desencadenantes primarios (consumo excesivo de alcohol en la ALD y resistencia a la insulina/obesidad en la MASLD), comparten múltiples vías fisiopatológicas comunes que explican por qué existe un espectro clínico superpuesto e incluso la condición mixta MetALD4. En la MetALD convergen, por un lado, el consumo crónico y excesivo de etanol, que causa toxicidad directa en los hepatocitos, genera alteraciones del metabolismo lipídico y promueve la inflamación17, y por otro, la resistencia a la insulina, la obesidad visceral y el síndrome metabólico, lo cual induce un estado de lipotoxicidad hepática18 (Tabla 1).
Tabla 1. Comparación de la patogénesis de la ALD y la MASLD
| Mecanismo | ALD | MASLD | Puntos clave de convergencia |
|---|---|---|---|
| Factor desencadenante primario | Consumo crónico y excesivo de alcohol | Resistencia a la insulina, obesidad visceral, síndrome metabólico | Ambas requieren un estímulo externo sostenido que altera la homeostasis hepática |
| Metabolismo lipídico | Acetaldehído y exceso de NADH inhiben β-oxidación y promueven lipogénesis | Hiperinsulinemia estimula SREBP-1c y ChREBP → aumenta la síntesis de ácidos grasos | Acumulación de triglicéridos (esteatosis hepática) |
| Estrés oxidativo | Metabolismo de etanol vía CYP2E1 → ROS y aductos de acetaldehído | Lipotoxicidad por ácidos grasos libres → peroxidación lipídica | Estrés oxidativo y daño mitocondrial como ejes centrales |
| Inflamación e inmunidad innata | Disbiosis intestinal, aumento de permeabilidad → LPS activa TLR4 en células de Kupffer → TNF-α, IL-1β | Tejido adiposo disfuncional libera TNF-α, IL-6; descenso de adiponectina | Activación de células de Kupffer y respuesta inflamatoria crónica |
| Fibrogénesis | Acetaldehído y ROS activan células estrelladas hepáticas | Señales metabólicas crónicas (lipotoxicidad, resistencia a la insulina) activan células estrelladas | Fibrosis progresiva mediada por depósito de matriz extracelular |
| Carcinogénesis | Mutagénesis directa por acetaldehído, ROS y alteraciones epigenéticas | Inflamación crónica, obesidad, hiperinsulinemia → activación de vías IGF/PI3K-AKT | CHC puede aparecer incluso en ausencia de cirrosis |
| Espectro clínico | Esteatosis → hepatitis relacionada con el alcohol → fibrosis → cirrosis → CHC | Esteatosis → MASH → fibrosis → cirrosis → CHC | Curso progresivo en espectro similar |
CHC: carcinoma hepatocelular; ChREBP: Carbohydrate Response Element-Binding Protein; CYP2E1: citocromo P2E1; IGF/PI3K-AKT: factor de crecimiento similar a la insulina/fosfoinositida 3-cinasa – proteína cinasa B; IL-1β: interleucina 1 beta; IL-6: interleucina 6; LPS: lipopolisacárido; MASH: Metabolic dysfunction Associated Steato Hepatitis; NADH: dinucleótido de nicotinamida y adenina reducido; ROS: especies reactivas de oxígeno; SREBP-1c: Sterol Regulatory Element-Binding Protein 1c; TNF- α: factor de necrosis tumoral alfa; TLR4: Toll-Like Receptor 4.
Alteraciones en el metabolismo lipídico
Tanto en la ALD como en la MASLD ocurre una acumulación intrahepática de triglicéridos (esteatosis) y hay un incremento en la lipogénesis de novo y una alteración en la β-oxidación mitocondrial. Sin embargo, en la ALD, la oxidación del etanol genera un exceso de dinucleótido de nicotinamida y adenina reducido (NADH), que a su vez favorece la lipogénesis y bloquea la oxidación de ácidos grasos, mientras que en la MASLD la hiperinsulinemia estimula factores de transcripción que son clave para regular la lipogénesis; dentro de los más relevantes se encuentran la Sterol Regulatory Element-Binding Protein 1c (SREBP-1c) y la Carbohydrate Response Element-Binding Protein (ChREBP), induciendo mayor síntesis de ácidos grasos17–20.
Estrés oxidativo y daño mitocondrial
En la ALD, el metabolismo del etanol por vía del citocromo P2E1 (CYP2E1) produce especies reactivas de oxígeno (ROS) y acetaldehído, que dañan a las proteínas y al ácido desoxirribonucleico17. En la MASLD, el exceso de ácidos grasos libres induce lipotoxicidad, disfunción mitocondrial y peroxidación lipídica20,21. Así, en la MetALD el estrés oxidativo y el daño mitocondrial son mecanismos que detonan inflamación y progresión a fibrosis17,20–22.
Inflamación y sistema inmunitario innato
El etanol incrementa la permeabilidad intestinal, favoreciendo la translocación bacteriana y la activación del toll-like receptor 4 (TLR4) por el lipopolisacárido (LPS), lo que es capaz de detonar una respuesta inflamatoria (factor de necrosis tumoral alfa [TNF-α], interleucina 1b [IL-1β] e interleucina 6 [IL-6])17,19,22. Por su parte, en la MASLD la resistencia a la insulina y la lipoperoxidación favorecen un perfil proinflamatorio (TNF-α, IL-6, leptina) y la reducción de adiponectina20,21. En ambas afecciones existe activación de células de Kupffer y reclutamiento de células inmunitarias, lo que amplifica la inflamación hepática19–22.
Fibrogénesis
Tanto en la ALD como en la MASLD, la inflamación crónica activa a las células estrelladas hepáticas, promoviendo el depósito de matriz extracelular y favoreciendo la progresión de la fibrosis17,19,21–23. En la ALD, el acetaldehído y las ROS actúan directamente sobre las células estrelladas22,23, mientras que en la MASLD la fibrosis se relaciona más con señales metabólicas crónicas (resistencia a la insulina, lipotoxicidad)21.
Carcinogénesis
En la ALD existe mutagénesis directa por acetaldehído y estrés oxidativo, además de efectos epigenéticos inducidos por el alcohol17,19,21. En la MASLD, la carcinogénesis está asociada a la obesidad, la diabetes y la inflamación crónica, incluso en ausencia de cirrosis. En ambas enfermedades, la inflamación, la disfunción mitocondrial y la señalización alterada de la insulina o del factor de crecimiento similar a la insulina contribuyen al desarrollo de carcinoma hepatocelular16,17,21,22.
Evaluación de la MetALD
El diagnóstico de MetALD requiere la integración de cuatro aspectos fundamentales: 1) evidencia de esteatosis hepática, 2) cumplir criterios de MASLD, 3) demostrar un consumo riesgoso de alcohol y 4) estratificar el riesgo de fibrosis1,3,4 (Fig. 2).
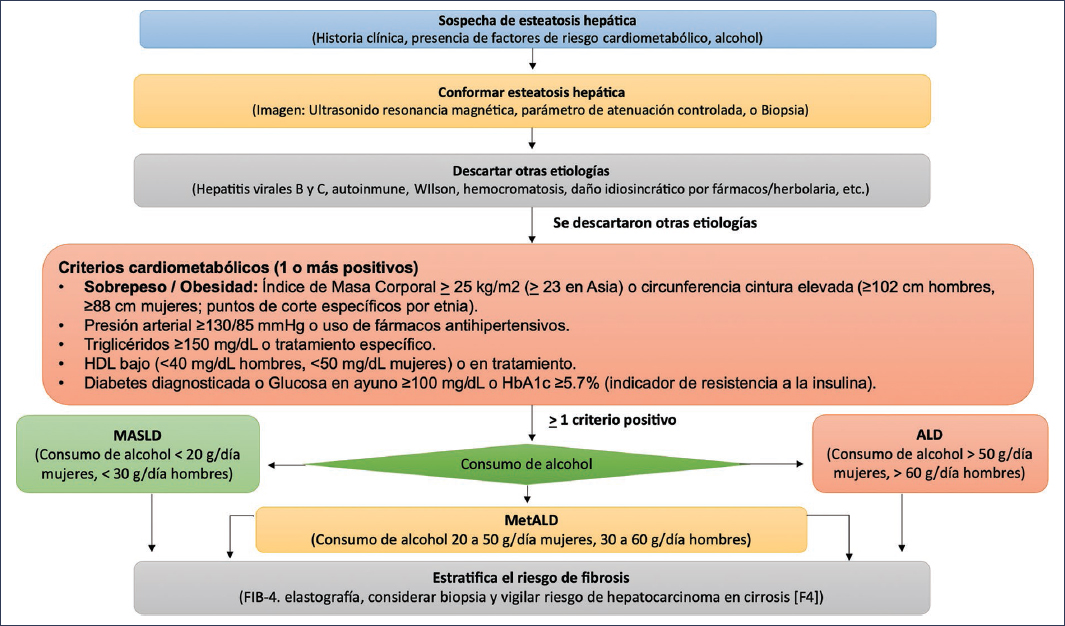
Figura 2. Algoritmo diagnóstico de la MetALD.
Estrategias terapéuticas
El tratamiento de la MetALD se basa en la abstinencia de alcohol, el control estricto de los factores metabólicos y la vigilancia de las complicaciones, complementado con terapias en investigación. No existe aún un fármaco específico aprobado, pero la combinación de estrategias conductuales, tratamientos farmacológicos para la comorbilidad y vigilancia hepática constituye la base terapéutica actual4 (Tabla 2).
Tabla 2. Estrategias terapéuticas en la MetALD1–4
| Estrategia | Intervención específica | Evidencia (clave) | Efecto hepático esperado | Nivel de recomendación |
Consideraciones de seguridad |
|---|---|---|---|---|---|
| Alcohol | Abstinencia total o reducción intensiva; consejería estructurada; manejo de trastorno por uso de alcohol | Metaanálisis y cohortes: descienden la descompensación y la mortalidad | Descienden la inflamación, la progresión de la fibrosis y el riesgo de CHC | A | Evaluar síndrome de abstinencia; derivar a adicciones; pruebas objetivas (PEth/EtG) cuando sea posible |
| Fármacos para alcohol | Naltrexona, acamprosato, baclofeno (cirrosis) | ECA y series: aumenta la abstinencia; baclofeno útil en hepatopatía | Descienden las recaídas → beneficio indirecto hepático | B | Naltrexona: evitar en hepatitis aguda; baclofeno: sedación; acamprosato: ajustar en IR |
| Pérdida de peso | Dieta hipocalórica 500-1000 kcal/d; objetivo 7-10% | ECA y estudios observacionales en MASLD: mejora MASH y fibrosis | Descienden esteatosis, NASH/MASH y posiblemente la fibrosis | A | Individualizar si sarcopenia; evitar pérdidas rápidas en cirrosis descompensada |
| Ejercicio | Aeróbico + resistencia ≥ 150 min/sem | ECA: desciende grasa hepática independientemente del peso | Desciende esteatosis y aumenta sensibilidad a la insulina | A | Adaptar en cirrosis; prevenir sarcopenia |
| Patrón dietético | Dieta mediterránea; menos fructosa y grasas trans/saturadas | ECA y estudios de cohortes: descienden esteatosis e IR | Descienden lipotoxicidad e inflamación | B | Adherencia sostenida; apoyo de nutrición clínica |
| DM2: agonistas GLP-1R | Semaglutida/liraglutida | ECA: resolución de MASH; descenso de peso | Desciende esteatohepatitis; posible descenso de fibrosis (en estudio) | A/B | GI, colelitiasis; vigilar en pancreatitis previa |
| DM2: inhibidores SGLT2 | Empagliflozina/dapagliflozina | ECA: desciende grasa hepática por imagen | Descienden esteatosis e inflamación | B | ITU micóticas; euglucémica cetoacidosis (rara) |
| DM2: metformina | Primera línea metabólica | Estudios de cohortes: beneficio CV; sin efecto claro en NASH | Beneficio metabólico sistémico | C | GI; evitar en IR avanzada con riesgo de acidosis |
| Dislipidemia | Estatinas | Ensayos y estudios de cohortes: seguras en hepatopatía compensada; descienden eventos CV; señal de descenso de CHC | Beneficio CV; posible descenso de CHC | A | Vigilar transaminasas; seguras en cirrosis compensada |
| Hipertensión arterial | Control intensivo individualizado | Estudios de cohortes: descienden eventos CV | Indirecto sobre pronóstico | B | IECA/ARA-II con cautela en ascitis avanzada |
| Procedimientos | Cirugía bariátrica (seleccionados) | Estudios de cohortes y ECA: resolución MASH y descenso de fibrosis | Descienden esteatohepatitis y fibrosis | B | Selección rigurosa; riesgo perioperatorio en cirrosis |
| Agentes en investigación | PPAR panagonista (lanifibranor), FXR (cilofexor/obetichólico), ACC/FASN inhibidores | Estudios de fase II–III: mejoría histológica y enzimática | Descienden actividad inflamatoria y lipogénesis; efecto antifibrótico potencial | B (en investigación) | Acceso en ensayos; EA prurito (FXR), perfil lipídico (ACC) |
| Vigilancia y complicaciones | Elastografía/FIB-4; US/AFP cada 6 meses en fibrosis avanzada | Guías | Desciende mortalidad por diagnóstico precoz de CHC | A | Asegurar adherencia; ruta de derivación a TPH |
| Trasplante hepático | Cirrosis descompensada o CHC no curable | Estándar | Supervivencia a largo plazo | A | Criterios de selección; soporte adicciones |
|
|
|||||
* Nivel de recomendación orientativo (A: fuerte/alta calidad; B: calidad moderada; C: calidad limitada/consenso).
ACC: acetil coenzima A carboxilasa; AFP: alfafetoproteína; ARA-II: antagonistas de los receptores de angiotensina II; CHC: carcinoma hepatocelular; CV: cardiovascular; DM2: diabetes mellitus tipo 2; EA: eventos adversos; ECA: ensayos clínicos aleatorizados; FASN: sintasa de ácidos grasos; FIB-4: índice de fibrosis 4; FXR: receptor farnesoide X; GI: gastrointestinales; GLP-1R: receptor del péptido similar al glucagón tipo 1; IECA: inhibidores de la enzima convertidora de angiotensina; IR: insuficiencia renal; ITU: infecciones del tracto urinario; PEth/EtG: fosfatidiletanol / etilglucurónido; PPAR: receptor activado por proliferadores de peroxisomas; SGLT2: cotransportador de sodio y glucosa tipo 2; TPH: programa de trasplante hepático; US: ultrasonido.
Conclusiones
- – La introducción del concepto de MetALD es conceptualmente valiosa, pero enfrenta retos significativos en su aplicación clínica y epidemiológica.
- – Se requieren estudios prospectivos que validen su utilidad pronóstica y definan con evidencia los umbrales clínicamente relevantes.
- – Es importante evitar estigmatizar a los pacientes; el enfoque ideal debería integrar múltiples factores de riesgo y enfatizar intervenciones centradas en el paciente.
- – Hasta que no se disponga de más evidencia, sería prudente considerar el alcohol como modulador de un riesgo continuo dentro de la MASLD, en lugar de delimitar categorías rígidas.
- – La MetALD afecta ya a millones de individuos en todo el mundo, con prevalencias del 3-10% en población general y de hasta el 30% en pacientes con riesgo metabólico.
- – Los datos actuales provienen de estudios retrospectivos y autoinformes, lo que limita la precisión de las estimaciones.
- – Existe una urgente necesidad de definiciones estandarizadas para estimar la carga global y de biomarcadores objetivos de consumo alcohólico y susceptibilidad metabólica, y se requieren estudios prospectivos multinacionales que determinen la verdadera carga de fibrosis avanzada y hepatocarcinoma atribuible a la MetALD.
- – La MetALD debe entenderse como una enfermedad emergente con un impacto epidemiológico significativo, cuyo reconocimiento temprano permitirá diseñar estrategias preventivas más efectivas.
- – La ALD y la MASLD comparten mecanismos patogénicos clave (esteatosis, estrés oxidativo, inflamación, fibrogénesis), pero difieren en el estímulo inicial (alcohol o disfunción metabólica) y en algunos mediadores predominantes (acetaldehído y disbiosis en la ALD, y resistencia a la insulina y adipocinas en la MASLD). Esta convergencia fisiopatológica explica la emergencia del concepto de MetALD, que reconoce la interacción sinérgica entre el alcohol y la disfunción metabólica en el desarrollo y la progresión del daño hepático.
- – La terapia actual de la MetALD se basa en estrategias enfocadas a mantener la abstinencia de alcohol y enfatizar el control metabólico.
Financiamiento
Los autores declaran no haber recibido financiamiento para este estudio.
Conflicto de intereses
F. Higuera-de la Tijera es oradora para Sanfer, Grünenthal, Gilead, Abbott, Medix y Adium. A. Servín-Higuera no tiene conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Las autoras declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. El estudio no involucra datos personales de pacientes ni requiere aprobación ética. No se aplican las guías SAGER.
Declaración sobre el uso de inteligencia artificial. Las autoras declaran que utilizaron inteligencia artificial para la redacción de este manuscrito, en concreto ChatGPT y Gemini para crear los algoritmos, las figuras y las tablas de este artículo.
