Introducción
La esteatosis hepática metabólica (MASLD, Metabolic Dysfunction-Associated Steatotic Liver Disease) se define como la presencia de esteatosis hepática en conjunto con al menos un factor de riesgo cardiometabólico1 (Fig. 1).
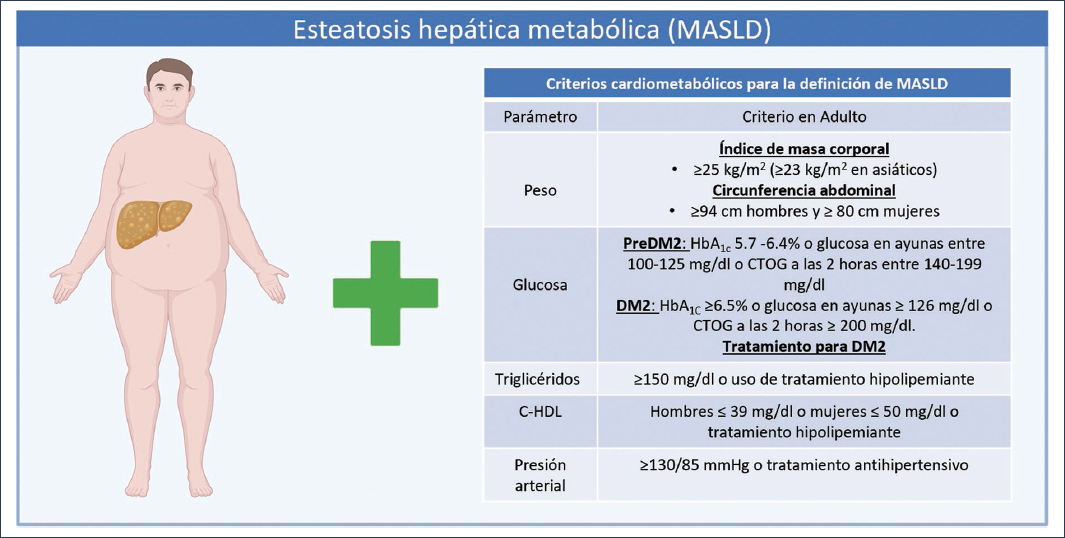
Figura 1. La MASLD es la presencia de esteatosis hepática junto con al menos uno de los cinco factores de riesgo cardiometabólico: peso elevado, glucosa elevada, trigliceridemia, bajo colesterol de alta densidad (C-HDL) e hipertensión arterial. CTOG: curva de tolerancia oral a la glucosa; DM2: diabetes mellitus tipo 2; HbA1c: hemoglobina glucosilada.
La MASLD toma gran relevancia al posicionarse como la causa más común de enfermedad hepática crónica, afectando hasta al 38% de los adultos globalmente2 y hasta al 65% de los pacientes con diabetes mellitus tipo 2 (DM2)3.
México es uno de los países con más sobrepeso y obesidad en el mundo. En la encuesta nacional de salud y nutrición (ENSANUT) se encontró que, en la población adulta, el 76.2% tiene sobrepeso u obesidad y el 18.4% padece diabetes mellitus tipo 24. En México se ha estimado una prevalencia de MASLD del 49.7%5. Por lo tanto, es de gran relevancia esta nomenclatura para una enfermedad tan prevalente (Tabla 1).
Tabla 1. Puntos clave acerca de la nueva nomenclatura
| Se elimina el término NAFLD y se adopta el nuevo término MASLD. |
| Se eliminan los términos negativo y alcohol para hacer énfasis en la base metabólica de la enfermedad y no ser un diagnóstico de exclusión. |
| La palabra fatty se retira de la nomenclatura por considerarla estigmatizante. |
| Para establecer el diagnóstico se requiere evidencia de esteatosis más algún factor de riesgo metabólico. |
| Se introduce por primera vez el concepto de MetALD para referirse a los pacientes que tienen tanto factores de riesgo metabólico como consumo de alcohol significativo. |
| En los países hispanohablantes, para dar continuidad a la terminología, se adoptan los acrónimos en inglés: SLD, MASLD, MASL, MASH, MetALD y ALD. |
| La evidencia y las recomendaciones generadas bajo el término NAFLD aplican también a la MASLD. |
Evolución de la terminología: más de 40 años de historia
En 1980, Ludwig et al.6 describieron una serie de 20 biopsias hepáticas de pacientes en los que encontraron esteatosis de causa no identificada. Característicamente, la mayoría de los pacientes tenían obesidad y algunos diabetes, y a estos hallazgos, al no tener un consumo importante de alcohol, se les clasificó como esteatohepatitis no alcohólica6.
En 2009, la European Association for the Study of the Liver (EASL) definió a la enfermedad hepática grasa no alcohólica (NAFLD, Non-Alcoholic Fatty Liver Disease) como aquella condición caracterizada por una acumulación de grasa en el hígado con un consumo diario de alcohol ≤ 20 g en las mujeres y ≤ 30 g en los hombres y sin otras causas de hepatopatía crónica. Es de destacar que está definición no requería la presencia de ningún factor de riesgo cardiometabólico7.
De NAFLD a MAFLD
Tras 40 años sin cambios en la terminología, en 2020 se propuso modificar la nomenclatura para reemplazar NAFLD por enfermedad hepática grasa asociada a disfunción metabólica (MAFLD, Metabolic-Associated Fatty Liver Disease). El diagnóstico en ese entonces requería la presencia de esteatosis hepática (detectada por imagen, biomarcadores, puntajes o histología) como criterio de entrada y la presencia de al menos dos factores de riesgo metabólicos8. Sin embargo, se mantuvo la palabra fatty, que puede ser ofensiva y estigmatizante; no se incluyó la cantidad de alcohol, lo que no permitía determinar la contribución del consumo de alcohol a la esteatosis hepática; no categorizaba la enfermedad y se propuso por un grupo de expertos sin ser un consenso oficial ni respaldado por las principales sociedades globales9.
De NAFLD a MASLD
En 2023, un consenso liderado por la American Association for the Study of Liver Diseases (AASLD), la EASL y la Asociación Latinoamericana para el Estudio del Hígado (ALEH) propuso un cambio en la nomenclatura previamente establecida en la que plantearon el cambio de NAFLD por un nuevo término que mejorara algunas deficiencias del antiguo. Algunos de los aspectos que mejoraron la terminología previa fueron la naturaleza excluyente para realizar un diagnóstico, el poco reconocimiento de la causa principal del problema, la falta de integración de la fisiopatología en la terminología y el uso de una palabra estigmatizante u ofensiva.
Para llegar a esta nueva nomenclatura se realizó un proceso Delphi en el que participaron médicos de sociedades de hepatología, endocrinología y pediatría, organizaciones de defensa de los pacientes y autoridades regulatorias, entre otras. Colaboraron 56 países con un total de 224 participantes, y al final se llegó a la nueva definición y al nuevo término MASLD. Para alcanzar el consenso se requería una mayoría del 67% de los votos10–12. Tras casi 3 años de trabajo, con cuatro rondas virtuales y dos presenciales de metodología Delphi y discusiones activas muy interesantes, se establecieron la nueva terminología para la esteatosis hepática y los criterios diagnósticos para la MASLD (Fig. 2).
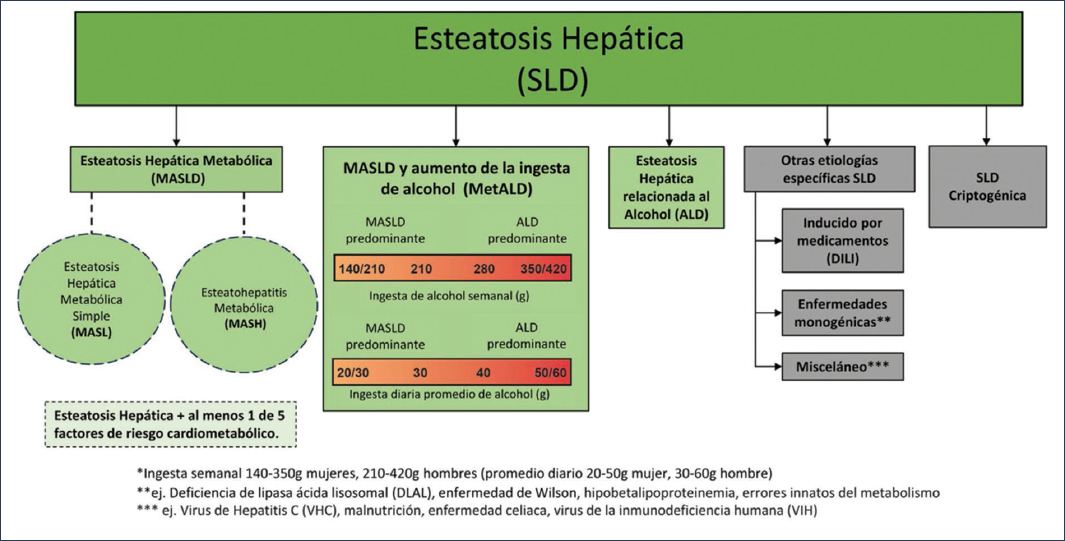
Figura 2. Nueva nomenclatura para la esteatosis hepática.
Los representantes de los países de habla hispana consensaron utilizar los mismos acrónimos independientemente del idioma para facilitar la estandarización de la nomenclatura13.
Más de 70 sociedades de todo el mundo aprobaron esta nueva nomenclatura, lo que ha generalizado su uso, facilita la investigación y es reproducible con los estudios previos de NAFLD14. En los últimos 2 años se han publicado más de 4400 artículos con el uso de esta nueva nomenclatura.
Beneficios de la nueva nomenclatura
Retirar la terminología negativa permite la coexistencia de dos enfermedades en un mismo paciente, incluido el consumo de alcohol, algo que vemos con frecuencia9. Además, es elemental mencionar que a menudo se utilizan términos «negativos» cuando se desconocen los aspectos fundamentales o las causas de una enfermedad, y se asume esta enfermedad en ausencia de otra. Sin embargo, la esteatosis hepática como componente del síndrome metabólico tiene una fisiopatología que, aunque compleja, está bien definida, por lo que un término negativo es incorrecto.
Agregar la palabra «metabólica» implica que la causa de la esteatosis hepática guarda relación con factores de riesgo metabólicos, por lo que se requieren para el diagnóstico. Anteriormente, al ser un diagnóstico de exclusión, se visualizaba como más relevante la exclusión de otra etiología y se minimizaba la contribución de los factores de riesgo metabólicos por los médicos y pacientes, que quedaron relegados a ser importantes solo en ausencia de otras causas de esteatosis, como el alcohol. Por ejemplo, en una encuesta a 250 médicos de primer contacto en los Estados Unidos de América se encontró que el 84% desestimaron la prevalencia de NAFLD en la población general y en la población obesa, el 91% reconocieron la NAFLD como parte del síndrome metabólico, y únicamente el 46% buscaban la enfermedad en la población obesa con diabetes15. Estas inconsistencias en el reconocimiento evidenciaron la necesidad de un cambio en la nomenclatura.
La nueva nomenclatura (Tabla 2)
Tabla 2. Nomenclatura antigua y nomenclatura actual
| Terminología antigua | Terminología actual |
|---|---|
| FLD | SLD |
| NAFLD/MAFLD | MASLD |
| NASL | MASL |
| NASH | MASH |
| Alcoholic Liver Disease (ALD) | Alcohol-related Liver Disease (ALD) |
| MetALD | |
| Otras etiologías específicas de SLD | |
| SLD criptogénica |
Esteatosis hepática (SLD, Steatotic Liver Disease) es el término general de la enfermedad, que incluye a todas las personas que tienen esteatosis sin importar la causa. Sustituye a enfermedad del hígado graso (FLD, Fatty Liver Disease)13. Se divide en cinco subtipos:
- MASLD
Es un tipo de SLD que reemplaza el término NAFLD10–12. Se divide en MASL (Metabolic Dysfunction-Associated Steatotic Liver) y MASH (Metabolic Dysfunction-Associated Steato Hepatitis): - − MASL: reemplaza al término antiguo NAFL. Son pacientes que cumplen criterios para MASLD, pero no para MASH. En general esto requeriría una biopsia hepática, pero la tendencia actual es disminuir el número de biopsias y en la mayoría de los casos se puede inferir la ausencia de esteatohepatitis usando estudios no invasivos10–12.
- − MASH: reemplaza al término esteatohepatitis no alcohólica (NASH, Non-Alcoholic Steatohepatitis). Los criterios histológicos para ambas son los mismos10–12.
- Esteatosis hepática metabólica relacionada con el alcohol (MetALD, Metabolic Dysfunction and Alcohol-related Liver Disease)
Es un término nuevo en la nomenclatura para un subtipo de SLD que engloba pacientes con factores de riesgo cardiometabólico y que además tienen consumo de alcohol. Se clasifica como MetALD un consumo diario de alcohol de 20-50 g en las mujeres y 30-60 g en los hombres10–12. - Enfermedad hepática relacionada con el alcohol (ALD, Alcohol-associated Liver Disease)
Es un subtipo de SLD en el que el consumo diario de alcohol es > 50 g en las mujeres y > 60 g en los hombres10–12. - Otras etiologías específicas de SLD
En ausencia de factores de riesgo cardiometabólico y de consumo de alcohol, hay que buscar otras etiologías que generen esteatosis hepática, como pueden ser daño hepático inducido por fármacos, deficiencia de lipasa ácida lisosomal, enfermedad de Wilson, hipobetalipoproteinemia, errores innatos del metabolismo, infección por el virus de la hepatitis C, malnutrición, enfermedad celiaca, virus de la inmunodeficiencia humana y algunas exposiciones ambientales (como inhalación de hidrocarburos)9. - SLD criptogénica
La nueva nomenclatura reconoce que habrá pacientes que no tengan ninguna causa identificable, y estos requerirán seguimiento con posibilidad de ser reclasificados posteriormente en MASLD10–12. - 1)¿El paciente tiene esteatosis identificada por imagen (incluye elastografía transitoria) o biopsia?
- 2)¿El paciente presenta algún factor de riesgo cardiometabólico?
- 3)¿El paciente no tiene otra causa identificable de esteatosis hepática?
- – El término «metabólico» no siempre tiene un entendimiento claro para los pacientes. Se resuelve explicándolo y esto ayuda a una mayor concientización.
- – La disfunción metabólica que causa la MASLD es la resistencia a la insulina, pero de los factores de riesgo cardiometabólico para diagnosticarla no todos contribuyen igual a la resistencia a la insulina. Pudiera ser útil ponderar los distintos factores de riesgo para refinar el diagnóstico.
- – Una persona puede tener esteatosis hepática y resistencia a la insulina, por lo que recomendamos buscar el diagnóstico de resistencia a la insulina (HOMA [Homeostasis Model Assessment], pruebas de tolerancia oral a la glucosa) para diagnosticar la MASLD. Por ejemplo, la MASLD en pacientes delgados, aunque en estos puede corresponder a otros subtipos de SLD.
- – En pacientes con MetALD, establecer biomarcadores que permitan ver cuál de los dos componentes es el que predomina, ya que en la clasificación actual el consumo de alcohol se basa en la cantidad autorreportada.
- – Los pacientes, aun cuando tengan múltiples factores de riesgo cardiometabólico, si su consumo diario de alcohol es > 50 g en las mujeres o > 60 g en los hombres se califican como ALD, quitando el peso en la terminología del resto de los factores de riesgo cardiometabólico que puedan tener.
La población que tiene MASLD coincide con la antigua NAFLD, por lo que la información de esta aplica también a la nueva nomenclatura.
Una interrogante que surge ante cualquier cambio de nomenclatura es si este cambio seguirá incluyendo al mismo grupo de pacientes que la terminología previa. Asimismo, se presenta el problema de si el tratamiento empleado para los pacientes usando la terminología previa también aplica para la nueva. Song et al.16 analizaron a 1016 pacientes de la comunidad en Hong Kong. Se les realizó espectroscopía por resonancia magnética de protones y se encontraron 277 con triglicéridos intrahepáticos ≥ 5%. De estos, 247 (89.2%) cumplieron las tres definiciones (NAFLD, MAFLD y MASLD). Hagström et al.17 reportaron hallazgos similares en 1333 pacientes con diagnóstico previo de NAFLD, de los cuales el 99.7% cumplieron los criterios para MASLD. Esto aplicó para el diagnóstico, los biomarcadores y los desenlaces. Por ejemplo, a 10 años del diagnóstico, el 7.9% de los pacientes con NAFLD y el 7.8% de los pacientes con MASLD desarrollaron algún desenlace relacionado con el hígado, y fallecieron el 10.4% y el 10.3%, respectivamente17. Así, es vital mencionar que estamos estudiando la misma población con posibilidad de categorizar esta enfermedad y por lo tanto estudiarla, diagnosticarla y tratarla mejor.
Para incluir a los pacientes con NAFLD solo bastaría tener algún factor de riesgo cardiometabólico para clasificarlos como MASLD, situación que ocurre en el 95-99% de los casos18.
Otro aspecto que se abordó es la detección mediante métodos no invasivos de fibrosis avanzada, uno de los parámetros que más impacta en el pronóstico de la MASLD. En una cohorte francesa de 2187 pacientes se encontró que el área bajo la curva para detectar fibrosis avanzada por elastografía de transición e índice de fibrosis 4 (FIB-4) fue similar para ambas terminologías19.
Todo esto pone de manifiesto que el cambio de nomenclatura no implica una modificación sustancial en el conocimiento previo ni altera los fundamentos anteriormente establecidos sobre la fisiopatología de esta enfermedad.
Evolución natural (Fig. 3)
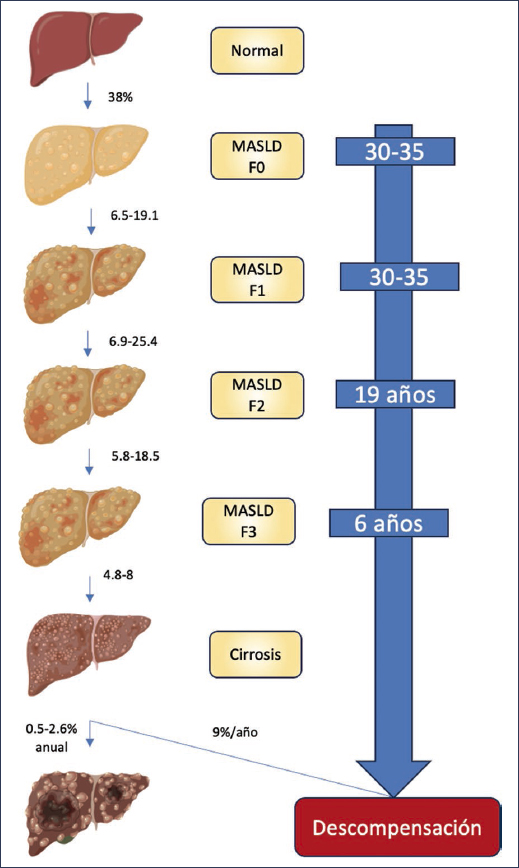
Figura 3. Evolución natural de la MASLD. Todas las tasas de progresión son casos por cada 100 personas-año (adaptada de Hagström et al.18).
La MASLD es la causa más común de enfermedad hepática crónica. Al ser una enfermedad multifactorial, habrá pacientes que progresarán a fibrosis avanzada y cirrosis, y otros no. Esto depende de los factores genéticos, los hábitos higiénico-dietéticos y la exposición a otros agentes hepatotóxicos, como el alcohol17.
Progresión a cirrosis hepática y descompensación
Parte de la importancia de la nueva nomenclatura radica en la identificación sencilla y oportuna de la MASLD con el objetivo primordial de dar un tratamiento temprano y oportuno que detenga la progresión a cirrosis hepática, con todas sus complicaciones y deterioro de la calidad de vida.
En un estudio en Olmsted County, en los Estados Unidos de América, que incluyó 5123 pacientes con MASLD diagnosticados en el primer nivel de atención, se encontró que el 3% progresarán a cirrosis hepática a 15 años20.
La velocidad con que los pacientes desarrollarán descompensaciones dependerá de la etapa de fibrosis en la que se encuentren en el momento del diagnóstico. En un estudio sueco con 646 pacientes diagnosticados de MASLD por biopsia, con una media de seguimiento de 20 años, se halló que de los pacientes F0 el 3.7%, de los F1 el 4.3%, de los F2 el 8.7%, de los F3 el 12.1% y de los F4 el 45% desarrollaron una descompensación durante el seguimiento. Se estimó que el tiempo promedio para presentar una descompensación fue de 33-34 años en F0-F1, 23 años en F2, 12 años en F3 y 6 años en F4. Esto pone de manifiesto que la etapa de la fibrosis constituye uno de los principales factores de progresión, y cuanto más temprano se detecte a los pacientes, más se podrá influir en la evolución natural de la enfermedad21.
Mortalidad relacionada con causas hepáticas y desenlaces en pacientes con cirrosis por MASLD
Los pacientes con MASLD presentan un problema dual, siendo uno la propia enfermedad hepática, con sus complicaciones en caso de progresar, y el otro todas las enfermedades relacionadas con el síndrome metabólico y las complicaciones asociadas a los factores de riesgo cardiovasculares.
En cuanto a la mortalidad relacionada con causas hepáticas, en una cohorte de 959 pacientes con MASLD corroborada por biopsia seguidos por una mediana de más de 18 años, de los pacientes que inicialmente tenían MASLD F0-F3 el 8-20% murieron por causas relacionadas con el hígado, mientras que de los que inicialmente presentaron cirrosis el 54% murieron en el seguimiento por causas hepáticas, por lo que la mortalidad asociada a causas hepáticas depende en mayor medida del grado de fibrosis22.
En un estudio prospectivo de 1773 pacientes con NAFLD seguidos por una mediana de 4 años se encontró que durante el tiempo de seguimiento la incidencia de mortalidad por todas las causas fue de 1.79, la de mortalidad relacionada con el hígado fue de 0.68, la de descompensación hepática fue de 2.69 y la de carcinoma hepatocelular fue de 0.14 por cada 100 personas-año23. En otro estudio, Ochoa-Allemant et al.24 analizaron la mortalidad por causa específica en una cohorte de 366,433 pacientes, diferenciando por primera vez MASLD, MetALD y ALD. Encontraron que las enfermedades cardiovasculares y el cáncer extrahepático, principalmente de pulmón y gastrointestinal, fueron las principales causas de mortalidad en los pacientes sin cirrosis hepática en todos los subtipos, mientras que en los pacientes con cirrosis hepática la mortalidad en todos los subtipos fue por causa hepática y por enfermedades cardiovasculares24. Esto debe tomarse en cuenta para la búsqueda sistemática del riesgo cardiovascular y el tamizaje oncológico con el fin de prevenir la mortalidad por estas causas.
Impacto de la nomenclatura en los pacientes
Estigma social
Una de las cuestiones que impulsaron el cambio en la nomenclatura fue la percepción de estigma con el término fatty (graso), aunque esta sensación de estigma puede ser variable dependiendo de la población estudiada. En una encuesta que se aplicó a 1976 pacientes con NAFLD en 23 países y a 825 trabajadores de la salud en 25 países, el 48% de los pacientes refirieron haber comentado el diagnóstico de NAFLD o NASH a sus familiares. El término MAFLD o enfermedad metabólica nunca fue utilizado en más del 84% de los pacientes, lo cual puede reflejar poca relevancia o escaso reconocimiento de la nueva terminología por la población o un pobre entendimiento de la misma. Al preguntar sobre la percepción de los términos NAFLD, FLD, NASH o MAFLD no se encontraron diferencias sustanciales. La respuesta más frecuente fue que los pacientes no se encontraban conformes ni inconformes con cualquiera de los términos (56-71% de las respuestas). Sin embargo, en los Estados Unidos de América y el sureste asiático, el 47-52% se mostraron inconformes con la terminología previa, lo cual puede poner de manifiesto cierta variabilidad en la percepción del estigma según la región, o también que la percepción del estigma depende en parte de la traducción al idioma local. El 8% reportaron haber vivido discriminación o estigmatización debido al término NAFLD. En cuanto a los trabajadores de la salud, el 38% consideraron el término fatty como estigmatizante25.
En México se realizó una encuesta a 163 personas en la Ciudad de México. De estas, el 69.5% indicaron el término alcohol como estigmatizante en el nombre de la enfermedad y preferirían retirarlo. Por otra parte, el 85.6% de los encuestados no percibieron la palabra fatty como estigmatizante y preferirían mantenerla en la terminología para facilitar la comunicación26.
Con los datos anteriores podemos pensar que la percepción de la terminología previa como estigmatizante varía entre pacientes, proveedores y regiones geográficas.
Empoderamiento
El término actual explica por sí solo que un aspecto fundamental es la presencia del síndrome metabólico o de factores de riesgo de este. Esto permite explicar a los pacientes de forma directa y positiva cuál es la razón de su enfermedad y, por ende, cuáles son las principales opciones preventivas y terapéuticas.
Es importante concientizar a los pacientes en cuanto a los cambios en la terminología y explicar a los previamente diagnosticados como NAFLD el cambio a MASLD y la razón de ello. Este cambio en la nomenclatura puede ser una oportunidad para explicar el término y concientizar acerca de la enfermedad27.
Sabemos que el pilar fundamental en la prevención y el tratamiento del síndrome metabólico son los cambios en el estilo de vida para mejorar el control glucémico, la presión arterial, la obesidad central y la dislipidemia, y para esto se requiere un compromiso importante por parte del paciente. Ligar este nuevo término con todos los componentes del síndrome metabólico permite al paciente reconocer con mayor facilidad su rol y cómo puede contribuir a mejorar la MASLD. También es fundamental informar a los enfermos sobre el estadio de fibrosis en el que se encuentran, ya que se ha observado que el desconocimiento de este aspecto se asocia con una baja adherencia a los cambios en el estilo de vida28.
Este nuevo término permite entender lo que sí está presente (disfunción metabólica) y no solo ver lo que no está (no alcohólico), así como comprender el porqué de las intervenciones terapéuticas y preventivas.
La nueva terminología, al no ser estigmatizante, permite a las personas con esta enfermedad tomar la decisión de buscar atención médica, unirse a grupos de ayuda o demandar apoyo dentro de su mismo núcleo familiar.
Criterios diagnósticos actuales y algoritmo diagnóstico de la SLD (Fig. 4)
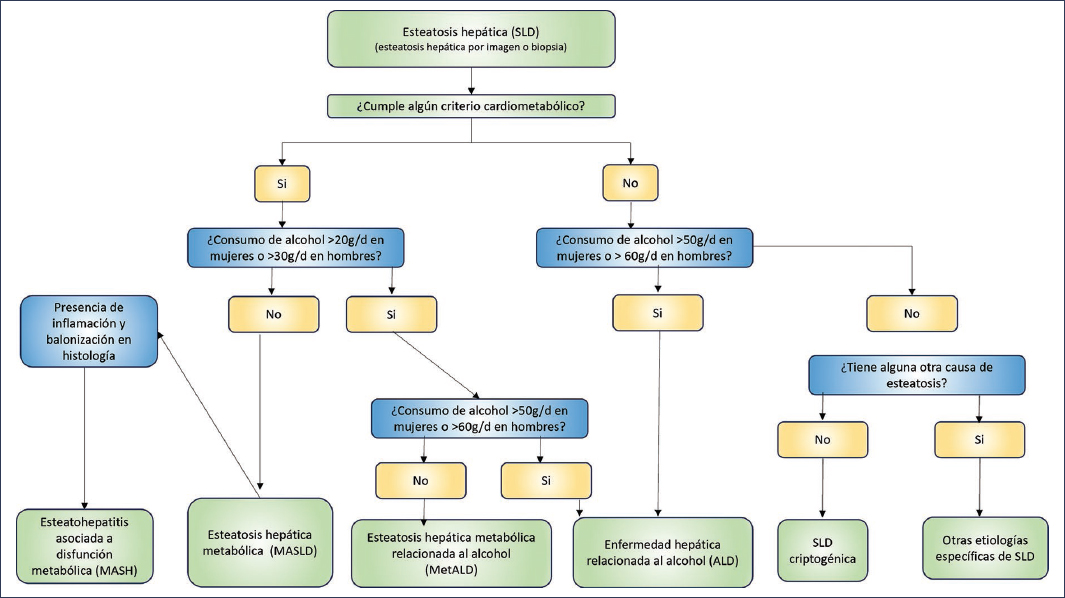
Figura 4. Algoritmo y criterios diagnósticos de MASLD y SLD.
De forma simplificada, se puede decir que si ante un paciente la respuesta a las siguientes tres preguntas es «sí» se establece el diagnóstico de MASLD:
Aspectos que deben mejorarse a futuro en la nomenclatura
Ciertamente, la nueva nomenclatura supone un paso enorme en el cuidado de los pacientes con MASLD, y además tiene la ventaja de que es perfectible y dinámica.
Aquí proponemos algunas áreas de oportunidad:
Conclusiones
La nueva nomenclatura permite unificar criterios para su uso tanto en la práctica clínica como en investigación, eliminando términos que resultan erróneos o estigmatizantes, y dejando claro que este no es un diagnóstico de descarte, sino un diagnóstico con criterios bien establecidos y basados en la fisiopatología de la enfermedad, que permite categorizarla. Esta nomenclatura aún es joven y sin duda veremos toda su aplicabilidad en los próximos años, así como las áreas que deben ser mejoradas.
Financiamiento
Los autores declaran no haber recibido financiamiento para este artículo.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. El estudio no involucra datos personales de pacientes ni requiere aprobación ética. No se aplican las guías SAGER.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no utilizaron ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.
