Introducción
El cáncer hepático es actualmente el sexto cáncer más común en todo el mundo y la tercera causa de muerte por cáncer1. Los estudios más recientes reportan que la esteatosis hepática metabólica (MASLD, Metabolic dysfunction Associated Steatotic Liver Disease) es la causa de carcinoma hepatocelular (CHC) con mayor aumento global2. El CHC relacionado con la MASLD (MASLD-CHC) tiene características particulares que lo diferencian de otras etiologías del CHC, como una mayor frecuencia en pacientes sin cirrosis hepática, tumores de mayor tamaño, estadio más avanzado en el momento del diagnóstico, mayor edad y más prevalencia de obesidad y otra comorbilidad metabólica3–5. Debido a estas características, las estrategias de cribado actuales parecen ser subóptimas en estos pacientes6. Además, el tratamiento del MASLD-CHC presenta algunos desafíos adicionales, sobre todo cuando es diagnosticado en estadios avanzados7.
El objetivo de esta revisión narrativa es analizar y sintetizar la evidencia disponible sobre el MASLD-CHC, abordando la epidemiología, los factores de riesgo, la patogénesis, el diagnóstico, el tratamiento, la prevención y las perspectivas futuras.
Método
Se llevó a cabo una revisión narrativa de la literatura sobre la relación entre la MASLD y el CHC. Para ello, se efectuó una búsqueda bibliográfica exhaustiva en PubMed/MEDLINE, Embase y Cochrane Controlled Register of Trials (CENTRAL), abarcando publicaciones desde 2005 hasta 2025. La estrategia de búsqueda combinó términos MeSH y palabras clave libres: “cirrosis”, “carcinoma hepatocelular”, “MASLD”, “MASH”, “NAFLD” y “NASH”. La selección de los estudios se basó en su relevancia temática y valor clínico, priorizando las revisiones sistemáticas con o sin metaanálisis, seguidas de los ensayos clínicos aleatorizados, los estudios de intervención no aleatorizados, los estudios observacionales (de casos y controles, transversales, cohortes) y, finalmente, series o reportes de casos y opiniones de expertos. Además, se realizó un cribado manual de las listas de referencias de los artículos relevantes para complementar la búsqueda electrónica. Dado el carácter narrativo de esta revisión, no se aplicaron criterios formales de revisión sistemática; en su lugar, la evidencia disponible se sintetizó de manera crítica y estructurada, con el objetivo de ofrecer una visión integral y actualizada del tema.
Epidemiología y carga global
La MASLD es la enfermedad hepática crónica más común, con una prevalencia global en la población general que ha aumentado desde el 25% en 2016 hasta más del 30% en los reportes más recientes8,9. El espectro clínico de la enfermedad abarca la esteatosis simple, la esteatohepatitis metabólica (MASH, Metabolic dysfunction Associated Steato Hepatitis), la fibrosis hepática, la cirrosis e incluso el CHC10. Se ha estimado que solo el 20% de los individuos con MASLD tienen MASH, y el 20% de estos desarrollarán cirrosis en un promedio de 2 a 4 décadas11.
El cáncer hepático es actualmente el sexto cáncer más común en todo el mundo y la tercera causa de muerte por cáncer1, con una incidencia que va en aumento, con la posibilidad de 1.4 millones de personas diagnosticadas con cáncer hepático para el año 204012. El CHC representa el 90% de los cánceres hepáticos y la mayoría de los casos surgen en el contexto de una enfermedad hepática crónica, siendo la cirrosis hepática el principal factor de riesgo para su desarrollo13, con hasta 30 veces mayor riesgo en comparación con pacientes sin cirrosis14.
La MASLD es la causa de CHC con mayor aumento en todo el mundo2. El MASLD-CHC representa alrededor del 10% de todos los casos de CHC15. Utilizando la información obtenida de la base de datos UNOS (United Network for Organ Sharing) de 2022, Koh et al.16 reportaron que la MASLD es la causa más frecuente de CHC en los candidatos a trasplante hepático en los Estados Unidos de América, superando a la hepatitis C crónica. En este registro, el MASLD-CHC representó el 24.3% de los casos de CHC en la lista de espera. Utilizando la modelización dinámica de Markov, se estima que la prevalencia de MASLD-CHC para el año 2030 aumentará hasta en un 130% en los Estados Unidos de América17.
La incidencia anual de CHC en pacientes con cirrosis por MASLD es actualmente del 0.5% al 2.6%15; sin embargo, utilizando el modelo predictivo antes mencionado, se ha predicho que la incidencia para el año 2030 podría aumentar hasta un 122% en los Estados Unidos de América17. Por otro lado, la frecuencia de MASLD-CHC es significativamente menor en los pacientes sin fibrosis, con una incidencia que varía de 0.8 a 1.2 por 1000 personas-año en los pacientes con esteatosis simple y con MASH sin fibrosis, respectivamente18.
Factores de riesgo para CHC en la MASLD
Existen numerosos factores de riesgo relacionados con el desarrollo de CHC en la MASLD, desde los asociados a la progresión de la enfermedad hepática crónica, como la fibrosis hepática, en la que la carcinogénesis es similar a la del CHC de otras etiologías19, hasta los que llevan a la activación de mecanismos fisiopatológicos no relacionados con la progresión de la fibrosis, como alteraciones metabólicas o inflamación crónica de bajo grado que resultan en mutaciones directas e indirectas de los factores oncogénicos, y que se postula que pueden ser la causa de la mayor susceptibilidad para desarrollar CHC19,20.
Fibrosis hepática y cirrosis
La inflamación hepática (esteatohepatitis) es el principal motor para el desarrollo de fibrosis hepática en la MASLD, y el grado de fibrosis constituye el factor pronóstico más importante para la progresión de la enfermedad y sus complicaciones, incluyendo el desarrollo de CHC. Una revisión sistemática y metaanálisis demostró que el riesgo de CHC aumenta de forma progresiva conforme el estadio de la fibrosis21. La fibrosis avanzada, definida como un estadio de METAVIR ≥ 3, se ha asociado con el desarrollo de descompensación hepática (ascitis, hemorragia variceal y encefalopatía hepática), trasplante hepático, mortalidad y CHC22–25.
Como ya se ha mencionado, la proporción de pacientes con CHC sin cirrosis es notablemente mayor en el MASLD-CHC, con estudios que reportan frecuencias que varían desde el 20% hasta el 63%4,26–29. Una revisión sistemática y metaanálisis que incluyó 19 estudios con 168,571 pacientes reportó una prevalencia de CHC en la MASH sin cirrosis del 38%, en comparación con un 14.2% en los pacientes con enfermedad hepática de otras etiologías (p < 0.001), con una mayor probabilidad de desarrollar CHC (odds ratio [OR]: 2.61; intervalo de confianza del 95% [IC 95%]: 1.27-5.35; p = 0.009)3.
Obesidad
La obesidad es el factor de riesgo para MASLD más ampliamente descrito. La grasa visceral es uno de los componentes más importantes en la fisiopatología de la enfermedad19. La presencia, la duración y la gravedad de la obesidad se han relacionado con riesgo de progresión de la enfermedad hepática, así como de progresión de la fibrosis30, desarrollo de descompensación hepática31 y aumento de hasta cuatro veces el riesgo de CHC (OR: 4.3; IC 95%: 2.1-8.4), reportando además una relación sinérgica entre la obesidad y otros factores de riesgo, como el consumo de alcohol y de tabaco32. Otros estudios han corroborado estos resultados; Borena et al. reportaron que el índice de masa corporal (IMC) se asocia con un riesgo relativo de cáncer primario hepático de 1.39 (IC 95%: 1.24-2.58)33, mientras que en un análisis multivariado de regresión logística Archambeaud et al.34 reportaron que la obesidad (IMC ≥ 30 kg/m1) es un factor de riesgo independiente para el desarrollo de CHC.
Diabetes mellitus tipo 2
La diabetes mellitus tipo 2 (DM2) es la segunda alteración metabólica más importante en la MASLD. La presencia de DM2 se ha asociado con el desarrollo de CHC independientemente de la etiología de la enfermedad hepática19,35. En un estudio Europeo que incluyó 136,703 pacientes con MASLD o MASH, la DM2 constituyó el principal factor asociado a un riesgo triplicado de CHC (hazard ratio [HR]: 3.51; IC 95%: 1.72-7.16)36. Otro estudio realizado en los Estados Unidos de América reportó un riesgo de CHC aún más elevado (HR: 4.2; IC 95%: 1.2-14.2; p = 0.02), sin una asociación significativa entre el riesgo de CHC y otros factores metabólicos como el IMC, la dislipidemia o la hipertensión arterial37. Por el contrario, en el estudio de Kanwal et al.38 el riesgo aumentó de forma progresiva con el número de alteraciones metabólicas (DM2, hipertensión, dislipidemia y obesidad), reportando un riesgo de desarrollar CHC o cirrosis hepática hasta dos veces mayor en los pacientes con DM2, obesidad, dislipidemia o hipertensión (HR: 2.6; IC 95%: 2.3-2.9). También se ha reportado que la duración de la DM2 tiene un impacto en el riesgo de CHC, con mayor riesgo en pacientes con DM2 de más de 10 años de diagnóstico (OR ajustada: 2.2; IC 95%: 1.2-4.8)39.
Consumo de alcohol
El alcohol ha demostrado ser un importante factor de riesgo para la progresión de la MASLD, con estudios que indican que una cantidad pequeña (5-9 bebidas/semana) a moderada (10-13 bebidas/semana) incrementa de forma significativa el riesgo de fibrosis hepática, con un efecto aditivo y dependiente de la dosis conforme aumenta el número de factores de riesgo cardiometabólicos40. Además, el consumo de alcohol se ha asociado con el desarrollo de CHC en pacientes con cirrosis hepática de cualquier etiología, con un incremento de hasta seis veces el riesgo de CHC (OR: 5.7; IC 95%: 2.4-13.7)32 y con un efecto sinérgico cuando se combina con obesidad (IMC ≥ 30 kg/m1) (HR: 3.82; IC 95%: 1.94-7.52; p < 0.01)41. En cuanto al MASLD-CHC, Kimura et al.42 demostraron que incluso un consumo de alcohol leve (< 20 g/día) se asocia con un aumento en la tasa de aparición de CHC en comparación con los pacientes sin consumo de alcohol (6.5% vs. 1.4%; p = 0.02); el efecto del consumo de alcohol contribuyó de forma importante al desarrollo de CHC, sobre todo en los pacientes con fibrosis avanzada (F3-4). Un metaanálisis que incluyó 31 estudios y más de 1 millón de individuos reportó que el consumo de alcohol se asoció con un aumento del riesgo de MASLD-CHC de hasta el 140% (2.41 OR; IC 95%: 1.03-5.65)43.
Consumo de tabaco
El consumo de tabaco se ha asociado con un mayor riesgo de CHC en pacientes con cirrosis hepática por cualquier etiología, incluyendo la MASLD43,44. Los resultados de la revisión sistemática realizada por Abdel-Rahman et al.44, que incluyó 81 estudios epidemiológicos, reportan una OR combinada para el desarrollo de CHC en fumadores actuales de 1.55 (IC 95%: 1.46-1.65; p < 0.00001), en exfumadores de 1.39 (IC 95%: 1.26-1.52; p < 0.00001) y en fumadores intensos de 1.90 (IC 95%: 1.68-2.14; p < 0.00001). En el metaanálisis antes mecionado43, el consumo de tabaco se asoció con un 30% mayor riesgo de MASLD-CHC (1.3 OR; IC 95%: 1.08-1.57). Y más recientemente, un estudio de corte retrospectivo que incluyó solo pacientes con MASLD reportó resultados similares, con una mayor incidencia de CHC en aquellos con consumo de tabaco actual o previo45.
Patogénesis del desarrollo de CHC en los pacientes con MASLD
La oncogénesis en la MASLD es consecuencia de múltiples vías desreguladas que contribuyen al daño hepatocelular y al desarrollo de fibrosis hepática19. La MASLD se caracteriza por una acumulación de lípidos que ocasionan lipotoxicidad, es decir, daño hepatocelular secundario a la alteración del metabolismo de la grasa, resultando en una producción excesiva de ácidos grasos libres que promueven la formación de especies reactivas de oxígeno e inducen estrés del retículo endoplásmico, daño mitocondrial, y transcripción de genes, activando vías de señalización inflamatorias y ocasionando un estado de inflamación crónica que eventualmente lleva a la fibrogénesis20,46. Estas alteraciones contribuyen a la carcinogénesis mediada por el daño oxidativo del DNA y la acumulacion de mutaciones en genes como FOXO1, CIDEB y GPAM47. En la tumorogénesis del MASLD-CHC se han implicado mútiples vías oncogénicas aberrantes, como señalización Wnt/β-catenina, fosfatidilinositol-3-cinasa/proteína cinasa B/objetivo de la rapamicina en mamíferos (PI3K/Akt/mTOR), Myc, señalización Hedgehog y transición epitelio-mesenquimatosa, que se ha asociado con las metástasis y la migración celular46.
Otros mecanismos fisiopatológicos implicados son la angiogénesis, con aumento en la expresión de CD34 y el factor de crecimiento endotelial vascular (VEGF, Vascular Endothelial Growth Factor), así como una disrupción del sistema inmunitario con depleción de las células T CD8+ y TCD4+, con una posible implicación en la respuesta a la inmunoterapia para el cáncer47.
Diagnóstico de CHC en los pacientes con MASLD
El MASLD-CHC tiene unas características particulares que lo diferencian de otras causas de CHC. Además de su aparición en ausencia de cirrosis3, se ha reportado que los pacientes con fibrosis leve a moderada (estadios F0-2) presentan tumores de mayor tamaño (93 ± 52 vs. 53 ±35 mm; p < 0.001) en comparación con los pacientes con MASLD y fibrosis avanzada (estadios F3-4), así como una mayor frecuencia de no ser candidatos a trasplante hepático según los criterios de Milán y de la Universidad de California (73% vs. 36% y 66% vs. 25%, respectivamente)4. Una revisión sistemática y metaanálisis que incluyó 61 estudios y 3631 pacientes reportó que aquellos con MASLD-CHC eran de mayor edad, tenían un IMC más alto y presentaban mayor comorbilidad metabólica, en comparación con los que presentaban CHC debido a otras etiologías, además de un mayor diámetro tumoral, con una diferencia media de 0.67 cm (IC 95%: 0.35-0.98; p = 0.0087), y una mayor probabilidad de lesiones uninodulares (OR: 1.36; IC 95%: 1.19-1.56; p = 0.0003). A pesar de esto, no se observaron diferencias significativas entre ambos grupos en cuanto a la distribución por estadios del sistema BCLC (Barcelona Clinic Liver Cancer), el sistema TNM (Tamaño, Nódulos, Metástasis), el estado funcional según la escala ECOG (Eastern Cooperative Oncology Group), el tratamiento otorgado ni la supervivencia5. Más recientemente, el análisis de una base de datos italiana (ITA.LI.CA) ha reportado resultados similares: los pacientes con MASLD-CHC fueron con mayor frecuencia hombres, con una edad promedio mayor y con menor frecuencia de cirrosis hepática (84% vs. 94%) e hipertensión portal clínicamente significativa (75% vs. 82%)48. En cuanto a la carga tumoral, hubo una mayor frecuencia de tumores de gran tamaño (27% vs. 21%) y con metástasis extrahepáticas (7% vs. 3%). Sin embargo, a pesar de tener un estadio tumoral más avanzado en el momento del diagnóstico, los pacientes con MASLD-CHC tuvieron un menor riesgo de muerte relacionada con el CHC, aunque sí mostraron un riesgo significativamente mayor de mortalidad no relacionada con el CHC (p = 0.006)48.
La figura 1 describe las características del MASLD-CHC.
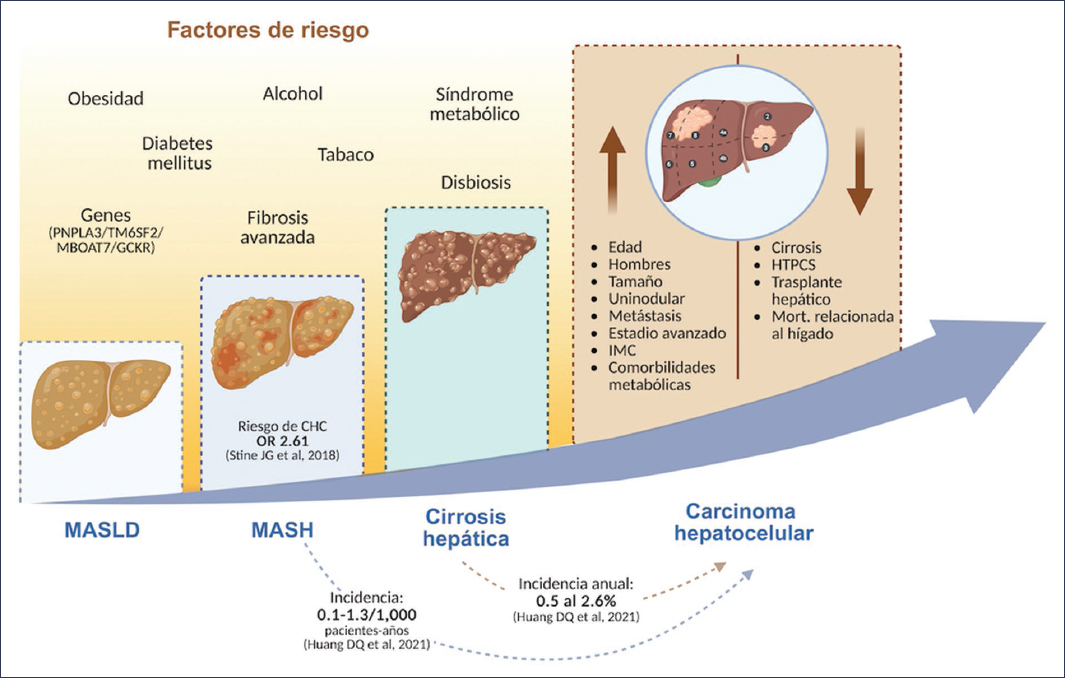
Figura 1. Factores de riesgo y características clínicas del MASLD-CHC. HTPCS: hipertensión portal clínicamente significativa; IMC: índice de masa corporal; MASLD: Metabolic dysfunction Associated Steatotic Liver Disease; MASH: Metabolic dysfunction Associated Steato Hepatitis.
Debido a que la función hepática en la MASLD-CHC suele estar respetada, una proporción significativa de pacientes no se encuentran en un programa de cribado y el diagnóstico de CHC suele ser incidental20,46. Las guías actuales establecen que el diagnóstico de CHC puede realizarse de forma no invasiva mediante estudios de imagen, ya sea por resonancia magnética (RM) o tomografía computarizada (TC) contrastadas multifásicas en pacientes con cirrosis hepática o con hepatitis crónica B49, observando hiperrealce en la fase arterial (APHE, Arterial Phase Hyperenhancement) y posteriormente lavado del contraste y presencia de cápsula en las fases venosa-portal o tardía, reportando los resultados de acuerdo con la terminología estandarizada del sistema LI-RADS (Liver Imaging Reporting and Data System)50. Si la RM y la TC no están disponibles, puede utilizarse el ultrasonido contrastado, aunque es una herramienta con poca utilidad para la estadificación. El diagnóstico invasivo mediante biopsia hepática debe reservarse para pacientes sin cirrosis o en caso de duda diagnóstica49.
Al igual que el CHC de otras etiologías, el diagnóstico de CHC en pacientes con cirrosis por MASLD puede establecerse mediante los estudios de imagen estándar (RM o TC). Una revisión sistemática y metaanálisis que incluyó 170 pacientes demostró que aquellos con MASLD-CHC tienen una frecuencia similar de APHE, aunque con una menor frecuencia de lavado y cápsula; los porcentajes estimados globales de APHE, lavado y cápsula fueron del 94.0% (IC 95%: 89.1-96.7), el 72.7% (IC 95%: 63.3-80.4) y el 57.5% (IC 95%: 45.1-69.1), respectivamente51. En comparación con la TC, la RM mostró un porcentaje agrupado más alto de cápsula (67.1% vs. 44.7%; p = 0.02)51. De forma similar, los estudios realizados en pacientes sin cirrosis han demostrado que el aspecto radiológico del CHC en la TC y la RM es típico en más del 80% de los casos, sin diferencias significativas en los patrones imagenológicos de los pacientes con y sin cirrosis52, lo que sugiere que los criterios no invasivos deberían extenderse a este grupo de pacientes. Al respecto, Barat et al.53 llevaron a cabo un estudio retrospectivo que demostró la aplicabilidad del sistema diagnóstico LI-RADS (v2018) en pacientes con MASLD-CHC, al no encontrar diferencias significativas entre las RM de pacientes con MASLD y de pacientes con hepatitis viral crónica.
Manejo del CHC en los pacientes con MASLD
El manejo actual del CHC está basado en el sistema de estadificación BCLC, que clasifica a los pacientes en cinco estadios (0, A-D) considerando la carga tumoral, la función hepática y el estado de salud asociado al cáncer, proponiendo un abordaje terapéutico basado en evidencia científica actualizada, con opciones quirúrgicas, tratamientos locorregionales y opciones de tratamiento sistémico para los pacientes en estadios avanzados54. El tratamiento del CHC en la MASLD presenta algunos desafíos adicionales, como se ha mencionado previamente, pues los pacientes con MASLD tienen una mayor prevalencia de comorbilidad cardiometabólica y suelen ser diagnosticados en estadios más avanzados, por lo que las opciones terapéuticas podrían estar limitadas46.
Manejo del CHC en estadios tempranos (BCLC 0-A)
En cuanto a los estadios iniciales, las terapias curativas incluyen la resección quirúrgica, el trasplante hepático y los tratamientos ablativos. Diversos estudios han evaluado la eficacia de estas terapias en los pacientes con MASLD. Un metaanálisis de 17 estudios retrospectivos reportó que los pacientes con MASLD-CHC podrían tener mayores supervivencia en general (HR: 0.87; IC 95%: 0.75-1.02) y supervivencia libre de recurrencia (HR: 0.93; IC 95%: 0.84-1.02) posterior a la hepatectomía, así como una tasa de complicaciones perioperatorias y una mortalidad similares a las de los pacientes con CHC de otras etiologías55. Los estudios que han evaluado la efectividad de las terapias ablativas (radiofrecuencia o microondas) en los pacientes con MASLD-CHC reportan que no existe diferencia en cuanto a la supervivencia, la morbilidad ni la recurrencia del tumor posterior a la ablación56,57.
La MASLD se ha convertido en la segunda causa más frecuente de trasplante hepático en los Estados Unidos de América58. Se ha postulado que los pacientes con MASLD podrían tener una mayor tasa de complicaciones peri- y postrasplante debido a la mayor prevalencia de enfermedad cardiovascular59; sin embargo, un reciente metaanálisis de 10 estudios comparativos con 51,761 pacientes demostró que la supervivencia a 1, 3 y 5 años, así como la supervivencia libre de enfermedad posterior al trasplante hepático, es similar en los pacientes con MASLD-CHC y en aquellos con CHC de otras etiologías60. En conclusión, los estudios sugieren que, a pesar del aumento en la prevalencia de comorbilidad, incluyendo la enfermedad cardiovascular, y el riesgo de tumores de mayor tamaño, no existe diferencia en la aplicación de terapias curativas en los pacientes con MASLD-CHC5, aunque algunos estudios reportan hasta un 47% de menor probabilidad de recibir cualquier tratamiento curativo debido al estadio más avanzado en el momento del diagnóstico56.
Manejo del CHC en estadio intermedio (BCLC B)
Las terapias locorregionales son el tratamiento de elección para los pacientes con CHC en estadio intermedio con lesiones bien delimitadas y flujo portal conservado54. Dentro de estas se encuentran la TACE (Transcatheter Arterial Chemoembolization) y la TARE (Transcatheter Arterial Radioembolization). Un estudio retrospectivo demostró que la TACE es igual de efectiva en los pacientes con MASLD-CHC en comparación con pacientes con CHC de otras etiologías, a pesar de tener lesiones de mayor tamaño (4.9 ± 5.8 vs 3.1 ± 2.4 cm), y sin un aumento en la tasa de complicaciones61. Los estudios que han evaluado la efectividad y la seguridad de la TARE en pacientes con MASLD-CHC reportan resultados similares en cuanto a seguridad, supervivencia en general y supervivencia libre de progresión local o hepática62,63.
Manejo del CHC avanzado (BCLC C)
El manejo del CHC avanzado está basado en la administración de tratamiento sistémico con inmunoterapia con inhibidores de puntos de control inmunitario (ICI)54. Basándose en los resultados de los ensayos clínicos IMbrave15064 e HYMALAYA65, las guías de tratamiento actuales establecen que las combinaciones atezolizumab-bevacizumab y durvalumab-tremelimumab son las opciones de primera línea49,54. De acuerdo con la actualización del algoritmo terapéutico del BCLC 2025, la combinación de nivolumab más ipilimumab se incorpora como una opción adicional de inmunoterapia en primera línea en escenarios clínicos seleccionados, recomendación que se fundamenta en los resultados del ensayo CheckMate 9DW, que demostró una mejora en la supervivencia global frente a sorafenib, junto con una mayor durabilidad de la respuesta, respaldando el papel del doble bloqueo inmunitario (PD-1/CTLA-4) en el tratamiento del CHC avanzado (Reig M, et al. BCLC 2025 strategy for prognosis prediction and treatment allocation in hepatocellular carcinoma. J Hepatol. 2025.)
Los resultados de estudios experimentales, retrospectivos e incluso de un metaanálisis de ensayos clínicos aleatorizados sugirieron inicialmente que la etiología del CHC podría influir en la respuesta a la inmunoterapia7,66. El metaanálisis mencionado reportó que los ICI fueron significativamente más eficaces en el CHC asociado a hepatitis viral que en el CHC de otras etiologías. Por el contrario, la etiología de la enfermedad hepática no pareció influir en la eficacia de los inhibidores de la tirosina cinasa ni de las terapias anti-VEGF7. Esta menor respuesta al tratamiento descrita en los pacientes con MASLD-CHC podría estar relacionada con la infiltración tumoral por macrófagos CCR2+ y CX3CR1+, así como con un deterioro en la “condición funcional” de los linfocitos T, lo que podría contribuir a la resistencia terapéutica a los ICI47. Además, se ha descrito que el CHC es habitualmente un tumor inmunológicamente «frío», es decir, un tumor inmunodeficiente o con funciones inmunitarias innatas deterioradas, con una baja expresión de PD-L1, escasa carga mutacional, disminución de la expresión de moléculas implicadas en la presentación antigénica y una infiltración limitada de linfocitos T67.
Aparte de una posible menor eficacia, el uso de tratamiento sistémico en estos pacientes podría verse condicionado por la presencia de síndrome metabólico, ya que la hipertensión arterial y la enfermedad cardiovascular pueden agravarse con el uso de estos fármacos20. No obstante, estudios más recientes han aportado resultados opuestos. Así, un análisis post hoc del estudio IMbrave150 no identificó diferencias significativas en cuanto a la respuesta objetiva evaluada con los criterios RECIST y RECIST modificado, ni en la supervivencia libre de progresión o la supervivencia en general, entre los pacientes con MASLD-CHC y aquellos con CHC de otras etiologías68.
En concordancia con estos resultados, un estudio retrospectivo que incluyó 295 pacientes tratados con atezolizumab–bevacizumab mostró que el número de factores de riesgo cardiovascular no tuvo impacto en la supervivencia global ni en la supervivencia libre de progresión69. En este mismo sentido, un reciente metaanálisis que incluyó los ensayos clínicos CheckMate 459, KEYNOTE-240, IMbrave150, COSMIC-312, HIMALAYA, LEAP-002, RATIONALE-301 y camrelizumab–rivoceranib demostró que la inmunoterapia ofrece una ventaja significativa en supervivencia tanto en el CHC de etiología viral como en el no viral, siendo el ensayo HIMALAYA el que mostró el mayor beneficio con ICI, lo cual destaca la importancia de la inhibición de CTLA-4 en este subgrupo de pacientes70. Estos hallazgos parecen más robustos, ya que en los estudios iniciales los resultados reportados estaban basados en subanálisis, sin definir que porcentaje de los pacientes con cirrosis no viral fueron verdaderamente pacientes con MASLD7. Hasta la fecha, no existen ensayos clínicos controlados aleatorizados diseñados específicamente para evaluar la respuesta a la inmunoterapia en pacientes con MASLD-CHC71, por lo que el tratamiento de primera línea continúa siendo el recomendado por las guías clínicas más recientes.
Prevención del CHC en los pacientes con MASLD
Las guías actuales recomiendan realizar cribado de CHC en todos los pacientes con cirrosis hepática, independientemente de su etiología. Si la función hepática permite el tratamiento oncológico, el cribado debe incluir la realización de ultrasonido abdominal cada 6 meses con o sin determinación de las concentraciones séricas de alfafetoproteína49; sin embargo, el desempeño del ultrasonido abdominal puede ser subóptimo en los pacientes con obesidad, que es uno de los factores metabólicos más prevalentes en esta enfermedad6, con una disminución de la sensibilidad y de la especificidad debido a la posible inadecuada visualización del parénquima hepático en los pacientes con MASH47. Hasta la fecha no se justifica el cribado sistemático en los pacientes sin fibrosis avanzada72,73. Además del ultrasonido, biomarcadores como el índice de fibrosis 4 (FIB-4, con punto de corte > 3.2)26 y el incremento en la dureza hepática evaluada por elastografía74 se asocian con un aumento del riesgo de CHC.
Se han diseñado diversos modelos de estratificación del riesgo de CHC en pacientes con cirrosis hepática, algunos de ellos específicos para la MASLD. El modelo de Ioannou et al.75, basado en siete predictores (edad, sexo, DM2, IMC, conteo plaquetario, albúmina sérica y relación entre aspartato aminotransferasa y alanina aminotransferasa), mostró un área bajo la curva ROC (AUROC) de 0.75. Otro modelo italiano confirmó que la combinacion de parámetros como el genotipo de PNPLA3, las pruebas de función hepática y la presencia de hipertensión portal fue útil para estimar el riesgo de CHC76.Y más recientemente, Lambrech et al.77 desarrollaron el puntaje APAC, basado en la edad, el receptor beta del factor de crecimiento derivado de plaquetas soluble, la alfa-fetoproteína y la creatinina, con una buena capacidad de predicción del CHC en pacientes con MASLD (AUROC 0.75)35.
Perspectivas futuras y medicina de precisión
La tendencia ascendente en la prevalencia de la MASLD es un determinante clave en la futura carga global del MASLD-CHC17. Como se ha descrito previamente, el MASLD-CHC presenta características específicas que lo convierten en un reto diagnóstico y terapéutico7, lo cual lleva a la inminente necesidad de implementar programas y mejorar las herramientas de cribado de CHC en pacientes con MASLD y fibrosis avanzada, con la integración de biomarcadores séricos e incluso con la aplicación de modelos de ultrasonido basados en inteligencia artificial (machine learning) para detectar el MASLD-CHC en estadios más tempranos20, así como estudios prospectivos sobre la respuesta al tratamiento con inmunoterapia en los distintos fenotipos de la MASLD19.
Financiamiento
Los autores declaran no haber recibido financiamiento para este estudio.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. El estudio no involucra datos personales de pacientes ni requiere aprobación ética. No se aplican las guías SAGER.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no utilizaron ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.
