Introducción
La dieta como intervención terapéutica no farmacológica se define como la modificación estructurada y personalizada (basándose en características físicas y necesidades nutricionales de acuerdo a patologías) de los hábitos de alimentación con la finalidad de mejorar el estado clínico y metabólico de los pacientes. Centrándonos en la esteatosis hepática metabólica (MASLD, metabolic-associated steatotic liver disease), la intervención nutricional es el pilar fundamental del manejo clínico, pues han demostrado lograr una mejoría de los parámetros metabólicos, así como una disminución de la resistencia a la insulina y de la inflamación sistémica, aunado a que la pérdida de peso asociada logra revertir la acumulación de lípidos intrahepáticos, factor clave en la progresión de la enfermedad hepática; en aquellos pacientes con fibrosis leve que logran una pérdida de peso > 0% de peso puede conseguirse la reversión de la misma1.
Además, la intervención nutricional combinada con actividad física regular potencia los beneficios metabólicos, favoreciendo la pérdida de peso sostenida, y mejora el perfil inflamatorio. Este enfoque multidisciplinario es esencial dado que la MASLD es una enfermedad compleja con múltiples factores etiológicos relacionados con el síndrome metabólico. Por lo tanto, la personalización de la dieta y la adherencia a largo plazo son cruciales para lograr resultados clínicos significativos y sostenibles2.
Importancia de la dieta en el tratamiento del espectro de la esteatosis hepática metabólica
La dieta desempeña un papel crucial en el manejo de MASLD en coadyuvancia con la terapia farmacológica. La reducción de peso lograda mediante restricción calórica y dieta saludable puede lograr una mejoría de las enzimas hepáticas, la grasa intrahepática, la inflamación hepática y la fibrosis, de manera dependiente del apego. Las guías de práctica clínica de la European Association for the Study of the Liver (EASL), la European Association for the Study of Diabetes (EASD) y la European Association for the Study of Obesity (EASO), y la guía de la European Society for Clinical Nutrition and Metabolism (ESPEN), recomiendan una pérdida de peso del 7% al 10% para mejorar la esteatosis y la bioquímica hepática, y de > 10% para hacer retroceder la fibrosis. Los pacientes de peso normal pueden beneficiarse de la reducción de la grasa visceral mediante la dieta y la actividad física; sin exigir una pérdida de peso > 5% se puede lograr la remisión de la esteatosis. Los pacientes con peso normal suelen cursar con determinantes genéticos que pueden beneficiarse de modificaciones dietéticas, en especial aquellos con el alelo G rs738409 de PNPLA3, genotipo que amplifica la influencia de la ingesta dietética. Además, la relación entre algunos nutrientes dietéticos específicos y el riesgo de fibrosis es más fuerte para los individuos con esta modificación genética3,4.
Para que una intervención nutricional sea óptima debe combinar perfectamente los aspectos cualitativos y cuantitativos de una nutrición adecuada, considerando el papel de los macro- y micronutrientes individuales en la aparición y el desarrollo de la enfermedad, así como la importancia de modular su ingesta diaria para promover la pérdida de peso y contrarrestar las condiciones patológicas colaterales5.La evidencia demuestra que, independientemente de la ingesta calórica total, ciertos macronutrientes específicos son cruciales en el desarrollo y la progresión de la MASLD; entre ellos, los hidratos de carbono, en particular la fructosa, tienen una relación estrecha con la aparición y la progresión de la MASLD. En este contexto, es esencial regular el consumo dietético total de hidratos de carbono, especialmente de aquellos con un alto índice glucémico, ya que la ingesta excesiva puede contribuir a la obesidad y las alteraciones metabólicas. Reducir la ingesta de hidratos de carbono puede mejorar de manera significativa los resultados relacionados con la MASLD, incluido el contenido hepático de triglicéridos, la trigliceridemia, la oxidación lipídica y la resistencia a la insulina3.
¿Es tiempo de un tratamiento individualizado en la dieta?
El espectro clínico de la MASLD abarca una variedad de fenotipos que van desde la esteatosis simple hasta la esteatohepatitis, condiciones que se diferencian por la presencia variable de inflamación bioquímica (elevación de las transaminasas o de los marcadores séricos de inflamación, como las interleucinas) y de daño hepático con evidencia de infiltrado inflamatorio en el tejido hepático, aunado a la presencia de fibrosis hepática y la gravedad de esta6.
Además de estos fenotipos clínicos, en la MASLD coexiste comorbilidad cardiometabólica, como sobrepeso y obesidad, resistencia a la insulina, diabetes tipo 2, dislipidemia aterogénica (caracterizada por un aumento del colesterol unido a lipoproteínas de baja densidad y una diminución del colesterol unido a lipoproteínas de alta densidad) e hipertensión arterial. La coexistencia de comorbilidad no solo agrava el pronóstico hepático, sino que también incrementa el riesgo cardiovascular global del paciente1.
Por lo anterior, antes de establecer una intervención nutricional en la MASLD se debe considerar y analizar la heterogeneidad de la comorbilidad presente en cada paciente, aunado a la presencia o no de inflamación (esteatohepatitis) y fibrosis hepática. Por ejemplo, en pacientes con obesidad que cumplen criterios de síndrome metabólico se ha demostrado que la restricción calórica con énfasis en la calidad de los macronutrientes, como la adopción de patrones dietéticos de estilo mediterráneo ricos en grasas monoinsaturadas y poliinsaturadas, mejora la sensibilidad a la insulina, reduce la carga lipídica hepática y modula la inflamación sistémica2. En los pacientes con diabetes tipo 2, el control estricto de la ingesta de glucosa y de alimentos con un alto índice glucémico es esencial para mejorar el metabolismo hepático y prevenir la progresión de la enfermedad7. Por tanto, cada situación de comorbilidad impone unos requisitos nutricionales específicos que deben ser abordados para optimizar los resultados terapéuticos.
La necesidad de individualizar las estrategias dietéticas en la MASLD radica en la compleja interacción de los fenotipos clínicos, la comorbilidad asociada y las características individuales del paciente, incluyendo factores sociales, genéticos, bioquímicos y ambientales. Los estudios resaltan que una «talla única» o plan único en las recomendaciones nutricionales resulta insuficiente e inefectivo para alcanzar la mejoría metabólica y lograr un seguimiento a largo plazo. La personalización de la dieta, integrando las preferencias culturales, el perfil metabólico y biomarcadores específicos, permite un enfoque eficiente y sostenible a largo plazo, promoviendo la adherencia y logrando mejores resultados clínicos8. De manera general, las recomendaciones nutricionales deben minimizar los alimentos ultraprocesados, los alimentos y las bebidas azucarados, y las grasas saturadas4.
Algunas recomendaciones dietéticas que desde un punto de vista práctico pueden ser de gran utilidad para el personal médico de primer contacto se basan en:
- − Reducir la ingesta total de energía: una restricción calórica moderada (500-1000 kcal/día) puede lograrse con diferentes patrones dietéticos; perder un 5-10% del peso corporal en un periodo de 6 meses.
- − Seguir un patrón de alimentación saludable y equilibrado, adecuado al contexto del paciente: rica en frutas, verduras, cereales integrales, legumbres, frutos secos, pescado y aceite de oliva, y baja en carnes rojas y procesadas, hidratos de carbono refinados y grasas saturadas.
- − Limitar el consumo de azúcares añadidos y de hidratos de carbono refinados: evitar o limitar el consumo de bebidas azucaradas, dulces y refrigerios densamente energéticos.
- − Evitar la ingesta de alcohol: el alcohol puede agravar el daño hepático, por lo que se debe evitar o limitar su consumo.
- − Reducir la ingesta de grasas saturadas.
Debemos recordar que los objetivos a largo plazo se centran en reducir la grasa intrahepática, mejorar la fibrosis y prevenir las complicaciones metabólicas y hepáticas. En conclusión, y en respuesta a la pregunta de si es tiempo de un tratamiento individualizado en la dieta, la respuesta es sí: la individualización de la dieta no solo es un imperativo clínico, sino también una estrategia fundamental para mejorar la calidad de vida y el pronóstico de los pacientes con MASLD y su comorbilidad (Fig. 1).
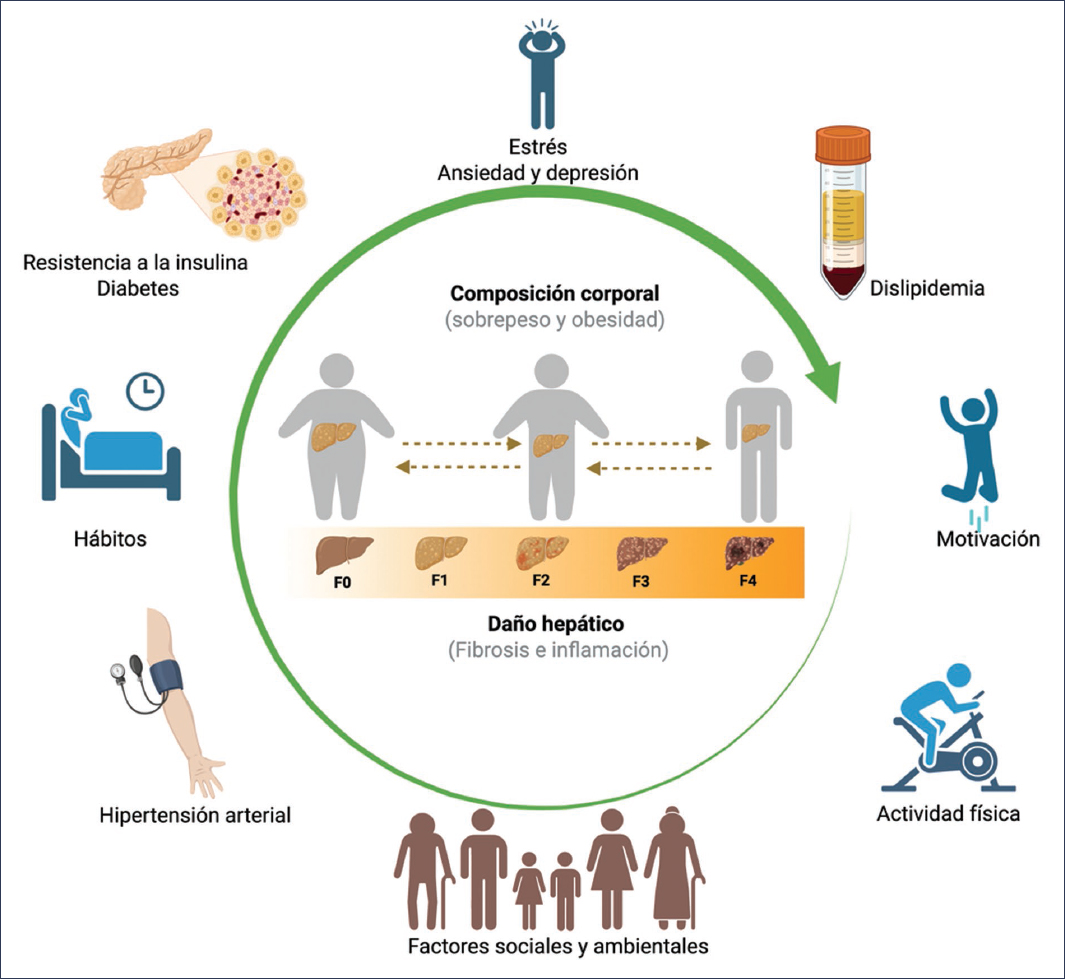
Figura 1. Componentes que se deben de considerar para la personalización de los planes nutricionales en pacientes con MASLD (creada en BioRender).
¿Cuál es la mejor dieta para los pacientes con esteatosis hepática metabólica?
Se ha demostrado claramente el vínculo entre unos hábitos alimentarios poco saludables y el desarrollo y la progresión de la MASLD. Por ello, se han explorado varias intervenciones nutricionales para el tratamiento de la MASLD, siendo la dieta mediterránea la más estudiada y recomendada. Otros enfoques dietéticos basados en plantas, incluyendo la dieta DASH (Dietary Approaches to Stop Hypertension) y la dieta vegetariana, también han demostrado beneficios potenciales8,9. Las estrategias óptimas de intervención dietética para la MASLD actualmente no se encuentran estandarizadas.
Considerando la evidencia existente, el enfoque de una dieta basada en patrones de alimentación saludable con alimentos mínimamente procesados o sin procesar, bajos en azúcar y grasas saturadas, y altos en polifenoles, ácidos grasos poliinsaturados omega-3 y ácidos grasos monoinsaturados, lleva a la conclusión de que, idealmente, la dieta mediterránea, u otros patrones dietéticos que se superponen, deberían servir de base y reestructurarse en diferentes tipos de dietas. El tipo exacto de dieta, en términos de composición de macronutrientes, elección de alimentos y horario de las comidas, puede adaptarse a las preferencias del paciente para aumentar la adherencia a largo plazo, siempre que se respeten estos principios4.
El plan de intervención nutricional debe corregir los problemas con la masa corporal magra que pueden aparecer en los sujetos de mayor edad. Feng et al.10 demostraron que los pacientes con sarcopenia (tanto jóvenes como de mediana edad) son más propensos a la MASLD (12.75%) que quienes no la presentan (3.73%). El abordaje actual de la MASLD enfatiza la exploración de la enfermedad junto con la comorbilidad del paciente, como hipertensión arterial, diabetes tipo 2 o síndrome metabólico, entre otras, y el plan higiénico-dietético debe ser adaptable y flexible a las diferentes situaciones y necesidades de cada paciente, considerando las diversas condiciones metabólicas que están implicadas. Por lo tanto, no existe una dieta mejor que otra, sino que se debe personalizar la intervención nutricional dependiendo de las carácteristicas de cada paciente.
Resultados clínicos relevantes
Es innegable que la dieta mediterránea se ha consolidado como el pilar fundamental en el manejo y la reversión de la MASLD, dado su impacto significativo sobre los parámetros hepáticos y clínicos. Este tipo de régimen dietético destaca por sus beneficios sostenidos a largo plazo. Jurek et al.1 demostraron, en un ensayo clínico controlado de 2 años realizado en pacientes con MASLD, que la mayor adherencia a la dieta mediterránea, combinada con la promoción de actividad física, condujo a mejoras significativas en la reducción del contenido de grasa intrahepática, el índice de hígado graso (FLI, fatty liver index) y los niveles plasmáticos de citoqueratina-18, además de lograr una disminución progresiva del índice inflamatorio dietético. Este estudio evidenció una mejora en las enzimas hepáticas, particularmente en la disminución sostenida de la aspartato aminotransferasa (AST), la alanina aminotransferasa (ALT) y la gamma-glutamil transferasa (GGT), indicadores clave de la función hepática y de daño celular, reflejando una recuperación hepatocelular y una reducción de la inflamación hepática1.
Los beneficios de la dieta mediterránea están mediados por su composición rica en grasas monoinsaturadas, polifenoles y ácidos grasos omega-3, considerándose como una dieta equilibrada, ya que sus elementos contribuyen a la modulación del estrés oxidativo y de la inflamación crónica, además de mejorar el metabolismo de los lípidos y de la glucosa. Yamazaki et al.11 realizaron un análisis de la diversidad y la viveza de colores de la dieta en los pacientes con MASLD en comparación con una dieta equilibrada, y demostraron que la menor variación en la cromaticidad y un cromatismo promedio inferior (indicando por dietas poco coloridas y menos variadas) se asocian con niveles elevados de ALT y fibrosis hepática. A partir de estas observaciones, se sugiere que los patrones de alimentación monótonos, con pocas variaciones, están asociados a una ingesta deficiente de nutrientes y de fibra dietética, y por ende con la progresión y la gravedad de la enfermedad hepática11.
Es importante destacar que las intervenciones basadas en la alimentación han logrado importantes reducciones en parámetros antropométricos como el peso corporal, el índice de masa corporal (IMC), la masa grasa y la circunferencia de la cintura, fundamentales en el control de la obesidad y sus complicaciones metabólicas1.
Otras estrategias dietéticas, incluyendo la alimentación restringida en el tiempo y las dietas bajas en calorías o con enfoques específicos, como la dieta DASH o la dieta vegetariana, también han mostrado efectos positivos sobre los parámetros metabólicos, aunque con evidencia menos robusta y con menor duración del seguimiento. No obstante, la sostenibilidad y el impacto a largo plazo parecen ser superiores con la dieta mediterránea, lo que la posiciona como la intervención nutricional de elección en la MASLD1,6.
En síntesis, la intervención dietética de estilo mediterráneo ha demostrado que, a largo plazo, logra mejoras clínicas relevantes en los pacientes con MASLD, evidenciadas por la reducción de la esteatosis hepática, la disminución de los marcadores bioquímicos hepáticos de inflamación y el control de la comorbilidad metabólica. La intervención dietética es una estrategia terapéutica no farmacológica que constituye un pilar fundamental en el manejo integral de la MASLD1,6.
Tipos de dieta en la esteatosis hepática metabólica
En esta revisión nos centramos en los modelos dietéticos con mayor evidencia, así como en modelos actualmente en estudio: la dieta mediterránea, las dietas mediterráneas modificadas, la dieta DASH, las dietas bajas en grasas, las dietas bajas en hidratos de carbono, la dieta cetogénica, la alimentación con restricción en el tiempo y las dietas basadas en plantas. En la figura 2 se muestran las características de las principales dietas más estudiadas en la MASLD.
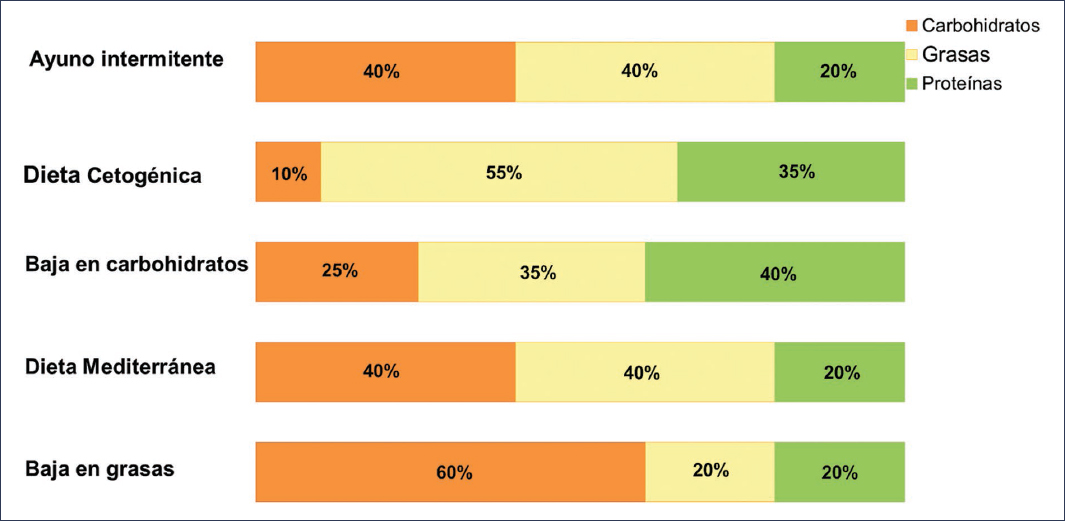
Figura 2. Distribución de los macronutrientes en los diferentes tipos de dieta para la MASLD. Los macronutrientes se presentan como porcentaje relativo de la energía total. Se recomienda que la distribución de macronutrientes en la dieta con restricción horaria se ajuste a la dieta mediterránea, aunque puede variar.
Dieta mediterránea y dietas mediterráneas modificadas
Las intervenciones dietéticas en el marco de la dieta mediterránea han demostrado una eficacia significativa en el manejo de la MASLD. Encontrándose entre los enfoques de mayor eficacia y más estudiados, se caracteriza por una ingesta más alta de lípidos que otros enfoques dietéticos, enfatizando los ácidos grasos insaturados y la ingesta regular de fibra, lo que contribuye a su capacidad para mejorar las condiciones clínicas relacionadas con la MASLD, el estado nutricional, la composición corporal y la inflamación, incluyendo una reducción significativa de la ALT; también tiene el potencial de bloquear o ralentizar la progresión de MASLD a etapas más graves1,3,12,13. Se destaca por un alto consumo de vegetales (frutas, verduras, panes y otros cereales mínimamente refinados, patatas, judías, frutos secos y semillas); alimentos mínimamente procesados, frescos de temporada y cultivados localmente; frutas frescas como postre típico, con dulces que contienen azúcares o miel algunas veces por semana; un elevado consumo de aceite de oliva (en especial aceite de oliva virgen y virgen extra) utilizado como principal fuente de grasa; una ingesta moderada de productos lácteos (principalmente queso y yogur); huevos, pescado y aves consumidos en cantidades bajas a moderadas; carnes rojas consumidas en bajas cantidades; y vino con moderación, consumido con las comidas1,14. Los estudios prospectivos observacionales respaldan una asociación inversa de la MASLD con la dieta mediterránea o los patrones dietéticos superpuestos. Los ensayos clínicos que prueban el efecto de las dietas mediterráneas clásicas o modificadas (bajas en hidratos de carbono o enriquecidas con polifenoles) respaldan su efecto beneficioso sobre la esteatosis hepática. Los dos ensayos clínicos aleatorizados más grandes y de mayor duración (18 meses) proporcionan la mejor evidencia del valioso papel de dos dietas mediterráneas modificadas. Gepner et al.15 demostraron la superioridad de la dieta mediterránea baja en hidratos de carbono sobre la dieta baja en grasas en cuanto a disminución de la grasa intrahepática. Yaskolka Meir et al.18 encontraron que la dieta mediterránea enriquecida con polifenoles y más estrictamente restringida en carne roja y procesada condujo a una pérdida de grasa hepática dos veces mayor que una dieta mediterránea regular isocalórica, a pesar de lograr una reducción de peso similar. En ambos estudios15,18 se demostró que la intervención nutricional es superior al asesoramiento nutricional estándar. El uso de dieta mediterránea, así como de sus versiones modificadas, dieta mediterránea baja en hidratos de carbono y dieta mediterránea baja en grasas, también ha resultado en reducciones significativas de las enzimas hepáticas, incluyendo ALT y AST, así como indice hepatico o fatty liver index (IHL) y fibrosis-4 index (FIB4)1,4,16–18.
Dietas bajas en hidratos de carbono
Las dietas bajas en hidratos de carbono también reducen eficazmente la esteatosis hepática y mejoran la resistencia a la insulina. Además, se están explorando estrategias dietéticas emergentes, como el ayuno intermitente y la terapia cetogénica de muy baja energía por su potencial para la reducción de peso y de masa grasa, y de la resistencia a la insulina, mejorando la salud metabólica, enfatizando su efectividad en la mejora de los resultados hepáticos asociados con la MASLD, así como en la reducción del estado inflamatorio3.
Las dietas bajas en hidratos de carbono se pueden clasificar en tres categorías según la ingesta. Una dieta moderada o reducida en hidratos de carbono podría definirse como una ingesta de hidratos de carbono del 26% al 45% de la ingesta total de calorías por día, o > 130 g/día (y menor que aproximadamente 250 g/día en una dieta de 2000 calorías, por ejemplo). Cuando la ingesta de hidratos de carbono es < 26 %, o > 30 g/día, se clasifica como una dieta baja en hidratos de carbono. Un paso más adelante, cuando la ingesta de hidratos de carbono es < 10 %, o < 30 g/día, se puede categorizar como dieta cetogénica o muy baja en hidratos de carbono. A medida que disminuye la proporción de la ingesta de hidratos de carbono, aumenta la proporción de grasa y proteína, por lo que las dietas llamadas «altas en proteínas» o «altas en grasa» generalmente son dietas reducidas o bajas en hidratos de carbono. En general, a pesar de la superioridad a corto plazo de la dieta baja en hidratos de carbono, a largo plazo ambas parecen ser igualmente efectivas en la reducción de la grasa hepática y la ALT siempre que se logre una pérdida de peso del 7%19.
La intervención dietética, especialmente el aumento de las proteínas en la dieta junto con el control del peso corporal general, ha demostrado ser una estrategia prometedora para disminuir el impacto de la MASLD. Se ha demostrado que las proteínas en la dieta reducen la acumulación de grasa en el hígado al aumentar el metabolismo hepático, generar saciedad, incrementar la sensibilidad a la insulina y mejorar la retención de masa muscular, lo que en conjunto contribuye al control del peso. Tanto las proteínas animales como las vegetales tienen beneficios; sin embargo, las proteínas vegetales (principalmente de legumbres, frutos secos y semillas) han demostrado mayores ventajas metabólicas, lo cual destaca la importancia de obtener suficiente proteína de fuentes de alimentos fácilmente disponibles y sostenibles. Además, se ha demostrado que las dietas ricas en proteínas, como la dieta mediterránea, retrasan la probabilidad y el avance de la MASLD20,21.
Dietas bajas en grasas
Una dieta baja en grasas restringe la cantidad de energía obtenida de fuentes de grasa. Típicamente, una dieta baja en grasas limita la energía de la grasa a no más del 30% de las calorías diarias totales22. Las dietas bajas en grasas o bajas en hidratos de carbono ofrecen estrategias alternativas, con evidencia que sugiere que reducir la ingesta de hidratos de carbono puede reducir la acumulación de lípidos intrahepáticos, la trigliceridemia, la oxidación de lípidos y la resistencia a la insulina1. Una revisión sistemática llevada a cabo por Jurek et al.1 encontró un ensayo clínico realizado en pacientes con MASLD, en los que el contenido hepático de triglicéridos disminuyó un 25% después de 12 semanas de dieta baja en grasas (p < 0.01), independientemente de la pérdida de peso corporal y de la ingesta calórica. En otro metaanalisis realizado por Ahn et al.19, en un estudio de pérdida de peso de 18 meses con 139 participantes con obesidad abdominal o dislipidemia, que comparó una dieta baja en grasas frente a una dieta mediterránea o baja en hidratos de carbono, halló que una dieta baja en grasas resultó en una reducción del contenido de grasa hepática del 3.8% (p < 0.001). En este estudio, los autores demostraron que las disminuciones en la proporción del contenido de grasa hepática parecen actuar como un mediador más fuerte de los efectos favorables de la dieta baja en grasas sobre algunos marcadores cardiometabólicos que la reducción general de la grasa visceral. Es importante destacar que en uno de los anteriores estudios la reducción del contenido de grasa hepática fue mayor en el grupo de dieta mediterránea o baja en hidratos de carbono (p < 0.05). A pesar de los hallazgos, los estudios más recientes sugieren que una dieta baja en hidratos de carbono podría ser más adecuada que una dieta baja en grasas para el tratamiento1,19.
Dieta cetogénica o muy baja en hidratos de carbono
El patrón de la dieta cetogénica muy baja en hidratos de carbono se caracteriza por restringir la ingesta de carbohidratos a < 30-50 g diarios (equivalente al 13-25% de las calorías totales). Esta dieta tiene un alto contenido de grasas, lo cual representa entre el 60 y el 70% de las calorías totales, y cantidad de proteínas que oscila entre 0.8 y 1.2 g por kg de peso corporal ideal. Por otro lado, la dieta cetogénica muy baja en hidratos de carbono y en calorías se define por un contenido de carbohidratos < 50 g diarios, ingesta de proteína de 1-1.5 g por kg de peso corporal ideal, y cantidad de grasa de 15-30 g al día, con una ingesta calórica total aproximada de 500-800 calorías diarias. Es una dieta altamente restrictiva y las pautas establecen que debe estar bajo la supervisión de un profesional de la salud y limitarse a 8 a 12 semanas, seguida de un aumento gradual de las calorías, los hidratos de carbono y la variedad de alimentos. Algunos estudios han investigado la eficacia de la dieta cetogénica muy baja en hidratos de carbono en pacientes con sobrepeso y obesidad, pero la evidencia a largo plazo y de alta calidad es limitada. Esta dieta fue una estrategia efectiva en algunos estudios en términos de pérdida de peso, reducción de la grasa visceral y mejora de los parámetros metabólicos y de los marcadores inflamatorios; sin embargo, no se han obtenido resultados concluyentes en ensayos clínicos aleatorizados de largo plazo sobre su efecto en la MASLD4.
En el metaanálisis realizado por Ahn et al.19 se encontró que ni la dieta baja en hidratos de carbono ni la dieta muy baja en hidratos de carbono son mejores para mejorar la esteatosis hepática o los niveles de transaminasas en comparación con una dieta baja en grasas. Además, existe evidencia de que, más allá de la distribución de los macronutrientes en la dieta, se puede considerar el tipo de calorías. Con respecto a los hidratos de carbono, el índice glucémico, relacionado con la respuesta glucémica posprandial, puede ser una herramienta útil en el manejo. En este contexto, en los estudios realizados por Ramon-Krauel et al.23 y por Parker A et al.24 se incorporó una dieta de bajo índice glucémico en las intervenciones nutricionales y tuvo un efecto positivo en la composición de la grasa hepática. Además de promover la reducción de peso, Kirk et al.26 observaron que estas dietas también pueden tener efectos positivos en la enfermedad hepática al reducir los niveles de insulina, la lipogénesis y la oxidación de ácidos grasos19,23–27.
Dieta DASH
La dieta DASH se ha utilizado como un enfoque de estilo de vida para tratar y prevenir la hipertensión. Consiste en una dieta baja en grasas saturadas, alta en proteínas, fibra y minerales, y baja en sodio. El plan de alimentación DASH se basa en frutas, verduras, productos lácteos bajos en grasa, pescado, cereales integrales, aves, nueces, semillas y legumbres, al tiempo que reduce el consumo de grasa, carne roja y productos con azúcar añadido. La dieta DASH ha demostrado disminuir la mortalidad por todas las causas, enfermedad cardiovascular, diabetes y cáncer; por ello, este enfoque dietético ha demostrado ser prometedor para mejorar los parámetros metabólicos y hepáticos1,25.
Hekmatdoost et al.28 hallaron una relación inversa entre la adherencia a la dieta DASH y el riesgo de MASLD; los sujetos en el cuartil más alto de la escala de la dieta DASH tuvieron una reducción del 30% en el riesgo (odds ratio [OR]: 0.70; intervalo de confianza del 95% [IC 95%]: 0.61-0.80). En consonancia con estos resultados, en una revisión realizada por Torres et al.25 se encontrón un estudio a largo plazo que evaluó una gran cohorte y después de dos décadas de seguimiento mostró que estar en el tercil más alto de adherencia a la dieta DASH se asoció con un menor riesgo (OR: 0.57-0.77). La evidencia de algunos estudios observacionales y de un ensayo clínico23,28 respalda que los patrones dietéticos DASH podrían ser una herramienta preventiva; sin embargo, se necesitan más ensayos clínicos para evaluar con mayor profundidad los hallazgos de una población heterogénea de estudios observacionales23,28.
Alimentación con restricción del tiempo
La alimentación restringida en el tiempo, también llamada «ayuno intermitente», es una estrategia nutricional en la cual las calorías se consumen en una ventana de tiempo definida, e implica varias formas de restricción de tiempo4. El término «ayuno intermitente» se utiliza para describir diversos métodos de restricción energética, que van desde la alternancia de periodos de alimentación y ayuno hasta la abstinencia total de alimentos o el consumo de muy baja energía23.
El ayuno en días alternos consiste en consumir alimentos de forma normal durante 24 horas y ayunar durante las siguientes 24 horas. El ayuno 5:2 consiste en reducir drásticamente la ingesta calórica durante 2 días (aproximadamente a 500 calorías al día), seguido de 5 días de consumo normal. Por otro lado, el ayuno periódico consiste en un ayuno intermitente de más de 2 días con una ingesta calórica mínima (≤ 500 calorías) sin ayunos repetidos. El ayuno con restricción de tiempo consiste en comer solo durante ciertas horas del día (p. ej., de 12 p. m. a 8 p. m.). Se plantea la hipótesis de que el ayuno intermitente puede tener beneficios metabólicos en el hígado, independientemente de la restricción calórica y la pérdida de peso; esto también puede mejorar la histología de la MASLD16.
En dietas como el ayuno intermitente, los pacientes pueden tener la impresión de que durante la hora de comer, también llamada «hora (o día) de fiesta», pueden comer lo que quieran, independientemente de si es saludable o no. Esto puede llevar a un consumo excesivo de azúcares, grasas saturadas y alimentos ultraprocesados. Además, puede haber un exceso de grasas saturadas y carne, especialmente carne roja y procesada, en las dietas bajas en hidratos de carbono y cetogénicas. Como mínimo, se deben preferir el pescado y las aves sin procesar o muy poco procesados4.
La alimentación restringida en el tiempo limita el periodo diario de ingesta de alimentos a 8-10 h la mayoría de los días de la semana. Esta estrategia nutricional cambia la proporción diaria entre los periodos de alimentación y ayuno sin reducir necesariamente la ingesta calórica diaria total. Sin embargo, en algunos estudios (dos ensayos controlados aleatorizados y un ensayo de un solo grupo) se observó una reducción involuntaria de la ingesta de energía de 250 a 600 calorías. El ayuno periódico mostró reducir la esteatosis hepatica en 697 participantes en un estudio observacional prospectivo de sujetos con y sin diabetes tipo 24,16. Johari et al.31 demostraron que con una intervención de restricción calórica en días alternos durante 8 semanas (día de ayuno, 30% del requerimiento calórico; día sin ayuno, ad libitum), en comparación con una dieta habitual normal (sin intervención) como control, tanto las puntuaciones de esteatosis hepática como de fibrosis se redujeron significativamente en la masa corporal ajustada para la edad (MACR) en comparación con los controles (ambas p < 0.01). Un ensayo controlado aleatorizado realizado por Holmer et al.30 en pacientes con MASLD comparó tres intervenciones durante 12 semanas. La alimentación restringida en el tiempo fue en forma de una dieta 5:2, en la que 2 días no consecutivos por semana los participantes consumieron 500 kcal/día las mujeres y 600 kcal/día los hombres, y mantuvieron una dieta generalmente saludable en los 5 días restantes de la semana. La alimentación restringida en el tiempo fue superior a las instrucciones dietéticas estándar para reducir el peso y la esteatosis, pero fue igualmente eficaz que una dieta regular baja en hidratos de carbono y alta en grasas4,29–31.
El ayuno intermitente incluye diferentes métodos de restricción energética: ayuno restringido en el tiempo, ayuno en días alternos y ayuno prolongado. El régimen de alimentación diaria restringida en el tiempo, con un periodo de ayuno de 18 h y una ventana de alimentación de 6 h (16/8), y el ayuno en días alternos, caracterizado por 24 h de ayuno al 25% de la energía basal, han ganado recientemente atención como posibles intervenciones para mejorar el manejo de las condiciones metabólicas. Aunque podrian ser beneficiosos, aún no se conoce cuál es el mejor método de ayuno intermitente para los sujetos con MASLD1,4. El uso de alimentación restringida en el tiempo, incluido el protocolo 16/8, ha reportado mejoras en la función hepática, demostrando una reducción de las enzimas hepáticas (AST y ALT)23. Se necesita mayor evidencia, con resultados y conclusiones de estudios a largo plazo, para confirmar el impacto beneficioso de las variaciones del ayuno intermitente en la aparición y la evolución de la MASLD.
Dietas basadas en plantas
Las dietas basadas en plantas se centran en una alta ingesta de alimentos vegetales y derivados (es decir, cereales, legumbres, verduras y frutas), y una baja ingesta de alimentos de origen animal. La dieta vegetariana se solapa parcialmente con la dieta basada en plantas, mientras que la dieta vegana se caracteriza por la abstinencia total de productos animales. Las dietas basadas en plantas ofrecen el beneficio de prevenir enfermedades crónicas, pero su efecto sobre la MASLD no se ha demostrado en ensayos clínicos aleatorizados a largo plazo13.
A pesar del creciente interés por la nutrición vegetal en la atención clínica, que destaca los beneficios para la salud, y las estrategias de las dietas vegetales, falta evidencia que vincule estas dietas con la salud hepática, pues aún es limitada la investigación centrada en la relación entre la calidad de la dieta vegetal y las complicaciones hepáticas, como la esteatosis y la fibrosis. En un amplio estudio transversal, la adherencia a dietas basadas en plantas, especialmente aquellas que priorizan alimentos vegetales saludables, se asoció con una menor probabilidad de fibrosis hepática, además de encontrar que el alto consumo de fructosa en las dietas basadas en plantas se asoció con un mayor riesgo de esteatosis hepática. No obstante, pocos estudios han destacado la relación entre las dietas basadas en plantas y la esteatosis hepática, con resultados controvertidos13,32,33.
Es importante diferenciar entre las fuentes de fructosa. Las frutas enteras, ricas en fibra y polifenoles, podrían tener efectos protectores, mientras que las fuentes refinadas o concentradas podrían promover la acumulación de grasa hepática34. La dieta vegetariana, en particular, ha ganado atención debido a su potencial para reducir la grasa hepática, disminuir la inflamación sistémica y mejorar la sensibilidad a la insulina. Sin embargo, a pesar del creciente interés, la evidencia de su impacto en la MASLD sigue siendo limitada. Aun considerando estos beneficios potenciales, el uso de dietas basadas en plantas debe abordarse con precaución, en particular en personas con resistencia a la insulina, ya que las ingestas altas de hidratos de carbono de ciertas fuentes vegetales pueden conducir a una acumulación de grasa hepática. No se pueden extraer conclusiones firmes sobre los méritos relativos de las dietas vegetarianas frente a las mediterráneas en términos de resultados en pacientes con MASLD. La composición óptima de macronutrientes (hidratos de carbono, grasas, proteínas) para el manejo de la MASLD sigue sin estar clara, en particular al comparar la dieta baja en hidratos de carbono y la dieta baja en grasas. Si bien la dieta mediterránea está bien estudiada en la MASLD, la efectividad y la adherencia a largo plazo de otros patrones dietéticos, como la dieta DASH, requieren mayor exploración, también en comparación con la mediterránea. Además, la mayoría de los estudios se han realizado durante unos pocos meses, lo que crea una brecha en el conocimiento respecto a los efectos a largo plazo de modelos dietéticos específicos en la MASLD16.
Dietas orientadas en el contexto mexicano
Algunas organizaciones internacionales de salud están promoviendo dietas tradicionales para combatir el aumento de las enfermedades no transmisibles y de las tasas de obesidad en todo el mundo. Las dietas tradicionales generalmente son dietas saludables porque su núcleo son alimentos de origen vegetal, como granos, legumbres, vegetales, frutas y tubérculos, con un bajo consumo de alimentos de origen animal35,36.
En un esfuerzo por definir la dieta tradicional mexicana, Valerino-Perea et al.35 realizaron una revisión sistemática de 61 documentos científicos y encontraron que los grupos de alimentos representativos y sus componentes son los siguientes: 1) granos y tubérculos, como maíz, amaranto, arroz, trigo, yuca, papa y camote; 2) productos de maíz, como tortilla, tamales y atole; 3) legumbres, principalmente frijoles; 4) verduras como calabaza, chayote, nopales, maguey, jitomate, tomatillo y quelites; 5) frutas como anona, capulín, guayaba, jícama, mamey, ciruelas, tuna y zapote; 6) carnes de pavo, pollo, pato, venado, conejo y res; 7) hierbas y condimentos, como chile, epazote, vainilla, sal y cebolla; 8) aceites y grasas de aguacate, semilla de calabaza y semillas de chía; 9) bebidas de chocolate y pulque (bebida fermentada de maguey); 10) insectos, como chapulines, gusanos de maguey, hormigas y sus larvas, chicatanas y escamoles; y 11) dulces y edulcorantes, como la miel, el azúcar y la caña de azúcar. Es importante señalar que algunos de los alimentos citados no son de origen mexicano, sino que fueron adoptados de otros países e incluso de otros continentes35.
Dieta regionalizada
En un ensayo clínico aleatorizado realizado por Cano et al.37 en pacientes con MASLD se seleccionó a aquellos con esteatosis demostrada ecográficamente de moderada a grave, de 18 a 70 años de edad, de nacionalidad mexicana y sin signos de alarma. Los participantes se dividieron equitativamente en dos grupos: dieta mediterránea y dieta regional mexicana. Se encontró que la dieta mediterránea y la dieta regional mexicana son igualmente eficaces para mejorar los síntomas de la enfermedad hepática, en particular la esteatosis hepática, lo que destaca la viabilidad de utilizar dietas adaptadas regionalmente para el tratamiento del hígado graso37. La dieta regional mexicana se caracterizó por verduras silvestres, como quelites, flores comestibles, frutas locales, cereales integrales (derivados de maíz, amaranto), tubérculos (camote), frijoles, aceites y grasas saludables, cacahuate, chía, girasol, calabaza, aguacate y mayor consumo de carnes blancas.
Dieta milpa
La milpa es un sistema de producción agrícola tradicional en Mesoamérica, particularmente en México, que se ha utilizado desde la época prehispánica. La dieta milpa, rica en proteínas, fibra, vitaminas y compuestos bioactivos, se alinea con las recomendaciones para la MASLD. Proporciona una mayor diversidad dietética y contribuye a una producción sostenible. Una de sus limitaciones es que la disponibilidad de los alimentos descritos varía según la región de Mesoamérica; la mayoría de ellos se encuentran disponibles en las regiones centrales de América, como México. Sin embargo, existe poca información sobre este tema y la mayoría de los datos encontrados están relacionados con componentes individuales y no con el patrón dietético general, como es el caso de la dieta mediterránea, que cuenta con sólida evidencia38 (Tabla 1).
Tabla 1. Intervenciones dietéticas y mejores resultados metabólicos
| Comparación modelos dietéticos en MASLD | Caracteristicas del estudio | AST | ALT | GGT | CAP | LSM | FLI | Fib4 | Estadificación patología hepática | Referencia |
|---|---|---|---|---|---|---|---|---|---|---|
| MED vs. LFD | 27 participantes hombres con sobrepeso/obesidad Diagnóstico: ecografía Edad 27-42 años Aleatorización 1:1 14 MED vs 13 LFD Duración: 12 Semanas |
p = 0.017 | p = 0.128 | p = 0.224 | NA | NA | p = 0.021 | NA | NA | Ristic-Medic et al.45 (2020) |
| TMD vs. LCMD vs. LFMD | 63 participantes con resistencia a la insulina y obesidad Diagnóstico: ecografía Edad 18-65 años Duración: 12 semanas Muestreo aleatorio simple Grupo 1 TMD: 40-45% HC, 15-20% P, 35-40%L Grupo 2 LCMD: ≤ 35% HC, 15-20% P, > 45% L Grupo 3 LFMD: ≥ 55% HC, 15-20% P, 20-25% L |
p = 0.010 | p = 0.410 | p = 0.010 | NA | NA | p = 0.003 | p = 0.020 | NA | Kestane y Bas46 (2024) |
| TRF 16/8 vs. CN | 45 participantes Grupo TRF: 22 Grupo CN: 23 Edad: 18-50 años Esteatosis hepática grado 2 (CAP) Ensayo controlado aleatorizado Duración: 12 semanas |
p = 0.010 | p = 0.013 | p = 0.026 | p = 0.009 | p < 0.001 | NA | NA | NA | Kord-Varkaneh et al.47 (2023) |
| DASH vs. LCD | 40 participantes con obesidad Grupo dieta DASH: 20 Grupo control: 20 RCT doble ciego Duración: 8 semanas |
p = 0.008 | p = 0.149 | NA | NA | NA | NA | NA | NA | Rooholahzadegan et al.48 (2023) |
| CR vs. ND | 60 participantes Ensayo clínico aleatorizado controlado Edad: 20-60 años Diagnóstico: ecografía Grupo CR: 20 Grupo control: 30 Duración: 12 semanas La dietas contenían 17% P, 30% L y 53% HC |
p = 0.020 | p = 0.010 | NA | NA | NA | NA | NA | p = 0.350 | Asghari et al.49 (2022) |
| LOV-D vs. SWL-D | 75 participantes con sobrepeso u obesidad Ensayo clínico aleatorizado Duración: 12 semanas |
p = 0.08 | p = 0.04 | NA | NA | NA | NA | NA | NA | Garousi et al.50 (2023) |
ALT: alanina aminotransferasa; AST: aspartato aminotransferasa; CAP: Parámetro de atenuación controlado; CN: dieta normal de control; CR: dieta restringida en calorías; DASH: Enfoques Dietéticos para Detener la Hipertensión; FLI: Fatty Liver Index; GGT: gamma-glutamil transferasa; HC: hidratos de carbono; L: lípidos; LCD: dieta baja en calorías; LCMD: dieta mediterránea baja en hidratos de carbono; LFD: dieta baja en grasas; LFMD: dieta mediterránea baja en grasas; LOV-D: dieta ovolactovegetariana; MASLD: Esteatosis hepática metabólica; MED: dieta mediterránea; ND: dieta normal; P: proteínas; SLM: Modificación Estándar del Estilo de Vida; SWL-D: dieta estándar para pérdida de peso; TMD: Dieta de Comidas Terapéuticas; TRF: alimentación restringida en el tiempo 16/8.
Educación, prevención y empoderamiento del paciente
Las pautas recomiendan implementar el tratamiento médico-nutricional a través de programas integrales de educación nutricional destinados a promover el autocuidado39.
Enfoques para la modificación del estilo de vida
Los enfoques de modificación del estilo de vida utilizan diversos contenidos de intervención, como evaluación de los comportamientos de estilo de vida de los participantes, información, educación, establecimiento de objetivos, asesoramiento y retroalimentación40,41. La educación sobre la modificación del estilo de vida en los pacientes con MASLD puede impartirse de diversas maneras; algunas son más tradicionales, como una consulta individual con un profesional de la salud. Desde un punto de vista práctico, el asesoramiento dietético personalizado y la educación alimentaria del paciente son esenciales para garantizar la adherencia a largo plazo a un patrón de alimentación saludable. Otras formas de educación implican enfoques más modernos, como programas web o el uso de aplicaciones para teléfonos inteligentes. Independientemente del método, es importante lograr los objetivos de pérdida de peso mejorando la calidad de la dieta y aumentando la actividad física. Diversos métodos y sus combinaciones pueden ser útiles en este caso20.
Tecnologías móviles para la MASLD
Varios estudios han demostrado la importancia del uso de tecnologías móviles para modificar el estilo de vida de los pacientes con MASLD. En un ensayo controlado aleatorizado42 se encontró que el uso de una aplicación móvil especial en el grupo de intervención demostró una probabilidad significativamente mayor de lograr una pérdida de peso ≥ 5% a los 6 meses, con un riesgo relativo de 5.2 (IC 95%: 1.8-15.4; p = 0.003). Se produjeron mejoras en los índices antropométricos, como la circunferencia de la cintura y el peso corporal, junto con reducciones en los niveles de enzimas hepáticas. Los pacientes con MASLD pueden carecer de motivación o adherencia al control de la enfermedad; las intervenciones que utilizan eSalud con diversos contenidos motivarían su comportamiento y, en última instancia, mejorarían el control sostenible20,40,42.
Un estudio realizado en Tailandia demostró que brindar información sobre estilos de vida saludables y educación sobre MASLD a través de una aplicación de redes sociales mejora significativamente la rigidez del hígado en los pacientes con MASLD en comparación con el estándar de atención, lo que destaca el potencial de las plataformas de redes sociales para mejorar los resultados clínicos en el manejo de la MASLD43.
Con más de un 25% de los pacientes que buscan asesoramiento dietético a través de plataformas como YouTube, la calidad y la fiabilidad de la información son fundamentales. Sin embargo, la disparidad en el valor educativo y las métricas de participación entre el contenido profesional y el no profesional sigue sin explorarse. En un estudio realizado por Tur44 se subraya el doble reto de garantizar información sanitaria de alta calidad y, al mismo tiempo, maximizar la interacción en plataformas digitales. Los hallazgos señalan la necesidad de colaboración entre profesionales sanitarios y creadores de contenido para proveer conocimiento científicamente riguroso y, al mismo tiempo, accesible. Mediante la adopción de técnicas narrativas y una mayor supervisión regulatoria, se puede mejorar la calidad y la accesibilidad de la guía dietética en línea, lo que en última instancia favorece unos mejores resultados de salud en los pacientes con MASLD44.
Conclusiones
La intervención nutricional es fundamental en el manejo de la MASLD, siendo crucial una pérdida de peso del 7-10% para mejorar la esteatosis y revertir la fibrosis en etapas tempranas. La dieta mediterránea es actualmente el patrón dietético con mayor evidencia; destaca por su abundancia en grasas monoinsaturadas, polifenoles y omega-3, que logran modular la inflamación y mejoran el metabolismo hepático. No obstante, la heterogeneidad clínica y la comorbilidad asociada en los pacientes con MASLD exigen un enfoque nutricional individualizado, adaptado a las características genéticas, metabólicas y culturales de cada paciente para asegurar la adherencia a largo plazo. Otras estrategias, como las dietas bajas en hidratos de carbono, la dieta DASH, las dietas vegetarianas y el ayuno intermitente, también muestran beneficios, pero con menor evidencia. Debemos considerar que las dietas regionalizadas, como la dieta tradicional mexicana y la dieta milpa, ofrecen alternativas viables adaptadas al contexto cultural. Finalmente, la educación nutricional y el uso de tecnologías móviles son herramientas clave para mejorar la adherencia y los resultados clínicos en los pacientes con MASLD.
Financiamiento
Los autores declaran no haber recibido financiamiento para este estudio.
Conflicto de intereses
A.D. Cano-Contreras es conferenciante de Medix. M.R. Francisco declara no tener conflicto de intereses para la realización del presente trabajo de investigación.
Consideraciones éticas
Protección de personas y animales. Las autoras declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki. Los procedimientos fueron autorizados por el Comité de Ética de la institución.
Confidencialidad, consentimiento informado y aprobación ética. Las autoras han seguido los protocolos de confidencialidad de su institución y cuentan con la aprobación del Comité de Ética. Se han seguido las recomendaciones de las guías SAGER, según la naturaleza del estudio.
Declaración sobre el uso de inteligencia artificial. Las autoras declaran que no utilizaron ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.