Introducción
La esteatosis hepática representa una acumulación excesiva de grasa en el hígado, cuya etiología incluye enfermedad metabólica, relacionada con el alcohol, inducida por fármacos y criptogénica1.
La esteatosis hepática asociada a disfunción metabólica (MASLD Metabolic dysfunction Associated Steatotic Liver Disease), anteriormente conocida como enfermedad del hígado graso no alcohólico (NAFLD, Non-Alcoholic Fatty Liver Disease) es la causa más común de enfermedad hepática. La MASLD es una enfermedad que está incrementando en todo el mundo; actualmente se reporta alrededor de un 38% de pacientes adultos con MASLD y un 7-14% de niños y adolescentes, por lo que plantea un problema importante de salud pública. Para el año 2040 se proyecta que la prevalencia de la MASLD sea de hasta el 55% en los adultos, acompañada del incremento de las tasas de obesidad y de diabetes1–3.
Aunque la MASLD no siempre evoluciona a una enfermedad hepática crónica, es la principal indicación de trasplante en los Estados Unidos de América, en mujeres y con hepatocarcinoma. La enfermedad cardiovascular (ECV) es la principal causa de mortalidad en los pacientes con MASLD2.
La MASLD incluye una amplia gama de patologías, que van desde la acumulación de grasa únicamente (esteatosis aislada) hasta la acumulación de grasa con inflamación asociada y daño de las células hepáticas (balonización de los hepatocitos), denominada colectivamente esteatohepatitis asociada a disfunción metabólica (MASH, Metabolic dysfunction Associated Steato Hepatitis), anteriormente conocida como esteatohepatitis no alcohólica (NASH, Non-Alcoholic Steatohepatitis), y grados crecientes de fibrosis (F0-F4) hasta cirrosis. Las etapas de empeoramiento de la enfermedad, desde la esteatosis aislada hasta la MASH con fibrosis, o la cirrosis, se asocian con un riesgo progresivamente mayor de resultados clínicos adversos4.
La progresión de la enfermedad de esteatosis a MASH, fibrosis y hepatocarcinoma es heterogénea y ocurre en varios años o décadas, influenciada por algunos factores no modificables (edad, sexo, raza o etnia, herencia) y otros modificables (dieta, estilo de vida, fármacos)5.
Siendo la MASLD la manifestación hepática del síndrome metabólico, esta es parte de una enfermedad compleja multiorgánica, con una relación bidireccional que incluye la superposición de los factores de riesgo. Respecto a los factores genéticos de la MASLD y la ECV, se han reportado diferentes variantes genéticas asociadas, como TM6SF2E16K y PNPLA3I148M6.
En el estudio NHANES III (National Health and Nutrition Survey) de 2017 a 2020 se reportó una prevalencia del 35.5% y la principal comorbilidad fue la obesidad, con un 89.1%, seguida de la prediabetes en el 66.6 %, la hipertensión en el 50.1%, la hipertrigliceridemia en el 51.3% y los niveles bajos de colesterol unido a lipoproteínas de alta densidad en el 54.7 %; el 65% presentaban tres o más enfermedades en comorbilidad7.
Diabetes
En los pacientes diabéticos, la prevalencia de MASLD en todo el mundo es de hasta el 65%, frente al 38% en la población global3.
Se ha observado una asociación bidireccional entre la diabetes tipo 2 y la MASLD, lo cual incrementa hasta dos veces la incidencia de MASLD en los pacientes diabéticos2,8.
Se ha descrito un aumento en la prevalencia de MASLD en los pacientes con diabetes, desde el 13% en 1990-2004 hasta el 68.8% en 2016-20212. Las prevalencias más altas fueron en Europa Occidental (80.6%) y Oriente Medio (71.2%), y las más bajas en África (53.1%)2.
Las guías de práctica clínica recomiendan realizar el cribado mediante la medición del índice de fibrosis basado en 4 factores (FIB-4), con la finalidad de detectar pacientes con alto riesgo de desarrollar fibrosis y complicaciones relacionadas con el hígado en caso de tener factores de riesgo cardiometabólico; si este es > 1.3, se sugiere realizar una elastografía transitoria controlada por vibración3,8.
En los pacientes con mayor riesgo, como los diabéticos, se ha observado que el punto de corte del FIB-4 de 1.3 permite clasificar a aquellos con riesgo aumentado de complicaciones hepáticas y mortalidad en un plazo de 5 años, considerando que el FIB-4 es un sistema de bajo costo y con un valor predictivo negativo aceptable, pero con una sensibilidad y un valor predictivo positivo moderados. Incluso en la guía de la American Diabetes Association de 2025 se menciona que los pacientes con diabetes y FIB-4 entre 1 y 1.3 pueden tener fibrosis avanzada, especialmente si presentan obesidad y otros factores cardiometabólicos8.
En pacientes con biopsia con diagnóstico de NASH/MASH, la prevalencia global fue del 66.4%, de los cuales el 40.8% presentaban fibrosis significativa y el 15.5% avanzada2.
En los pacientes con MASLD se ha observado un exceso de resistencia a la insulina (RI) del tejido adiposo, asociada a un perfil lipídico enriquecido en lípidos saturados, mayor actividad de los macrófagos y más gravedad de la fibrosis hepática, aumentando la síntesis de lípidos de novo, que también se ve favorecida por el metabolismo de los ácidos grasos libres provenientes de la dieta; el aumento de la síntesis de lípidos de novo también se observa en diversas enfermedades metabólicas9.
La acumulación excesiva de lípidos no solo es por el exceso de ácidos grasos libres, sino también por una inadecuada oxidación de estos, probablemente por disfunción mitocondrial o por una menor flexibilidad metabólica (capacidad para adaptarse a las fluctuaciones en la demanda y el suministro de energía para mantener la homeostasis del cuerpo)9.
Este efecto bidireccional en los pacientes con diabetes y aumento del índice de masa corporal IMC se asocia a la reducción en la flexibilidad metabólica, lo que aumenta la oxidación de los ácidos grasos libres. En fases tempranas de la MASLD hay una disminución de la lipólisis por un aumento de la insulina, acompañado de un incremento en la oxidación de los ácidos grasos y en la actividad mitocondrial, así como un aumento en la biogénesis. Sin embargo, en estadios tardíos, la respiración mitocondrial se ve reducida por las anomalías del DNA y de las proteínas9.
Este círculo vicioso entre la MASLD y la RI de los tejidos es clave en la fisiopatología, ya que las consecuencias metabólicas de la RI son hiperglucemia, dislipidemia y aumento en la adiposidad visceral, así como aumento de la grasa abdominal. La RI disminuye la captación de la glucosa, liberación de ácidos grasos libres y suprime el suministro de ácidos grasos no esterificados al hígado durante el período posprandial, lo que empeora la infiltración de grasa en el hígado, especialmente por lípidos tóxicos como las ceramidas. Esta acumulación de grasa hepática causa estrés oxidativo, induciendo estrés del retículo endoplásmico, alterando la activación mitocondrial, con disfunción lisosomal, activación del inflamasoma, liberación de citocinas y peroxidación lipídica, causando daño hepático o la muerte10–12.
Por otro lado, se han reportado cambios en la expresión génica relacionados con la MASLD y la diabetes, con menor expresión de los genes FYN, HNRNPU y FUBP1. La cinasa de fyn regula la permeabilidad epitelial intestinal, y al estar comprometida la barrera intestinal, permite el paso de más endotoxinas bacterianas, las cuales incrementan la inflamación hepática y el desarrollo de esteatohepatitis. La proteína HNRNPU desempeña un papel importante en la unión con el RNA, en la regulación de genes de la transcripción, organización de la cromatina y respuesta de las células al daño del DNA. Esta proteína, junto con las ribonucleoproteínas nucleares (hnRNP), modulan la expresión de genes relacionados con la regulación de la insulina, el estrés oxidativo y la función renal, los cuales son de gran relevancia en el contexto de la diabetes. Por tanto, estas proteínas tienen un efecto protector en el desarrollo de las complicaciones asociadas a la diabetes, incluyendo la hipertensión y la lesión renal. En el tejido hepático se han observado cambios en la expresión de las hnRNP en pacientes con NAFLD.
Respecto al gen FUBP1, que codifica el elemento de unión a la proteína 1 río arriba (FUB1), este regula la expresión del oncogén c-Myc, por lo que desempeña un papel importante en diversos procesos celulares, incluidas la proliferación, la apoptosis y la diferenciación. Además, esta proteína regula la expresión de los genes de la hexocinasa (HK1 y HK2), que regulan las vías de la glucólisis, la cual es esencial en el metabolismo de la glucosa. La disfunción de estas vías se asocia directamente a RI y a alteraciones de la homeostasis de la glucosa. Además, la regulación del oncogén c-Myc mediante la proteína FUBP1 es importante en las enfermedades hepáticas, ya que promueve el desarrollo de células tumorales hepáticas y su sobrevida13.
Hipertensión arterial
Se ha reportado que hasta un 50% de los pacientes con NAFLD o MASLD presentan hipertensión arterial sistémica (HAS); además, los pacientes con HAS y NAFLD tienen niveles de presión más elevados (hasta un 20%), la HAS es un factor independiente de NAFLD y los pacientes con NAFLD tienen mayor riesgo de incidencia de HAS7,14.
En una cohorte en China se observó que la MASLD se asocia a mayores niveles de presión arterial, y que el efecto de la HAS sobre la MASLD es menor.
En la cohorte de NHANES III, con un seguimiento de 22.3 años, se observó una mortalidad de 19.5 por cada 1000 personas por año. En los pacientes con MASLD, la principal comorbilidad asociada a mortalidad fue la HAS (hazard ratio ajustada [HRa]: 1.42; intervalo de confianza del 95% [IC 95%]: 1.25-1.61), seguida de la (pre) diabetes (HRa: 1.28; IC 95%: 1.09-1.49) y la hipertrigliceridemia (HRa: 1.19; IC 95%: 1.05-1.34). Un hallazgo importante fue que en las edades de 20 a 40 años la HAS fue un factor de riesgo mayor (HRa: 1.96; IC 95%: 1.29-2.99), y en las edades de 60 a 80 años esta comorbilidad fue la única asociada a mortalidad (HRa: 1.29; IC 95%: 1.09-1.52), siendo entonces la HAS la principal enfermedad como predictor independiente de mortalidad en todos los grupos de edad7.
El mecanismo por el que la MASLD se relaciona con un mayor nivel de presión arterial no se entiende por completo; sin embargo, se ha propuesto que la MASLD, la lipotoxicidad hepatocelular y el daño a los hepatocitos activa el sistema inmunitario innato promoviendo la producción de factores proinflamatorios, como la interleucina 6, el factor de necrosis tumoral alfa y el ligando de la quimiocina CC2. Estos factores proinflamatorios aceleran la inflamación crónica, la cual activa el sistema nervioso simpático, y esto puede elevar la presión sanguínea. Además, el proceso inflamatorio también puede activar el sistema renina-angiotensina, que desempeña un papel fundamental en el desarrollo de la hipertensión14.
Se ha observado una estrecha relación entre la diabetes tipo 2, los niveles de insulina y la RI en el posible mecanismo relacionado con el aumento de la presión sanguínea y la MASLD, ya que el daño de los hepatocitos incrementa la RI, y esta se asocia también con activación del sistema nervioso simpático. Además, los depósitos de grasa perivascular ectópicos y la disfunción endotelial promueven la vasoconstricción y la elevación de la presión arterial, aunado a la reabsorción de sodio y la retención de agua promovidas por la RI15.
Otro posible mecanismo es el relacionado con los hepatocitos esteatósicos que liberan vesículas extracelulares e incrementan la inflamación endotelial y promueven la angiogénesis a través del miR-1, reducen el factor Kruppe-like 4 y activan el factor nuclear kappa B14.
Respecto a los factores de riesgo genéticos, se han descrito variantes asociadas a MASLD, como TM6SF2 E16K y PNPL3 I148M, las cuales causan esteatosis al impedir la producción hepática de lipoproteínas ricas en triglicéridos (TG)6.
Sobrepeso y obesidad
Los dos principales factores predisponentes para prediabetes y diabetes son el sobrepeso o la obesidad y la MASLD, siendo el aumento de la masa de tejido adiposo visceral lo que está vinculado con estas enfermedades8,16.
En un estudio microfisiológico se observó que el incremento de la proporción de adipocitos-hepatocitos afectaba la función de los hepatocitos, así como que inducía la inflamación mediada por macrófagos secundaria a la acumulación de lípidos en los hepatocitos y un incremento en la RI, lo cual es acorde a lo observado en la MASLD16.
La expansión del tejido adiposo relacionada con la obesidad se asocia con la infiltración y la activación de células inmunitarias, como los macrófagos, lo que conduce a un estado de inflamación crónica y leve17.
Tanto la expansión del tejido adiposo como la inflamación desempeñan papeles importantes en la patogénesis de la diabetes tipo 2 a través de varios mecanismos, incluida la liberación de citocinas que interfieren directamente con la vía de señalización de la insulina17. La RI parece ser el vínculo fisiopatológico que conecta la obesidad, la diabetes tipo 2 y la MASLD2.
En los Estados Unidos de América, hasta el 40% de los adultos jóvenes (de 18 a 44 años) presentan RI; esta es más frecuente en aquellos con un IMC más alto, con hipertensión o hipercolesterolemia, y de origen mexicano-estadounidense2.
El papel de la insulina en el desarrollo de MASLD podría estar relacionado con la presencia de polimorfismos de un solo nucleótido (SNP) en la proteína 3 que contiene el dominio de la fosfolipasa similar a la patatina (PNPLA3), por lo que se sugiere que las personas con MASLD y el SNP de PNPLA3 son resistentes a la insulina y podrían experimentar resultados hepáticos más adversos debido a su mayor susceptibilidad a los efectos de la obesidad y la diabetes. Por lo tanto, esta población podría necesitar un tratamiento más temprano y más agresivo que otros grupos de pacientes con MASLD2.
Además, en pacientes con obesidad se ha observado un incremento significativo del GDF-15 (Growth Differentiation Factor-15), una citocina de la familia del factor de crecimiento transformante beta. Este aumento es controversial, ya que el GDF-15 es un inhibidor del apetito que actúa en el núcleo del tracto solitario del área postrema, y sin embargo, se ha observado que el GDF-15 está incrementado en muestras de hígado de pacientes con MASLD, así como en el tejido visceral y subcutáneo de pacientes con obesidad. De forma interesante, la presencia de diabetes tipo 2 en pacientes con obesidad aumenta aún más la expresión de GDF15 en el tejido adiposo17.
Existe una asociación entre la disfunción de los macrófagos del tejido adiposo humano y el fenotipo hepático de MASLD, lo que propone un nuevo mecanismo mediante el cual la diferenciación y la función aberrantes de los macrófagos en el tejido adiposo pueden provocar una alteración de la integridad de la barrera vascular, y contribuir potencialmente a una mayor señalización inflamatoria entre el tejido adiposo y el hígado en los pacientes con MASH18.
Impacto del síndrome metabólico en la MASLD
En el estudio de Pustjens et al.7, durante el periodo de seguimiento (mediana de 22.3 años [16.9-24.2]) se registraron 1405 muertes en la población con MASLD, lo que resultó en una tasa de mortalidad de 19.5 por 1000 personas/año. En el análisis multivariable, la hipertensión, la (pre)diabetes, la hipertrigliceridemia y el IMC se asociaron significativamente con la mortalidad por cualquier causa7. Se observaron tasas de mortalidad más altas para cada trastorno cardiometabólico adicional (log-rank, p > 0.001) (Fig. 1). En comparación con la menor carga cardiometabólica posible de un trastorno en la población MASLD, a partir de tres trastornos cardiometabólicos se observó una asociación positiva con la mortalidad por cualquier causa. Cuando se cumplieron los cinco criterios cardiometabólicos, el riesgo de mortalidad por cualquier causa fue casi el doble que al cumplir solo un criterio (HRa: 1.92; IC 95%: 1.47-2.51)7.
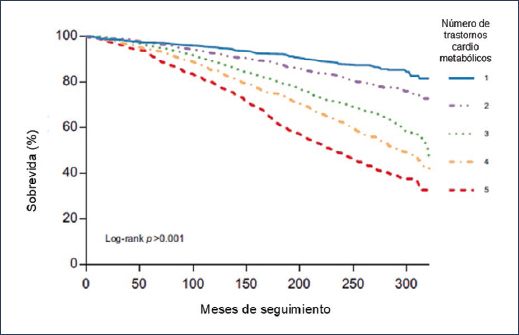
Figura 1. Análisis de supervivencia de los pacientes con MASLD estratificado por el número de trastornos cardiometabólicos7.
Enfermedad cardiovascular
Fundamentalmente, la MASLD aumenta de forma independiente el riesgo de ECV, que es la principal causa de muerte en esta población2,19.
Vías compartidas sustentan la relación bidireccional entre la MASLD y la ECV; el depósito ectópico de grasa que ocurre con el desarrollo de la MASLD también se produce en el epicardio. En combinación con la inflamación sistémica presente en la MASLD, estos factores aumentan la disfunción endotelial y la inflamación intramiocárdica, y aceleran la aterogénesis, lo que provoca enfermedad coronaria, un mayor riesgo de disfunción e hipertrofia diastólica del ventrículo izquierdo, calcificación valvular cardiaca, arritmias (principalmente fibrilación auricular permanente) e insuficiencia cardiaca2,19.
Los pacientes con tres criterios simultáneos para MASLD, caracterizados por diabetes, obesidad y múltiples anomalías metabólicas, presentan niveles marcadamente elevados de colesterol unido a lipoproteínas de baja densidad, triglicéridos, hemoglobina glucosilada y enfermedad cardiovascular aterosclerótica (ECVA), junto con índices avanzados de fibrosis hepática (FIB-4 y NAFLD fibrosis score [NFS]). Estos hallazgos concuerdan con la evidencia previa que posiciona a la MASLD como un factor determinante de la morbilidad cardiovascular, a menudo eclipsando las secuelas hepáticas en esta población19.
La European Association for the Study of the Liver (EASL), la American Association for the Study of Liver Diseases (AASLD), la European Society of Cardiology (ESC) y la American Heart Association (AHA) recomiendan encarecidamente la evaluación del riesgo de ECV en todos los pacientes con MASLD. Para ello, se pueden utilizar varios sistemas de puntuación del riesgo. Dos escalas de evaluación del riesgo de ECV a 10 años, la Framingham Risk Score (FRS) y la escala Atherosclerotic Cardiovascular Disease (ASCVD), están validadas para su uso en pacientes con MASLD, aunque en estudios relativamente pequeños que incluyeron solo a 309 y 1262 individuos, respectivamente6. Los modelos SCORE2 (Systematic Coronary Risk Evaluation 2) y SCORE2-OP (Older Persons) fueron actualizados por la ESC en 2021 para estimar el riesgo a 10 años de eventos de ECV de primera aparición en población europea sin antecedentes de ECV ni diabetes, dividiendo a los países europeos en cuatro zonas de riesgo regionales (riesgo bajo, moderado, alto y muy alto)6.
Los pacientes con un riesgo alto o muy alto de un evento de ECV en los próximos 10 años deben iniciar tratamientos multimodales que incluyan cambios en el estilo de vida, optimización del control glucémico, fármacos hipolipidemiantes, tratamiento antihipertensivo y dejar de fumar. Si bien se debe considerar la monoterapia con estatinas o el tratamiento antihipertensivo en pacientes de bajo riesgo, si corresponde, inicialmente se recomienda centrarse en la intervención en el estilo de vida6.
Enfermedad renal crónica
La inflamación sistémica crónica y de bajo grado, impulsada por el hígado, parece contribuir no solo a la ECV, sino también a la enfermedad renal crónica (ERC)2.
La MASLD se asocia significativamente con un aumento de 1.45 veces en el riesgo a largo plazo de ERC incidente en estadio ≥ 3, siendo la MASLD un factor predictor independiente para ERC2.
Este riesgo se ha observado que es independiente de la edad, el sexo, la obesidad, la hipertensión, la diabetes tipo 2 y otros factores de riesgo renal tradicionales. Además, el riesgo de ERC aumenta aún más con la enfermedad hepática más avanzada, especialmente con la gravedad de la fibrosis hepática20.
La ERC es una enfermedad multisistémica que comparte numerosos factores de riesgo cardiometabólicos con la MASLD, lo que dificulta analizar las relaciones causales entre ambas, por lo que es probable que una compleja combinación de cambios metabólicos y hemodinámicos, nefrotoxicidad lipídica y predisposición genética impulse el desarrollo de ERC en personas con MASLD20.
Otra comorbilidad
Younossi et al.2 hallaron en su revisión que la MASLD se asocia al desarrollo de novo de diabetes, ERC, sarcopenia y canceres extrahepáticos, así como de falla cardiaca, fibrilación atrial y algunos cánceres extrahepáticos, con una disminución de la calidad de vida, menor productividad de trabajo, fatiga y un incremento en la utilización de recursos sanitarios y de salud, convirtiéndose en una carga económica sustancial2,3.
Conclusión
La prevalencia de la MASLD va en aumento junto con la comorbilidad como obesidad y diabetes tipo 2, que tienen un efecto bidireccional con el desarrollo, la gravedad y la progresión de las enfermedades. Ya que la MASLD es un trastorno sistémico con impactos significativos en la salud cardiovascular, la función del músculo esquelético y la integridad renal, el abordaje debe ser multidisciplinario y personalizado, priorizando la detección temprana y la evaluación precisa del riesgo para mitigar la progresión de la comorbilidad.
Financiamiento
Los autores declaran no haber recibido financiamiento para este estudio.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. El estudio no involucra datos personales de pacientes ni requiere aprobación ética. No se aplican las guías SAGER.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no utilizaron inteligencia artificial para la redacción de este manuscrito.
