Introducción
La enfermedad por reflujo gastroesofágico (ERGE) es una patología crónica caracterizada por el retorno del contenido gástrico hacia el esófago, lo que produce síntomas molestos como pirosis y regurgitación, afecta la calidad de vida y puede dar lugar a complicaciones1–3. El tratamiento farmacológico es la base de su manejo, especialmente en las formas moderadas a graves de la enfermedad3,4.
Opciones terapéuticas
Inhibidores de la bomba de protones
Los inhibidores de la bomba de protones (IBP) constituyen la piedra angular en el tratamiento farmacológico de la ERGE. Han demostrado ser los fármacos más eficaces para la supresión del ácido gástrico y para la cicatrización de la esofagitis erosiva.
Clasificación
Los IBP disponibles clínicamente se clasifican en:
- −IBP de liberación retardada: tienen una capa entérica que se disuelve a pH 5.5 en el duodeno. A este grupo pertenecen el omeprazol, el esomeprazol, el lansoprazol, el pantoprazol, el rabeprazol, el dexrabeprazol y el ilaprazol.
- −IBP de liberación dual retardada: se presentan en gránulos con dos capas entéricas; una se disuelve a pH 5.5 en el duodeno y la otra a pH 6.75 en el íleon terminal. A este grupo pertenece el dexlansoprazol.
- −IBP de liberación inmediata: combinación de 20 mg de omeprazol y 1100 mg de bicarbonato. En esta formulación, el IBP no tiene capa entérica y el bicarbonato amortigua el ácido protegiendo la molécula de omeprazol4–6.
Todos tienen mecanismos de acción similares, aunque difieren ligeramente en su farmacocinética, metabolismo hepático y potencia relativa.
Mecanismo de acción
Los IBP actúan inhibiendo de forma irreversible la enzima H+/K+ ATPasa (bomba de protones) localizada en las células parietales gástricas, que es la encargada de la secreción de ácido clorhídrico en el estómago. Al unirse de forma covalente a esta enzima, los IBP suprimen la secreción ácida basal y estimulada.
Los IBP son profármacos que requieren dos protonizaciones en el medio ácido de la célula parietal para transformarse en el fármaco activo. Se unen solo a bombas de protones activadas por el alimento. Por ello, deben administrarse 30 a 60 minutos antes del desayuno o la cena. Su absorción es rápida, pero su vida media plasmática es corta; en los IBP de liberación retardada, es de un promedio de 2 horas. En el caso del dexlansoprazol, la liberación dual permite prolongar la vida media plasmática hasta por 4 horas. El ilaprazol tiene una vida media de 5 horas.
Los IBP se metabolizan principalmente en el hígado por el sistema enzimático CYP450, en especial CYP2C19 y CYP3A4.
Hay una variabilidad interindividual significativa por polimorfismos genéticos del CYP2C19. En metabolizadores lentos pueden tener mayores concentraciones plasmáticas y más efecto, y en metabolizadores ultrarrápidos pueden tener menor eficacia.
El rabeprazol y el ilaprazol son los IBP que tiene un menor metabolismo por la isoenzima 2C196.
El parámetro para evaluar la eficacia clínica de un antisecretor en la ERGE es la capacidad para mantener el pH intragástrico por arriba de 4. El dexlansoprazol y el esomeprazol mantienen el pH por arriba de 4 hasta 17 y 15 horas, respectivamente7.
En la tabla 1 se enlistan las principales diferencias farmacocinéticas y las dosis estándar de los IBP.
Tabla 1. Diferencias entre los inhibidores de la bomba de protones6
| Fármaco | Vida media plasmática (h) | Duración pH > 4 (h/día) | Dosis usual (mg/día) |
|---|---|---|---|
| Omeprazol | 0.5-1 | 10 | 20 |
| Esomeprazol | 1-1.5 | 13 | 20-40 |
| Pantoprazol | 1 | 10 | 40 |
| Lansoprazol | 1-1.5 | 12 | 30 |
| Rabeprazol | 1-1.5 | 12 | 20 |
| Dexrabeprazol | 1-2 | 13 | 10-20 |
| Ilaprazol | 5 | 17 | 10-20 |
| Dexlansoprazol | 1-2 | 17 | 30-60 |
Indicaciones y dosis en la ERGE2–5
- −ERGE erosiva: en los grados A y B se usa una dosis estándar de IBP por 8 semanas. En los grados C y D se usa doble dosis de IBP por 8 semanas. El tratamiento de mantenimiento puede ser con el esquema «a demanda» en las variedades leves de esofagitis y con tratamiento continuo con dosis estándar en las variedades graves.
- −Enfermedad por reflujo no erosiva: se recomienda una dosis estándar de IBP por 4 semanas y tratamiento de mantenimiento con dosis a demanda.
- −Esófago de Barrett: se recomienda usar la dosis continua de IBP suficiente para mantener al paciente sin síntomas.
- −Manifestaciones extraesofágicas de la ERGE: se recomienda doble dosis de IBP por 3 meses y terapia de mantenimiento continua con dosis estándar.
- −ERGE en el embarazo: los IBP pueden usarse en el embarazo. Tienen una clasificación B según la Food and Drug Administration, excepto el omeprazol, que pertenece al grupo C3.
Efectos adversos
Los IBP son generalmente bien tolerados, pero su uso prolongado se ha asociado con algunos efectos adversos (Fig. 1), como:
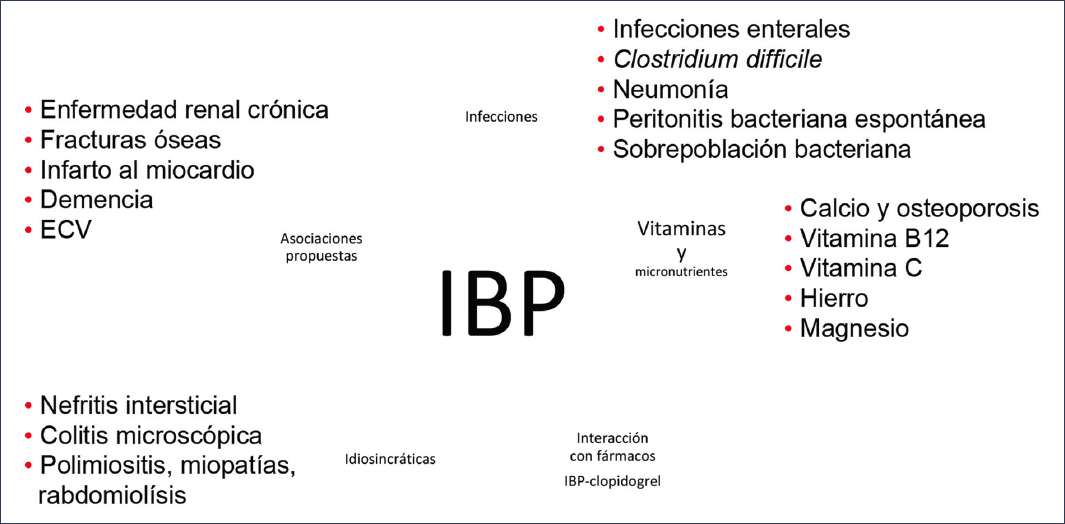
Figura 1. Efectos adversos de los inhibidores de la bomba de protones8.
- −Infecciones entéricas.
- −Mayor riesgo de neumonía adquirida en la comunidad.
- −Malabsorción de vitamina B12, magnesio y calcio.
- −Posible aumento del riesgo de fracturas óseas.
- −Hipergastrinemia con uso prolongado.
- −Nefritis intersticial aguda (raro, pero grave).
De estos efectos adversos, las infecciones entéricas son las únicas que tienen una razón de momios clínicamente significativa (> 3)8.
Criterios para deprescribir IBP
Aunque son eficaces, muchos pacientes continúan usando IBP innecesariamente. Se recomienda evaluar de manera periódica la necesidad de continuar el tratamiento. Algunos criterios para deprescribir son:
- −Remisión mantenida de los síntomas (> 6 meses).
- −Ausencia de esofagitis al suspender el tratamiento.
- −Uso en ERGE no confirmada que ha respondido a cambios en el estilo de vida.
- −Pacientes que los usan solo como «protección gástrica», sin uso concomitante de antiinflamatorios no esteroideos.
La retirada debe hacerse de manera gradual en los pacientes con uso prolongado para evitar un efecto rebote de hipersecreción ácida. En algunos casos, se puede cambiar a un régimen a demanda o utilizar antagonistas H2 como terapia puente9.
Bloqueadores de ácido competitivos de potasio
Los bloqueadores de ácido competitivos de potasio (P-CAB, potassium-competitive acid blockers) son una nueva clase de fármacos antisecretores utilizados en el tratamiento de la ERGE. Su mecanismo de acción consiste en inhibir de manera reversible y competitiva la H+/K+ ATPasa en las células parietales gástricas, el mismo blanco terapéutico que los IBP, pero mediante un mecanismo diferente10–13.
A diferencia de los IBP, que necesitan activarse en un ambiente ácido, no son profármacos y ejercen su efecto de forma rápida y sostenida, con una mayor consistencia en la supresión del ácido gástrico10–14.
Mecanismo de acción
Los P-CAB producen una inhibición competitiva del potasio en la bomba de protones H+/K+ ATPasa. Esto evita el intercambio del potasio por el hidrógeno, lo que impide la unión de los hidrogeniones con el cloro, evitando la formación de ácido clorhídrico en la célula parietal10–14.
La unión irreversible de los P-CAB con la H+/K+ ATPasa hace posible que estos fármacos puedan inhibir bombas de protones tanto activas como inactivas en la fase de reposo de la célula parietal, lo cual permite una inhibición mantenida del ácido desde la primera dosis. Además, los P-CAB son resistentes al ácido gástrico, por lo que no tienen capa entérica y no requieren ser administrados con alimentos10–14.
Diferencias farmacocinéticas con los IBP
En la tabla 2 se presentan las principales diferencias entre los IBP y los P-CAB. Destaca que los PCAB se superconcentran más de 100,000 veces en el espacio ácido de la célula parietal, inhiben de manera reversible la bomba de protones, tienen una vida media plasmática mayor (de hasta 9 horas) e inhiben la secreción de ácido por completo desde la primera dosis.
Tabla 2. Diferencias farmacocinéticas entre los P-CAB y los IBP11
| P-CAB | IBP |
|---|---|
| Actúan directamente (después de su protonización) en la bomba H+/K+-ATPasa | Requieren transformación a la forma activa, sulfenamida |
| Se superconcentran en el espacio ácido de la célula parietal (100,000 veces más que en el plasma) | Se concentran en el espacio ácido de la célula parietal (1000 veces más que en el plasma) |
| Se unen competitivamente al sitio de enlace con el K + de la bomba H+/K+-ATPasa | Unión covalente de la sulfenamida con H+/K+-ATPasa |
| Unión reversible con la bomba de protones Vida media 9.06 h | Unión irreversible con la bomba de protones Vida media 0.5-2.1 h |
| Duración del efecto relacionado con la vida media plasmática del fármaco | Duración del efecto relacionado con la vida media del complejo sulfenamida-bomba de protones |
| Efecto completo desde la primera dosis | Efecto completo después de dosis repetidas |
|
IBP: inhibidores de la bomba de protones; P-CAB: bloqueadores de ácido competitivos de potasio. |
|
Además, los P-CAB se metabolizan por isoenzimas diferentes de la CYP2C19, con lo que se evitan los polimorfismos de metabolizadores rápidos o lentos, y tienen una menor interacción farmacológica10–14.
En la tabla 3 se presentan las características farmacocinéticas de los diferentes P-CAB14. En México están disponibles el tegoprazan y el fexuprazán.
Tabla 3. Farmacología de P-CAB y los IBP
| Farmacocinética y farmacodinamia de los diferentes P-CAB | ||||||
|---|---|---|---|---|---|---|
| Fármaco (Dosis máxima) | Revaprazan (200 mg diarios) | Vonoprazan (40 mg diarios) | Tegoprazan (200 mg diarios) | Fexuprazan (160 mg diarios) | Keverprazan (40 mg diarios) | Zastaprazan (20 mg diarios) |
| Estructura | Pirimidina | Sulfonil pirrol | Benzimidazol | Pirrol | Sulfonil pirrol | Imidazopyiridina |
| pKa | 6.68 | 9.06 | 5.2 | 8.40 | 9.12 | 6.02 |
| Tmax, h | 2.1 ± 1.3 | 1.5 (0.75-3.0) | 1.8 (1.0-4.0) | 2.75 (1.5-5.0) | 1.40 (1.0-3.0) | 1.2 (0.75-2.0) |
| Vida media, h | 2.4 ± 0.2 | 6.1 ± 1.1 | 7.1 ± 2.2 | 7.5 ± 0.8 | 6.5 ± 1.1 | 10.28 ± 3.87 |
| 24-h pH, U – Day 1 | 2.2 | NA | 5.8 ± 0.4 | 5.8 ± 0.3 | NA | 4.95 ± 0.49 |
| 24-h pH, U – Day 7 | 2.5 | NA | 6.4 ± 0.3 | 6.5 ± 0.3 | NA | 5.47 ± 0.45 |
| 24-h pH > 4 Holding Time, % – Day 1 | 28.1 | 85.3 ± 8.3 | 76.8 ± 10.4 | 91.3 ± 4.1 | 85.8 ± 16.9 | 69.8 ± 15.9 |
| 24-h pH > 4 Duración % – Día 7 | 34.2 | 100.0 ± 0.0 | 94.6 ± 3.5 | 99.2 ± 1.9 | 100.0 ± 0.0 | 85.2 ± 11.4 |
| Fuga ácida nocturna | Sí | No | No | No | No | No |
|
IBP: inhibidores de la bomba de protones; P-CAB: bloqueadores de ácido competitivos de potasio. |
||||||
Eficacia clínica
Los ensayos clínicos han demostrado que los P-CAB son tan eficaces como los IBP en la cicatrización de la esofagitis erosiva, y son más efectivos en los casos de esofagitis grave. Esta superioridad también se ha observado en la terapia de mantenimiento en las esofagitis graves. También se ha observado que logran un mayor porcentaje de pacientes libres de síntomas en las primeras semanas de tratamiento. En la ERGE erosiva se usa una dosis estándar de P-CAB durante 8 semanas. Para el tratamiento de mantenimiento se usan dosis estándar o la mitad de la dosis de manera continua3–14.
Los P-CAB son superiores al placebo en el alivio de los síntomas en la enfermedad por reflujo no erosiva. Se usan a dosis estándar por 4 semanas. En el tratamiento de mantenimiento puede usarse el esquema a demanda3–14.
Efectos adversos
Aunque en general son bien tolerados, los P-CAB pueden provocar algunos efectos secundarios, como dolor abdominal, diarrea o estreñimiento, náuseas, cefalea, elevación de las enzimas hepáticas e hipergastrinemia. Hasta ahora no se han reportado efectos adversos graves frecuentes, pero su uso a largo plazo aún está bajo evaluación en estudios de seguimiento prolongado14.
Antagonistas de los receptores H2
Los antagonistas de los receptores H2 fueron durante muchos años el principal tratamiento farmacológico de la ERGE, antes del desarrollo de los IBP. Aunque han sido en gran parte desplazados por estos últimos, siguen teniendo un lugar en el manejo de ciertos pacientes con reflujo gastroesofágico15.
Los fármacos más comunes de esta clase son la ranitidina (retirada en muchos países por impurezas posiblemente carcinógenas), la famotidina (disponible en México), la nizatidina y la cimetidina.
Mecanismo de acción
Actúan bloqueando de forma reversible los receptores H2 de la histamina localizados en las células parietales gástricas. Esto reduce la producción de ácido gástrico, especialmente la secreción basal (no relacionada con la ingesta de alimentos). Inhiben la acción de la histamina sobre la secreción ácida, disminuyen principalmente la secreción nocturna de ácido y su efecto es más rápido que el de los IBP, pero menos potente y de menor duración3.
Indicaciones en la ERGE
- −Pacientes que no toleran los IBP.
- −Terapia combinada con IBP para el control de los síntomas nocturnos.
- −Alternativa en regímenes de deprescripción o de manejo a demanda.
Se usan por periodos cortos de tiempo (2 a 3 semanas), debido al fenómeno de taquifilaxia.
Efectos adversos
Son en general bien tolerados, pero pueden presentarse algunos efectos adversos, más frecuentes con cimetidina, como dolor de cabeza, mareos o fatiga, diarrea o estreñimiento, confusión mental (en pacientes mayores o con insuficiencia renal), ginecomastia y disfunción sexual (especialmente con cimetidina), e interacciones medicamentosas (la cimetidina inhibe varias enzimas hepáticas)2,3.
Antiácidos
Actúan neutralizando el ácido gástrico ya secretado. Ofrecen alivio sintomático rápido, pero de corta duración. Contienen compuestos como hidróxido de magnesio, aluminio y carbonato de calcio (Table 4).
Tabla 4. Principales antiácidos no absorbibles
| Hidróxido de magnesio
Las sales de Mg son osmóticamente activas: diarrea; 15-20% excreción renal |
| Hidróxido de aluminio
El Al reacciona con proteínas de la mucosa intestinal: estreñimiento Impide la absorción de fosfatos: hipomagnesemia; 17-30% excreción renal |
| Sales de aluminio y magnesio
Magaldrato (hidroxisulfato de Mg y Al) Almagato (hidroxicarbonato hidratado de Al y Mg) Melox®: hidróxido de Al y Mg |
| Carbonato de calcio
CaCO3 Estreñimiento |
| Combinaciones
Melox® noche: carbonato de calcio/alginato de magnesio/carbonato de magnesio/hidróxido de aluminio |
Su uso en la ERGE está restringido al alivio de los síntomas ocasionales. No deben usarse como tratamiento a largo plazo por su pobre eficacia. El uso prolongado puede ocasionar eventos adversos como diarrea, estreñimiento e hipomagnesemia.
En la tabla 4 se detallan los principales antiácidos y sus efectos adversos2,3.
Alginatos
Los alginatos son compuestos derivados de algas marrones (como Laminaria) que se utilizan frecuentemente en el tratamiento sintomático de la ERGE, en especial en formas leves o como complemento de otras terapias2,3.
Mecanismo de acción
A diferencia de los fármacos que actúan reduciendo la producción de ácido gástrico, los alginatos forman una barrera física que impide el reflujo del contenido gástrico hacia el esófago. Al entrar en contacto con el ácido gástrico, los alginatos reaccionan formando un gel espeso y viscoso de baja densidad. Este gel flota sobre el contenido gástrico como una balsa, actuando como barrera mecánica que previene el ascenso del ácido hacia el esófago.
Cuando ocurre reflujo, lo que llega al esófago es este gel, no el contenido ácido, reduciendo la lesión esofágica. Algunas formulaciones combinan alginatos con antiácidos (por ejemplo, bicarbonato de sodio y carbonato de calcio), lo cual mejora tanto la protección mecánica como la neutralización del ácido.
Eficacia
Son especialmente útiles en pacientes con síntomas posprandiales o regurgitación ácida. Pueden emplearse como tratamiento a demanda o como coadyuvante junto con IBP en pacientes con síntomas persistentes. No curan la esofagitis erosiva, pero mejoran significativamente el control sintomático16.
Efectos adversos
Los alginatos son bien tolerados. Sus efectos adversos, poco frecuentes y leves, incluyen distensión abdominal, náuseas ocasionales, estreñimiento o diarrea. Debido a su perfil de seguridad, pueden usarse en embarazadas y en pacientes pediátricos bajo supervisión médica16.
Barreras bioadhesivas
Esoxx One es un dispositivo médico que contiene ácido hialurónico, sulfato de condroitina y polímeros bioadhesivos (poloxámeros), que se usa en el tratamiento adyuvante de la ERGE.
Mecanismo de acción
En estudios in vitro se ha demostrado que el ácido hialurónico repara y regenera la mucosa, y el sulfato de condroitina protege contra el daño ácido-pepsina-biliar. Ambos compuestos, combinados con poloxámero, forman una barrera mucoadhesiva que recubre el esófago con una película protectora sobre la mucosa esofágica17.
Indicaciones en la ERGE
En ensayos clínicos controlados, Esoxx One en terapia adyuvante con IBP ha mostrado ser superior al IBP solo para el control de los síntomas en la enfermedad por reflujo no erosiva. También se utiliza en combinación con IBP para acelerar la cicatrización de la esofagitis erosiva. Puede usarse en el embarazo y la lactancia17.
Eventos adversos
En general, Esoxx One es bien tolerado. Se han descrito ocasionalmente náuseas leves o hipersensibilidad a alguno de los componentes17.
Tratamiento de la ERGE refractaria
Es importante saber diferenciar los pacientes que tienen síntomas persistentes de ERGE de aquellos que tienen ERGE refractaria. Los primeros son pacientes que ya han sido estudiados con endoscopia o monitoreo de pH esofágico, tienen evidencia objetiva de ERGE y después de un tratamiento con doble dosis de IBP por 8 semanas continúan con síntomas. Los pacientes con ERGE refractaria son aquellos que tienen evidencia demostrada de ERGE y no han respondido al tratamiento con doble dosis de IBP por 8 semanas, y que en una nueva evaluación diagnóstica bajo tratamiento con IBP persisten con esofagitis, con exposición anormal al ácido o con impedancia basal nocturna < 1500 ohmios o un número de episodios de reflujo > 80 en 24 horas18.
El tratamiento de los síntomas persistentes de ERGE incluye las siguientes opciones:
- −Insistir en las modificaciones del estilo de vida (pérdida de peso, elevación de la cabecera, cena temprana, etc.) y la dosificación adecuada del IBP, 30 a 60 minutos antes del desayuno y la cena.
- −Optimización del tratamiento con IBP, que consiste en utilizar un fármaco diferente del empleado inicialmente, de preferencia uno que no se metabolice por el CYP2C19, como el rabeprazol o el ilaprazol, para sortear la posibilidad de un metabolismo acelerado de IBP.
- −Uso de tratamientos adyuvantes, como antiácidos, alginatos, protectores de la mucosa o dosis nocturna de famotidina por periodos cortos de 2 a 3 semanas.
- −Cambiar el tratamiento con IBP por un P-CAB. Existe evidencia de que los P-CAB pueden ser efectivos en casos de síntomas de ERGE refractarios a los IBP.
El tratamiento de la ERGE refractaria implica la optimización de los antisecretores, como se ha señalado, y el uso de tratamientos avanzados como la funduplicatura en casos de hernias hiatales grandes, la derivación gastroyeyunal en pacientes con ERGE y obesidad mórbida, y en pacientes seleccionados tratamientos endoscópicos, como la gastroplicatura, realizados por endoscopistas entrenados en estos procedimientos18.
Conclusiones
El tratamiento de la ERGE ha evolucionado con el desarrollo de fármacos más rápidos, efectivos y con mayor potencia antisecretora. El uso apropiado de los P-CAB y de los IBP representa la piedra angular en el tratamiento médico de esta condición.
El conocimiento de la farmacología, la farmacodinamia, la eficacia terapéutica y la seguridad de los P-CAB y de los IBP es indispensable para su correcta prescripción. La fenotipificación del paciente con ERGE mediante las pruebas diagnósticas disponibles permite hacer una medicina de precisión y garantiza un mayor éxito terapéutico.
Financiamiento
El autor declara no haber recibido financiamiento para este estudio.
Conflicto de intereses
El autor declara haber sido conferencista para Carnot, Chinoin y M8.
Consideraciones éticas
Protección de personas y animales. El autor declara que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. El estudio no involucra datos personales de pacientes ni requiere aprobación ética. No se aplican las guías SAGER.
Declaración sobre el uso de inteligencia artificial. El autor declara que no utilizó ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.
