Introducción
El síndrome de intestino irritable (SII) es un trastorno de la interacción intestino-cerebro (TIIC), basado en síntomas, definido por los criterios de Roma IV y caracterizado principalmente por dolor abdominal recurrente y alteraciones en la frecuencia o la consistencia de las heces1. Su prevalencia global varía ampliamente, desde cifras tan bajas como un 1% en Francia hasta cerca del 35% en México. Se estima que entre el 5 y el 10% de la población occidental presenta esta condición2,3.
Más allá de su elevada prevalencia, el SII ejerce un impacto considerable sobre la calidad de vida. Aunque históricamente se consideró un trastorno funcional sin base estructural, hoy se reconoce que múltiples mecanismos fisiopatológicos subyacen a su expresión clínica, lo cual permite comprender su frecuente coexistencia con otros trastornos digestivos y extradigestivos.
En este contexto, el concepto de sobreposición alude a la presencia simultánea de síntomas o criterios diagnósticos de dos o más TIIC en un mismo paciente. Este fenómeno puede incluir afecciones digestivas como la dispepsia funcional (DF) o el estreñimiento funcional (EF), y comorbilidad extradigestiva como fibromialgia (FM), síndrome de fatiga crónica (SFC), cefalea, trastornos del sueño y afecciones uroginecológicas.
En este artículo se revisa la sobreposición del SII con otros TIIC y comorbilidad asociada, enfatizando su relevancia clínica, los fundamentos fisiopatológicos comunes y las estrategias para su manejo.
Definición de sobreposición en gastroenterología
En gastroenterología, el término «sobreposición» se refiere a la coexistencia de síntomas o criterios diagnósticos correspondientes a dos o más TIIC en un mismo paciente. Este fenómeno no es infrecuente y representa un desafío tanto diagnóstico como terapéutico, asociado a un aumento en los costos de atención y un deterioro significativo de la calidad de vida.
La sobreposición también plantea retos para la investigación y la práctica clínica, ya que los pacientes suelen presentar síntomas que no se explican por un diagnóstico único. Por ello, se requiere un abordaje individualizado, multidimensional y centrado en el paciente, que contemple los aspectos tanto digestivos como extradigestivos4.
Importancia clínica de la sobreposición en el síndrome de intestino irritable
La sobreposición entre los distintos TIIC y otra comorbilidad es un hallazgo frecuente en los pacientes con SII y conlleva implicaciones clínicas sustanciales. Se ha demostrado que una proporción significativa de estos pacientes cumplen criterios para más de un TIIC, presentan comorbilidad extradigestiva o experimentan síntomas en distintas regiones anatómicas (Fig. 1).
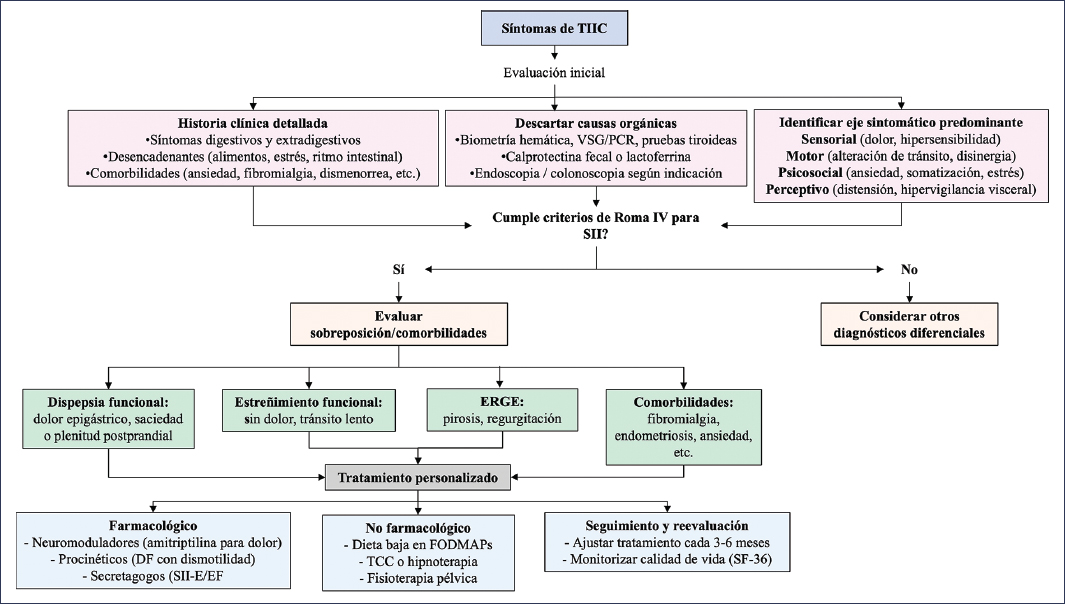
Figura 1. Algoritmo de abordaje clínico para pacientes con síntomas compatibles con trastornos de la interacción intestino-cerebro (TIIC) y posible sobreposición. DF: dispepsia funcional; EF: estreñimiento funcional; ERGE: enfermedad por reflujo gastroesofágico; FM: fibromialgia; FODMAP: oligosacáridos, disacáridos, monosacáridos y polioles fermentables; PCR: proteína C reactiva; SII: síndrome de intestino irritable; SII-E: SII con estreñimiento; TCC: terapia cognitivo-conductual; VSG: velocidad de sedimentación globular.
El Estudio Global de Epidemiología de Roma5 reportó que más del 30% de la población general que cumplía criterios para un TIIC según Roma IV presentaba síntomas en dos o más regiones anatómicas. En unidades de atención terciaria, esta cifra puede superar el 47%, mientras que en población general se aproxima al 26.5%. Esto sugiere que los pacientes atendidos en unidades especializadas suelen tener cuadros más complejos y refractarios.
La sobreposición de TIIC se asocia con mayor gravedad de los síntomas gastrointestinales, peor calidad de vida, mayor carga psicológica (ansiedad, depresión, somatización) y menor respuesta a los tratamientos de primera línea. Por ejemplo, los pacientes con SII y DF suelen experimentar mayor intensidad de los síntomas y más carga emocional en comparación con quienes presentan un único TIIC. Esta complejidad clínica refuerza la necesidad de identificar la sobreposición desde la evaluación inicial y adaptar el abordaje diagnóstico-terapéutico de manera integral, considerando todos los ejes sintomáticos implicados.
En México, el Estudio SIGAME (Síntomas Gastrointestinales en México)6 constituye la primera evaluación epidemiológica poblacional enfocada en los trastornos funcionales digestivos, incluyendo el análisis específico de su sobreposición. Este estudio, realizado en más de 3,900 sujetos adultos provenientes de diversas regiones geográficas y estratos socioeconómicos, evidenció que el SII tiene una prevalencia del 7.6%, mientras que el EF y la dispepsia no investigada alcanzaron prevalencias del 22.3 y el 12%, respectivamente. Estos datos confirman que los TIIC son altamente prevalentes en la población mexicana, y que una proporción importante de pacientes experimentan síntomas que se ajustan a más de un diagnóstico funcional.
En particular, el capítulo dedicado a la sobreposición en el Estudio SIGAME documentó que la coexistencia de SII con otros trastornos funcionales digestivos es común. La sobreposición con síntomas de enfermedad por reflujo gastroesofágico (ERGE) se presentó en 67 sujetos con SII (22.3%; intervalo de confianza del 95% [IC 95%]: 17.9-29.2), con síntomas dispépticos en 54 sujetos (17.9%; IC 95%: 14-22.6) y con eructos excesivos en 37 sujetos (12.2%; IC 95%: 9-16). Estos datos refuerzan la necesidad de una evaluación integral y multidimensional desde el primer contacto clínico.
Los hallazgos de SIGAME son concordantes con lo reportado en estudios internacionales, pero aportan el valor añadido de estar basados en una muestra representativa de la población general mexicana, evaluada mediante herramientas validadas (Roma III, PAGI-SYM, PAGI-QoL). Además, se identificó una mayor frecuencia de sobreposición en mujeres, en adultos jóvenes y en personas en edad productiva, lo que subraya la necesidad de estrategias diagnósticas y terapéuticas sensibles al contexto sociodemográfico.
La incorporación de estos datos en la práctica clínica permite fortalecer un enfoque centrado en el paciente, evitando tratamientos y estudios innecesarios, y favoreciendo intervenciones dirigidas al eje sintomático predominante. Este abordaje resulta esencial para mejorar la calidad de vida, reducir la carga emocional y optimizar el uso de los recursos en sistemas de salud con limitaciones estructurales como el nuestro.
Consideraciones fisiopatológicas
Los TIIC comparten mecanismos fisiopatológicos que pueden coexistir y potenciarse, facilitando la cronicidad y la gravedad de los síntomas. Entre los más relevantes se encuentran hipersensibilidad visceral, disfunción motora, activación inmunitaria de bajo grado, disbiosis intestinal, aumento de la permeabilidad epitelial y alteraciones en la modulación central del dolor1,7 (Tabla 1).
Tabla 1. Mecanismos fisiopatológicos compartidos en los trastornos de la interacción intestino-cerebro y su expresión clínica
| Mecanismo fisiopatológico | Síntomas o manifestaciones clínicas | Trastornos digestivos asociados | Comorbilidad extradigestiva asociada |
|---|---|---|---|
| Hipersensibilidad visceral | Dolor abdominal, distensión, urgencia, sensación de evacuación incompleta | SII, DF, EF, DAF | FM, dolor pélvico crónico |
| Alteraciones de la motilidad | Plenitud y saciedad posprandial, náusea, estreñimiento, diarrea | SII, DF, EF, gastroparesia, ERGE | Migraña, CI |
| Disbiosis intestinal | Flatulencias, distensión, malestar abdominal, síntomas sistémicos | SII, DF, SIBO, SII-PI | FC, ansiedad, trastornos del estado de ánimo |
| Inflamación de bajo grado | Dolor persistente, hiperalgesia, síntomas crónicos inespecíficos | SII, DF, SII-PI | FC, FM |
| Aumento de la permeabilidad intestinal | Malestar abdominal, inflamación sistémica, síntomas multiorgánicos | SII, disbiosis | Endometriosis |
| Disfunción del eje intestino-cerebro | Ansiedad, depresión, insomnio, amplificación del dolor, disautonomía | Todos los TIIC | Trastornos del ánimo, trastornos del sueño |
| Sensibilización central | Dolor generalizado, respuesta exacerbada a estímulos leves | SII, DF | FM, cefalea crónica |
| Alteraciones en la modulación neurológica | Trastornos del ritmo circadiano, cambios de apetito, hiperalgesia | SII, DF, EF | Trastornos del sueño, ansiedad, depresión |
|
CI: cistitis intersticial; DAF: distensión abdominal funcional; DF: dispepsia funcional; EF: estreñimiento funcional; ERGE: enfermedad por reflujo gastroesofágico; FC: fatiga crónica; FM: fibromialgia; SIBO: sobrecrecimiento bacteriano del intestino delgado; SII: síndrome de intestino irritable; SII-PI: SII posinfeccioso; TIIC: trastornos de la interacción intestino-cerebro. |
|||
Hipersensibilidad visceral
Es una respuesta exagerada a estímulos viscerales normales, mediada por sensibilización central y periférica. Es frecuente en el SII, la DF, el EF y la distensión abdominal funcional8. La hiperalgesia puede abarcar distintas regiones digestivas; por ejemplo, los pacientes con DF suelen presentar hipersensibilidad gástrica, mientras que en el SII predomina la hipersensibilidad rectal9,10.
Alteraciones de la motilidad
Pueden afectar diversos segmentos del tubo digestivo, presentándose como vaciamiento gástrico retardado (en el SII y la DF), tránsito colónico lento (en el SII con estreñimiento [SII-E] y el EF) o hipocontractilidad. Estos trastornos pueden influirse entre sí a través de mecanismos reflejos y neurohormonales, como la interferencia del tránsito colónico en la acomodación gástrica7. Además, productos de fermentación como los ácidos grasos de cadena corta pueden modular la motilidad y el tono esfinteriano, exacerbando los síntomas de ERGE o la distensión5.
Disbiosis intestinal
El desequilibrio de la microbiota, tanto luminal como asociada a la mucosa, puede alterar la barrera epitelial, inducir inflamación subclínica y modificar la señalización neuroinmunitaria del eje intestino-cerebro (EIC)7,11. Estas alteraciones se asocian también a manifestaciones sistémicas como fatiga, ansiedad o trastornos del sueño, especialmente en pacientes con múltiples TIIC o comorbilidad como FM12,13.
Disfunción del EIC
El EIC es una red bidireccional que integra el sistema nervioso central, el sistema nervioso entérico, el sistema inmunitario y la microbiota intestinal8. Su alteración puede amplificar la percepción del dolor, afectar la regulación emocional y modular la respuesta autonómica, explicando la expresión multisistémica de muchos TIIC7,13 (Fig. 2).
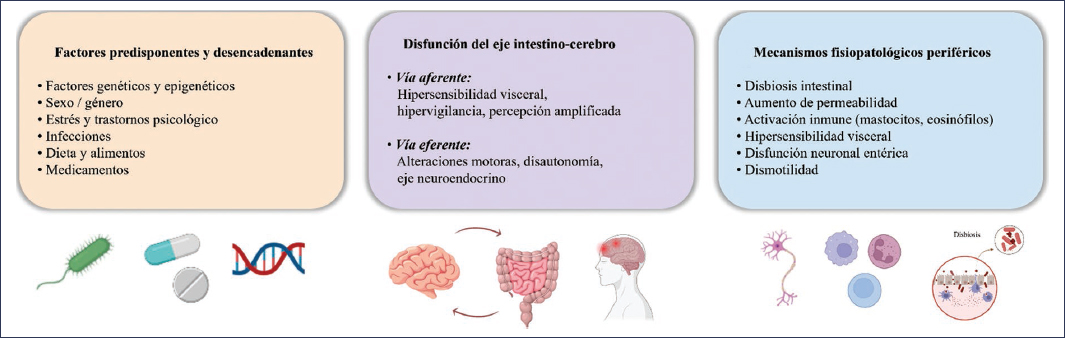
Figura 2. Modelo fisiopatológico de los trastornos de la interacción intestino-cerebro.
Evolución clínica y fluctuación sintomática
La sobreposición entre TIIC condiciona una evolución clínica más tórpida, caracterizada por síntomas más persistentes y de mayor duración, más variabilidad sintomática a lo largo del tiempo, menor respuesta a las terapias convencionales e incremento en la utilización de recursos diagnósticos y asistenciales.
Además, la coexistencia de varios TIIC favorece la fluctuación entre subtipos. En el caso del SII, solo el 24% de los pacientes mantienen el mismo subtipo a lo largo del tiempo, mientras que más del 50% transitan entre SII-E, SII con diarrea [SII-D] y SII mixto14. Esta inestabilidad sintomática exige reevaluaciones clínicas periódicas y un enfoque terapéutico flexible, adaptado a la evolución individual de cada paciente.
Desde el inicio, es fundamental considerar la posibilidad de sobreposición. Esto implica una anamnesis dirigida que explore síntomas en distintas regiones anatómicas, la evaluación de comorbilidad psicosocial, la identificación del eje sintomático predominante y la priorización del síntoma más incapacitante como guía terapéutica.
Reconocer estos patrones permite evitar tratamientos fragmentados, reducir intervenciones innecesarias y promover una visión integral orientada a mejorar la calidad de vida del paciente.
Impacto en la calidad de vida del paciente
La sobreposición del SII con otros TIIC y comorbilidad extradigestiva repercute negativamente en múltiples dimensiones de la calidad de vida, incluyendo aspectos físicos, emocionales, funcionales, sociales y laborales. Este impacto va más allá del malestar digestivo, afectando de forma integral la experiencia del paciente.
Diversos estudios han demostrado que los pacientes con diversos TIIC presentan mayor gravedad de los síntomas, más carga somática, ansiedad relacionada con la salud y una interferencia más significativa en sus actividades cotidianas. También tienden a utilizar con mayor frecuencia los servicios de salud y a experimentar menor satisfacción terapéutica15–18.
El número de TIIC se correlaciona directamente con peor percepción de la salud general, mayor ausentismo laboral y disminución en la productividad. En el Estudio Global de Roma19, los individuos con síntomas en múltiples regiones anatómicas reportaron puntuaciones significativamente más bajas en todos los dominios del SF-36, especialmente en las dimensiones física, emocional y funcional.
Además, la coexistencia de síntomas viscerales con somatización o trastornos psicológicos aumenta el riesgo de cumplir criterios diagnósticos para trastornos mentales según el Diagnostic and Statistical Manual of Mental Disorders. Esto favorece un ciclo de retroalimentación negativa, donde los síntomas físicos amplifican la ansiedad y la catastrofización, intensificando a su vez la percepción del dolor7,20,21.
Muchos pacientes también refieren sentirse estigmatizados o invalidados por el personal médico, lo que puede derivar en frustración, búsqueda reiterada de atención, intervenciones innecesarias y pobre adherencia al tratamiento. La falta de reconocimiento de la complejidad de su cuadro clínico contribuye a esta percepción.
Por todo lo anterior, la calidad de vida debe considerarse un objetivo terapéutico explícito. El abordaje debe ser integrador y centrado en el paciente, incluyendo:
- − Alivio sintomático dirigido al eje predominante.
- − Intervenciones psicosociales (p. ej., terapia cognitivo-conductual [TCC] o mindfulness).
- − Validación empática de la experiencia del paciente.
- − Educación sobre la naturaleza crónica y multifactorial del trastorno.
- − Una estrategia interdisciplinaria con metas realistas, que puede mejorar sustancialmente la percepción de salud y reducir la carga global de la enfermedad2,22.
Implicaciones diagnósticas y terapéuticas de la sobreposición del síndrome de intestino irritable
El reconocimiento de mecanismos fisiopatológicos compartidos entre los TIIC tiene importantes repercusiones clínicas. En la práctica, es frecuente que los pacientes presenten síntomas en más de una región anatómica o que cumplan criterios para varios TIIC, lo cual demanda un enfoque diagnóstico más flexible e integral.
Diagnóstico en el contexto de la sobreposición
Aunque los criterios de Roma IV resultan útiles para clasificar los TIIC, su aplicación estricta puede limitar la identificación de cuadros superpuestos. Por ejemplo, una proporción significativa de pacientes con DF también cumple criterios para SII, especialmente en los subtipos de síndrome de malestar posprandial y síndrome de dolor epigástrico, con prevalencias de sobreposición del 17% al 55%7.
Se sugiere adoptar un enfoque diagnóstico centrado en:
- − Anamnesis detallada que explore síntomas en distintas regiones anatómicas y su relación con la alimentación, el estrés o la defecación.
- − Evaluación sistemática de comorbilidad psicológica o somática.
- − Utilización de herramientas validadas, como cuestionarios o pictogramas, que favorezcan la comunicación entre médico y paciente.
- − Identificación del síntoma predominante o más incapacitante como eje guía del tratamiento.
Los estudios han demostrado que un diagnóstico clínico basado en estos elementos suele ser estable en el tiempo, con bajo riesgo de omitir enfermedades orgánicas relevantes si la evaluación inicial es adecuada.
Evolución clínica y fluctuación sintomática
Como se mencionó previamente, los TIIC son trastornos dinámicos con alta variabilidad temporal. En el caso del SII, más del 50% de los pacientes modifican su subtipo durante el seguimiento clínico. Esta inestabilidad exige reevaluaciones periódicas y ajustes terapéuticos individualizados según la evolución sintomática14.
Implicaciones terapéuticas
El tratamiento debe orientarse a la fisiopatología dominante y al eje sintomático más incapacitante. Es importante evitar enfoques rígidos o excesivamente sintomáticos. En muchos casos, una combinación racional de terapias resulta más efectiva. Por ejemplo, tratar el estreñimiento en pacientes con SII-E puede mejorar también la plenitud posprandial en casos de sobreposición con síndrome de malestar posprandial.
El uso de neuromoduladores, como antidepresivos tricíclicos, inhibidores selectivos de la recaptación de serotonina, inhibidores selectivos de la recaptación de norepinefrina o ligandos de los canales de calcio, ha mostrado eficacia en el manejo del dolor, la dismotilidad, la ansiedad y la hipervigilancia visceral. Se recomienda:
- − Evitar términos como «antidepresivo» o «antipsicótico» para reducir el estigma y mejorar la adherencia.
- − Iniciar con dosis bajas y ajustar progresivamente.
- − Evitar combinaciones del mismo grupo para prevenir efectos adversos, como el síndrome serotoninérgico.
Adicionalmente, algunos neuromoduladores han demostrado utilidad en comorbilidad frecuente, como FM, migraña o cistitis intersticial.
Rol de la salud mental
La identificación de síntomas afectivos es clave para una estrategia terapéutica efectiva. Se recomienda realizar interconsulta con psiquiatría o psicología en casos de trastornos afectivos moderados a graves, así como en aquellos con síntomas somáticos persistentes. Además, las terapias no farmacológicas (como TCC, hipnoterapia o mindfulness) deben considerarse como parte del tratamiento integral del paciente2.
Sobreposición entre síndrome de intestino irritable y otros trastornos de la interacción intestino-cerebro
SII y DF
La DF es la afección que con más frecuencia se sobrepone con el SII. Hasta el 64% de los pacientes con DF también cumplen criterios para SII, en particular en los subtipos SII-D y síndrome de malestar posprandial23,24. Esta combinación se asocia con mayor intensidad de síntomas, más carga emocional y peor calidad de vida.
En una encuesta panasiática25, entre el 25 y el 33% de los pacientes con SII reportaron dolor epigástrico como síntoma predominante, formando un clúster sintomático independiente.
Ambas condiciones comparten diversos mecanismos fisiopatológicos: hipersensibilidad visceral, disfunción duodenal (con aumento de mastocitos y eosinófilos), disbiosis y un reflejo gastrocólico exacerbado. Además, la sobreposición puede presentarse como una secuela posinfecciosa tras gastroenteritis agudas.
El tratamiento debe orientarse al síntoma predominante y las estrategias incluyen:
- − Neuromoduladores viscerales (como amitriptilina o duloxetina).
- − Antihistamínicos H1/H2 en pacientes con componente alérgico o hipersensibilidad posprandial.
- − Procinéticos en casos con dismotilidad asociada.
- − Dieta baja en oligosacáridos, disacáridos, monosacáridos y polioles fermentables (FODMAP).
- − Técnicas de relajación diafragmática y abordajes psicosociales.
SII y EF
La diferenciación entre SII-E y EF puede ser compleja, ya que comparten síntomas como evacuación infrecuente, pujo, esfuerzo excesivo y sensación de evacuación incompleta. La presencia de dolor abdominal recurrente orienta hacia SII-E, mientras que su ausencia favorece el diagnóstico de EF.
Los estudios basados en los criterios de Roma III han reportado que entre el 18 y el 44% de los pacientes cumplen criterios para ambos trastornos26,27, lo cual refleja una significativa sobreposición sintomática. Asimismo, el Estudio Global de Epidemiología de Roma mostró que cerca de un tercio de los pacientes inicialmente diagnosticados con SII-E o EF migraron hacia el otro diagnóstico con el tiempo, lo que evidencia su carácter dinámico23.
Desde la perspectiva fisiopatológica, el tránsito colónico lento y la disinergia del piso pélvico son más frecuentes en el EF, mientras que la hipersensibilidad visceral predomina en el SII-E. Sin embargo, estos hallazgos no son excluyentes. Por ejemplo, la disinergia defecatoria se ha documentado en el 59% de los pacientes con EF, pero también en una proporción relevante de pacientes con SII-E. De igual forma, el tránsito lento se observa en el 47% de los pacientes con EF y en el 22% al 30% de los pacientes con SII-E28.
Clínicamente, los pacientes con sobreposición de SII-E y EF presentan mayor afectación de la calidad de vida, más síntomas de ansiedad y depresión, y mayor frecuencia de consultas médicas. Estas diferencias también impactan en la respuesta al tratamiento. Mientras que algunos agentes, como los secretagogos y los procinéticos, son útiles en ambos grupos, los antidepresivos y la TCC parecen ser más eficaces en los pacientes con SII-E. En cambio, la biorretroalimentación del piso pélvico es una terapia clave en la disinergia defecatoria, característica de ciertos casos de EF29.
En conjunto, el SII-E y el EF deben considerarse afecciones relacionadas dentro de un espectro clínico y fisiopatológico compartido. El abordaje debe individualizarse según la presencia o ausencia de dolor, el patrón de tránsito, las pruebas fisiológicas disponibles y el perfil psicológico del paciente.
SII y ERGE
La sobreposición entre SII y ERGE ocurre en hasta un 47% de los casos, según diversos estudios observacionales23. Esta coexistencia no solo es común, sino también clínicamente significativa, ya que se asocia a mayor refractariedad al tratamiento convencional y peor calidad de vida.
Ambos trastornos comparten mecanismos fisiopatológicos, como hipersensibilidad visceral, dismotilidad segmentaria y vulnerabilidad psicosocial10. En estudios manométricos se ha observado que la distensión colónica puede inducir relajaciones transitorias del esfínter esofágico inferior, exacerbando los síntomas de ERGE30. Esto sugiere una interacción refleja entre segmentos del tracto digestivo.
Además, los pacientes con SII y ERGE presentan mayor prevalencia de ansiedad, hipervigilancia somática y catastrofización, lo cual amplifica la percepción de los síntomas.
El tratamiento debe considerar la disfunción global del EIC y las estrategias incluyen:
- − Neuromoduladores como duloxetina o antidepresivos tricíclicos a dosis bajas.
- − TCC o terapias de regulación emocional.
- − Ajustes dietéticos específicos (p. ej., evitar comidas copiosas y alimentos desencadenantes).
- − Optimización del tratamiento antisecretor si hay criterios de ERGE principalmente erosiva.
Es fundamental evitar una escalada innecesaria en el tratamiento con inhibidores de la bomba de protones cuando los síntomas persisten pese a la normalización endoscópica, y considerar mecanismos funcionales asociados al SII.
SII y distensión abdominal funcional
La distensión abdominal es un síntoma altamente prevalente en los pacientes con SII, especialmente en aquellos con el subtipo SII-E; se estima que hasta el 90% de los pacientes con SII lo experimentan en algún momento31. En muchos casos, la distensión visible no se relaciona con una acumulación objetiva de gas, sino con alteraciones motoras, disfunción diafragmática o percepción somática anómala.
Los estudios con pletismografía abdominal y resonancia magnética han demostrado que la distensión funcional puede deberse a un patrón respiratorio disinérgico, con descenso paradójico del diafragma durante la inspiración y protrusión abdominal secundaria. Esta alteración puede ser inconsciente y reflejar un componente de somatización o hipervigilancia visceral.
Desde la perspectiva fisiopatológica, también se ha propuesto una disfunción en la acomodación del intestino a volúmenes normales de gas o contenido intestinal, exacerbada por dismotilidad segmentaria y alteraciones de la microbiota.
El abordaje terapéutico incluye:
- − Entrenamiento en respiración diafragmática con biorretroalimentación abdominal.
- − Terapias dirigidas a la reeducación postural y del patrón ventilatorio.
- − Neuromoduladores en casos con hipersensibilidad visceral predominante.
- − Intervenciones psicosociales para reducir la atención somática excesiva (p. ej., TCC o mindfulness).
La educación del paciente sobre la fisiopatología funcional de la distensión y la validación de su experiencia son fundamentales para mejorar la adherencia y reducir la ansiedad relacionada con el síntoma.
Comorbilidad extradigestiva
SII y enfermedad inflamatoria intestinal
Aunque la enfermedad inflamatoria intestinal (EII) y el SII son enfermedades distintas, se ha documentado que hasta un 30-40% de los pacientes con EII en remisión clínica presentan síntomas compatibles con SII. Esta situación es más frecuente en pacientes con colitis ulcerosa, y representa un importante desafío diagnóstico y terapéutico7,32.
En estos casos, los síntomas funcionales pueden deberse a alteraciones persistentes en la mucosa intestinal, incluso en ausencia de inflamación activa evidente. Entre los hallazgos más frecuentes se observan:
- − Hipersensibilidad visceral evaluada con barostato, asociada a mayor densidad de mastocitos y sobreexpresión de receptores como TRPV1.
- − Inflamación subclínica, con calprotectina fecal elevada, infiltración de linfocitos intraepiteliales y aumento de citocinas proinflamatorias (como el factor de necrosis tumoral alfa), pese a la aparente remisión clínica y endoscópica33.
- − Cambios neuroinmunitarios posinflamatorios que perpetúan la sensibilización visceral a través de una plasticidad persistente en las vías aferentes32,34.
Desde el punto de vista clínico es crucial distinguir entre síntomas funcionales y un brote inflamatorio. Para ello, se recomienda el uso de biomarcadores (como la calprotectina fecal), estudios de imagen y, en casos necesarios, endoscopía.
La identificación de una sobreposición de SII y EII permite evitar el uso innecesario de inmunosupresores o tratamientos biológicos, y enfocar el manejo en estrategias dirigidas a los síntomas funcionales, tales como:
- − Dieta baja en FODMAP.
- − Neuromoduladores intestinales.
- − Abordajes psicosociales, como TCC o hipnoterapia.
Este enfoque integral mejora el control sintomático y reduce la carga emocional y médica de los pacientes35.
SII y trastornos uroginecológicos
Las mujeres con SII presentan con frecuencia disfunciones pélvicas concomitantes, entre las que destacan dismenorrea, dispareunia, dolor pélvico crónico y vejiga hiperactiva. Esta coexistencia refleja mecanismos fisiopatológicos compartidos, como la hipersensibilidad viscerovisceral y la convergencia sensorial a nivel medular.
Se ha propuesto que la irritación vesical o ginecológica puede sensibilizar aferencias comunes, exacerbando los síntomas digestivos. Además, factores como la disbiosis, la inflamación de bajo grado y la disfunción autonómica pueden modular tanto la percepción del dolor como la motilidad pélvica.
La evaluación de estos casos debe incluir una anamnesis detallada con enfoque multidisciplinario. El abordaje terapéutico se beneficia de la colaboración entre gastroenterología, ginecología, urología, fisioterapia del piso pélvico y salud mental. Las estrategias recomendadas incluyen:
- − Ejercicios de rehabilitación del piso pélvico y biorretroalimentación.
- − Neuromoduladores con acción visceral y somática (como amitriptilina o duloxetina).
- − Intervenciones psicoterapéuticas para el abordaje de la hipervigilancia, la ansiedad o el dolor crónico.
- − Tratamientos específicos para disfunciones urinarias o ginecológicas (según valoración especializada).
La validación del síntoma, el abordaje integral y la coordinación entre especialidades son aspectos clave para mejorar el pronóstico clínico y la calidad de vida en esta población7.
