Introducción
La enfermedad por reflujo gastroesofágico (ERGE) es una de las enfermedades digestivas más frecuentes, con un espectro clínico que va desde pirosis y regurgitación hasta complicaciones estructurales y funcionales del esófago y de otros órganos. Afecta al 10-20% de la población y trasciende el aparato digestivo, asociándose con complicaciones esofágicas y extraesofágicas clínicamente relevantes. Entre las primeras, destacan la estenosis péptica y el esófago de Barrett. Las manifestaciones respiratorias abarcan desde síntomas leves, pero crónicos (tos, disfonía), hasta afecciones complejas como disfunción crónica del injerto (CLAD, chronic lung allograft dysfunction), bronquiolitis obliterante (BOS, bronchiolitis obliterans syndrome) y neumonía por aspiración. En este capítulo se abordan la fisiopatología, el diagnóstico, el tratamiento y el seguimiento de las principales complicaciones esofágicas y respiratorias: estenosis péptica, esófago de Barrett, reflujo en trasplante pulmonar, neumonía por aspiración, fibrosis pulmonar idiopática y asma refractaria. El consenso de Lyon 2.0 redefine los criterios concluyentes por endoscopia y pH-metría de 24 horas: un tiempo de exposición al ácido (TEA) > 6%, esofagitis de Los Angeles B, C o D, y estenosis péptica o esófago de Barrett, y propone el enfoque de «ERGE accionable» con el significado de actuar cuando la presencia de ERGE y de sus consecuencias sean demostradas en forma objetiva y además expliquen los síntomas. Como evidencia en contra de ERGE se consideran un TEA < 4% y la ausencia de hallazgos endoscópicos, y criterios de apoyo1. Las guías del American College of Gastroenterology (ACG) de 2022 y de la American Gastroenterological Association (AGA) de 2023 enfatizan realizar pruebas objetivas antes de tomar decisiones terapéuticas1–3. Debe considerarse que, aunque se demuestre la existencia de reflujo patológico por medio de hallazgos endoscópicos o de un monitoreo de pH-impedancia de 24 horas, incluyendo el registro de reflujo con extensión proximal, dichos resultados no son concluyentes para establecer una relación causal con los síntomas respiratorios. Por ello, la interpretación debe hacerse con cautela y siempre en el contexto clínico integral del paciente, de manera que el criterio clínico prevalezca sobre los hallazgos de los diferentes estudios.
Métodos (búsqueda y criterios)
Se realizó una búsqueda dirigida en PubMed (2015 a 2024) combinando los siguientes términos MeSH: “Gastroesophageal Reflux”, “Peptic Stricture”; “Barrett’s Esophagus”; “Extra-esophageal Complications”; “Lung Transplantation”, “Aspiration Pneumonia”, “Idiopathic Pulmonary Fibrosis”, “Refractory Asthma”, “Esophageal pH Monitoring”, “High-Resolution Manometry”, “Anti-reflux Surgery” y “Radiofrequency Ablation”. Se priorizaron las guías AGA/ACG y el consenso Lyon 2.0, revisiones sistemáticas, metaanálisis y estudios de cohorte; además, revisiones narrativas y series contemporáneas en trasplante pulmonar y cirugía antirreflujo.
Estenosis péptica
Definición y epidemiología
La estenosis péptica es un estrechamiento adquirido del esófago distal secundario a inflamación crónica por exposición ácida. Es la causa más común de estenosis esofágica benigna, aunque su prevalencia ha disminuido con el uso de los inhibidores de la bomba de protones (IBP). La ERGE crónica sin tratamiento lleva a inflamación, fibrosis submucosa y formación de tejido cicatricial en la pared esofágica.
Manifestaciones
Los datos clínicos que sugieren la presencia de una estenosis secundaria a ERGE son la presencia de síntomas típicos de reflujo que se acompañan de datos de alarma, como disfagia y pérdida de peso significativa y progresiva. Algunas veces, los pacientes pueden negar la existencia previa de pirosis y regurgitación.
Diagnóstico
El abordaje inicia con la realización de una endoscopia para clasificar el tipo de estenosis y descartar malignidad. Existen dos tipos relevantes de estenosis: las simples, que son aquellas con una longitud corta (< 2 cm), un trayecto recto, sin angulaciones y que generalmente se encuentran en el tercio distal del esófago, y las complejas, que son largas (> 2 cm), irregulares, anguladas y tienden a recurrir. Las estenosis simples tienen mejor respuesta al tratamiento. Durante la endoscopia es importante considerar la obtención de tejido ante la sospecha de malignidad o para descartar algún diagnóstico diferencial, como esofagitis eosinofílica. Si existe sospecha de esófago de Barrett en presencia de esofagitis, se sugiere dejar la toma de biopsias para otro momento4.
Tratamiento
El manejo de las estenosis benignas secundarias a ERGE se basa principalmente en la dilatación endoscópica acompañada de tratamiento antisecretor intensivo con IBP o bloqueadores ácidos competitivos de potasio (P-CAB, potassium-competitive acid blockers), lo cual ha demostrado reducir el número de sesiones requeridas y prolongar el intervalo libre de síntomas. La esofagectomía se reserva para casos refractarios graves o con fístulas crónicas. Además, existen otras modalidades terapéuticas emergentes que se expondrán al final de esta sección4.
Dilatación endoscópica
Como ya se mencionó, la dilatación endoscópica es el tratamiento de primera línea para las estenosis sintomáticas. Se pueden utilizar diferentes dilatadores (Savary, Maloney) o balones a través del canal del endoscopio, dependiendo del tipo de estenosis y de la experiencia del endoscopista, ya que no se han demostrado diferencias significativas en la eficacia5.
Los dilatadores son unos instrumentos cilíndricos (generalmente flexibles) que consiguen una dilatación mecánica con fuerza radial y longitudinal al ser introducidos a ciegas sobre un alambre guía (Savary-Gilliard) para franquear la estenosis. El dilatador Maloney-Hurst, al no ser guiado, tiene mayor riesgo de perforación, por lo que se reserva para casos seleccionados6. Se prefiere utilizar visión por fluoroscopia en estenosis complejas que no han permitido el paso del endoscopio, para visualizar el grado de dilatación y permitir el diagnóstico inmediato de perforaciones. Con el objetivo de prevenir las perforaciones se aplica la «regla de los 3», que consiste en no dilatar más allá de 3 mm por sesión, pero es posible que esta conducta no tenga efecto sobre la reducción de la tasa de perforaciones4,6,7. Por otro lado, los balones ofrecen la ventaja de que se introducen por el canal de trabajo de los endoscopios y permiten una visualización directa, por lo que se prefieren en estenosis anguladas o muy estrechas; también se pueden usar bajo guía de fluoroscopia4 (Fig. 1). En general, una estenosis péptica esofágica puede requerir varias sesiones de dilatación, dependiendo de su complejidad y etiología. La mayoría de las estenosis benignas simples responden en una a tres sesiones, programadas cada 2 semanas. Se considera que una estenosis péptica es refractaria cuando no se logra un diámetro ≥ 14 mm después de cinco o más sesiones programadas cada 2 semanas4,6.
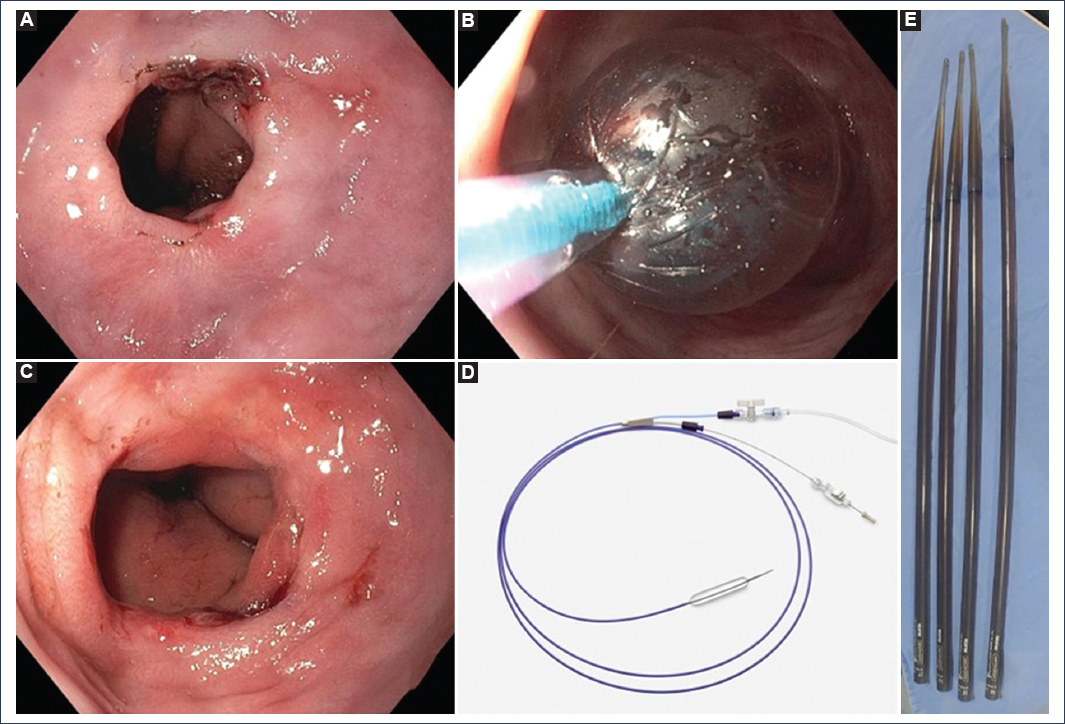
Figura 1. Estenosis esofágica de origen péptico. A: imagen endoscópica de una estenosis péptica con borde ulcerado, asociada a una hernia hiatal. B: dilatación de la estenosis con balón hidrostático. C: apariencia de la estenosis a las 2 semanas de la segunda sesión de dilatación con balón e inhibidor de ácido. D y E: balón hidrostático y dilatadores Savary-Gilliard.
Las complicaciones del tratamiento endoscópico de las estenosis son principalmente la perforación, con un riesgo del 0.1% al 0.4%, el cual es mayor cuando se utiliza un dilatador tipo bujía, en estenosis complejas y posradiación. Esta complicación debe ser tratada de inmediato con clips o cirugía. La hemorragia suele ser poco común y en general se autolimita. En raras ocasiones puede ocurrir leve dolor torácico. Se recomienda evaluar el riesgo de hemorragia, monitorizar al paciente al menos 2 horas después del procedimiento y vigilar datos de alarma como fiebre, dolor torácico persistente u odinofagia grave6.
Esteroides intralesionales
Para el tratamiento de las estenosis pépticas refractarias se pueden inyectar esteroides con el fin de mejorar la remodelación. En una revisión sistemática que incluyó cuatro ensayos clínicos, dos cohortes y seis series de casos con 341 pacientes, se describió que las inyecciones de esteroides añadidas a la dilatación redujeron la necesidad de nuevas dilataciones en estenosis pépticas, por radiación y por cáusticos, sin efectos consistentes en estenosis de anastomosis. Los datos fueron insuficientes para la esofagitis eosinofílica, la esclerosis y las estenosis por fármacos. Se reportaron pocas complicaciones no graves, incluyendo candidiasis esofágica. El esteroide más utilizado fue la triamcinolona a dosis de 20 a 80 mg inyectada en los cuatro cuadrantes de la pared esofágica antes o después de la dilatación. Aunque en la actualidad no existe un consenso sobre la dosis, el momento ni frecuencia óptima de la inyección, en general se recomienda un máximo de tres sesiones con 20 mg de triamcinolona en cada cuadrante, antes de la dilatación. Específicamente para la estenosis péptica, se encontró evidencia sólida a favor del uso de esteroide intralesional en casos refractarios o recurrentes, evidencia limitada en las estenosis por radiación, por cáusticos y de anastomosis, y falta de evidencia en las estenosis por esofagitis eosinofílica, por lo que no se recomienda. Estos datos tienen la limitación de una alta heterogeneidad, un limitado tamaño de muestra y la necesidad de ensayos controlados aleatorizados5.
Prótesis esofágicas
Otra opción es el uso de prótesis metálicas totalmente cubiertas, que logran mantener la luz abierta de manera continua para inducir la remodelación. Se ha reportado un éxito hasta del 45%, pero con un porcentaje de migración importante del 25% al 35% y efectos adversos del 20% al 25%. Existe otro tipo de prótesis que son biodegradables, pero tienen menor fuerza radial y requieren dilatación adicional4.
En la actualidad se dispone de nuevas modalidades para el tratamiento de las estenosis benignas del esófago, como el capuchón dilatador, las incisiones endoscópicas y las prótesis metálicas de aposición luminal. El cap dilatador es un dispositivo con forma de cono que se coloca en la punta del endoscopio y permite la dilatación bajo visión directa; se ha reportado una efectividad de 96%. Las incisiones se reservan para estenosis cortas o membranas; consisten en realizar cortes en forma radial con aguja o tijeras para posteriormente hacer una dilatación con balón. Las prótesis de aposición luminal han demostrado ser útiles para estenosis cortas (< 1 cm), ya que mantienen la luz abierta, pero tienen una alta tasa de migración, de hasta el 40%4.
Esófago de Barrett
Definición y epidemiología
El esófago de Barrett es una metaplasia columnar que reemplaza el epitelio escamoso normal, debido a la exposición crónica al ácido, que afecta aproximadamente al 5% de la población en los Estados Unidos de América y al 1% de la población mundial. Se considera una lesión premaligna, con un riesgo de desarrollar adenocarcinoma esofágico entre el 0.12% y el 0.5% anual8.
Se reconoce que los principales factores de riesgo para desarrollar esófago de Barrett son la ERGE crónica, el sexo masculino, la edad mayor de 50 años, el tabaquismo, la obesidad, la raza blanca y la dieta rica en carnes y alimentos procesados8.
Diagnóstico
El diagnóstico de esófago de Barrett se realiza por endoscopia con el hallazgo de mucosa columnar (metaplasia intestinal) en el esófago distal más allá de 1 cm del término de los pliegues gástricos, confirmada por histopatología. Se desaconseja la toma de biopsias en longitudes < 1 cm debido a que el riesgo de cáncer es extremadamente bajo (0.007% en un seguimiento > 4 años)8,9. Durante la endoscopia se deben medir de manera estandarizada la longitud circunferencial y el segmento más largo de metaplasia utilizando los criterios de Praga, con lo cual se puede clasificar como esófago de Barrett de segmento corto cuando la extensión es < 3 cm y de segmento largo cuando es ≥ 3 cm. La importancia de esta clasificación radica en que el esófago de Barrett de segmento largo tiene mayor riesgo de displasia y cáncer, pero el riesgo de progresión a adenocarcinoma también depende de la presencia y del grado de displasia. En caso de no presentar displasia, el riesgo es del 0.12% al 0.5% anual, para la displasia de bajo grado el riesgo aumenta a un 0.5% a 0.7% anual, y si se presenta displasia de alto grado el riesgo va del 5% al 7% anual8. Las recomendaciones de seguimiento se basan en el resultado histopatológico y se resumen en la tabla 1.
Tabla 1. Recomendaciones para el seguimiento del esófago de Barrett según el resultado histopatológico
| Guía | Displasia negativa | Resultado indeterminado | Displasia bajo grado | Displasia alto grado |
|---|---|---|---|---|
| AGA, 2011 | Cada 3-5 años | – | Cada 6-12 meses | Tratamiento de erradicación + seguimiento cada 3 meses |
| ASGE, 2012 | Cada 3-5 años | Endoscopia después de supresión ácida | Repetir a los 6 meses, luego anual | Considerar tratamiento; si no es candidato, seguimiento cada 3 meses |
| BSG, 2014 | < 3 cm: sin vigilancia ≥ 3 cm: cada 2-3 años | Repetir a los 6 meses | Cada 6 meses | Tratamiento endoscópico |
| ACG, 2016 | Cada 3-5 años | Repetir a los 3-6 meses | Cada 12 meses | Tratamiento endoscópico |
| AMEG, 2017 | < 3 cm: cada 3-5 años ≥ 3 cm: cada 2-3 años | Supresión ácida por 3 meses y repetir endoscopia | Cada 6-12 meses | Tratamiento endoscópico |
| ESGE, 2017 | 1-3 cm: cada 5 años 3-10 cm: cada 3 años > 10 cm: referir a experto | Repetir a los 6 meses | Repetir a los 6 meses; si persiste, ablación | Ablación. Si hay lesión: REM; si no hay displasia: repetir en 3 meses |
ACG: American College of Gastroenterology; AGA: American Gastroenterological Association; ASGE: American Society for Gastrointestinal Endoscopy; BSG: British Society of Gastroenterology; ESGE: European Society of Gastrointestinal Endoscopy; REM: resección mucosa endoscópica.
En relación con la toma de biopsias, tradicionalmente se utiliza el protocolo de Seattle, que consiste en tomar biopsias en los cuatro cuadrantes cada 1-2 cm de la longitud circunferencial de la mucosa con esófago de Barrett, y una biopsia por centímetro en las lengüetas9,10. La detección de displasia depende de la vigilancia endoscópica, el muestreo, la variabilidad entre los patólogos y la distribución en parche de la displasia. Se ha reportado que hasta el 75% de los diagnósticos iniciales de displasia de bajo grado pueden reclasificarse como ausencia de displasia cuando otro patólogo experto hace una revisión, y que en el 50% de los nuevos casos de adenocarcinoma no hubo un diagnóstico previo de esófago de Barrett10.
Tratamiento
El manejo estándar del esófago de Barrett incluye tratamiento médico y tratamiento endoscópico, con vigilancia endoscópica. La base del tratamiento médico es la supresión ácida, y aunque la aspirina ha demostrado tener un papel en la quimioprevención, no se recomienda de manera sistemática debido a sus efectos adversos. La vigilancia endoscópica para la evaluación de la mucosa con toma de biopsias en el esófago de Barrett de segmento corto se debe realizar cada 5 años, mientras que para el de segmento largo el tiempo se acorta a cada 3 años. Cuando los pacientes presentan displasia de bajo grado se indica cada 6 a 12 meses, y en el contexto de displasia de alto grado hay que realizar tratamiento endoscópico inmediato8. Es muy importante señalar que la detección de la displasia depende de la calidad del procedimiento endoscópico, por lo que se deben enfatizar el uso de luz blanca de alta definición, una correcta limpieza y un adecuado tiempo de inspección. Las tasas de detección de neoplasia aumentan con inspecciones de al menos 1 minuto por cada centímetro de esófago de Barrett. Para incrementar el rendimiento diagnóstico pueden emplearse nuevas tecnologías de mejoramiento de imagen que permiten realizar la toma dirigida de biopsias, como NBI (narrow band imaging), LCI (linked color imaging) o herramientas de inteligencia artificial en endoscopia11.
El tratamiento endoscópico incluye la resección de las lesiones visibles, ya sea por resección endoscópica de la mucosa o bien por disección endoscópica de la submucosa, así como la ablación por radiofrecuencia para erradicar toda la superficie de metaplasia residual. Existen técnicas alternativas, como la crioterapia y la coagulación con argón plasma, para la erradicación de la metaplasia residual8.
La ablación por radiofrecuencia ha demostrado ser efectiva para erradicar el esófago de Barrett con o sin displasia. En el caso de la displasia de alto grado, se ha demostrado una tasa de erradicación del 81%, en comparación con el 19% en el grupo control12. De manera similar, en la displasia de bajo grado, la progresión posterior a radiofrecuencia se reportó en el 15%, en comparación con el 26% solo con vigilancia13. Aunque la ablación puede erradicar el esófago de Barrett sin displasia, esta conducta no ha demostrado reducir la mortalidad y en dicho escenario se recomienda identificar a los pacientes con mayor riesgo de progresar para beneficiarse de la ablación (p. ej., con factores de riesgo o mutaciones en el gen p53)10.
Enfermedad por reflujo gastroesofágico en el trasplante pulmonar
Epidemiología y relevancia
La prevalencia de reflujo patológico (ácido y no ácido) después del trasplante pulmonar oscila entre el 50% y el 70%, con alta frecuencia de dismotilidad esofagogástrica14–16. Las microaspiraciones contribuyen a la inflamación de la vía aérea y se asocian con CLAD y BOS. Biomarcadores como la pepsina y los ácidos biliares en el lavado broncoalveolar apoyan la ocurrencia de microaspiraciones gástricas15.
Fisiopatología
Los factores contribuyentes incluyen cambios anatómicos, denervación, alteración del tono del esfínter esofágico inferior, hipomotilidad esofágica, gastroparesia y alteración del aclaramiento esofágico posquirúrgicos. El reflujo no ácido posprandial y la exposición proximal pueden ser particularmente lesivos para el injerto14–16.
Diagnóstico
El consenso Lyon 2.0 define los criterios concluyentes de «ERGE accionable» por endoscopia y pH-metría de 24 horas: TEA > 6%, esofagitis de Los Angeles B, C o D, y estenosis o esófago de Barrett1. La evidencia de soporte incluye > 80 episodios de reflujo en 24 horas, hernia hiatal y asociación sintomática positiva con un índice de síntomas (IS) > 50% o una probabilidad de asociación de síntomas (PAS) > 95%. La manometría de alta resolución identifica hipomotilidad o aperistalsis, y guía la factibilidad de la funduplicatura. La evidencia en contra de ERGE consiste en TEA < 4% y ausencia de hallazgos endoscópicos1–3,14–16.
Tratamiento
En series contemporáneas, la cirugía antirreflujo (funduplicatura) temprana se asocia con menor incidencia de CLAD y BOS, y con mejor preservación de la función del injerto cuando se realiza antes del establecimiento de la CLAD17,18. Sin embargo, la evidencia deriva de cohortes y metaanálisis con heterogeneidad. La selección del paciente exige reflujo demostrado de manera objetiva, correlación clínico-fisiológica y valoración multidisciplinaria. Los IBP reducen la acidez, pero no evitan el reflujo no ácido ni la aspiración. La optimización del vaciamiento gástrico con el empleo de procinéticos, medidas posturales e higiene del comer (comidas pequeñas y frecuentes, evitar el decúbito antes de 3 horas tras ingerir alimentos) son coadyuvantes2,3,15–18.
Neumonía por aspiración
Epidemiología y clínica
La neumonía por aspiración representa el 5-15% de las neumonías comunitarias y afecta a pacientes con alteraciones neurológicas, disfagia orofaríngea o ERGE grave.
Clínicamente puede presentarse con tos crónica, disnea, sibilancias o neumonitis química. Los hallazgos radiológicos típicos incluyen consolidaciones en lóbulos susceptibles, especialmente el lóbulo inferior derecho19.
Fisiopatología y biomarcadores
Las microaspiraciones de ácido, pepsina y bilis causan lesión epitelial e inflamación. El hallazgo de pepsina o ácidos biliares en el lavado broncoalveolar respaldan el origen gástrico15,19. La pH-metría con impedancia permite correlacionar los eventos de reflujo (ácidos, mixtos o no ácidos) con tos o desaturación19. Un estudio ha mostrado que la predisposición genética a ERGE se asocia con mayor riesgo de enfermedad pulmonar obstructiva crónica (EPOC) y neumonía20.
Diagnóstico y tratamiento
Se recomienda documentar ERGE patológica (criterios de Lyon) antes de proponer cirugía antirreflujo. Los estudios de imagen de esófago y de vaciamiento gástrico y esofágico son de apoyo. El uso de IBP a dosis doble, la terapia deglutoria y las medidas posturales constituyen la primera línea de tratamiento. En los niños con daño neurológico, la funduplicatura reduce, pero no elimina, el riesgo de neumonía por aspiración (razón de momios [RM]: ≈ 0.44)21. En los adultos, la cirugía debe individualizarse tras demostrar reflujo relevante (TEA > 6%)1–3,19,21.
Fibrosis pulmonar idiopática
Definición y carga de enfermedad
La fibrosis pulmonar idiopática es una neumonía intersticial fibrosante crónica, de causa desconocida, limitada al pulmón y caracterizada por un patrón radiológico/histológico de neumonía intersticial usual. Tiene un curso progresivo, con una mediana de supervivencia menor de 3 años y peor pronóstico en los varones y en edades avanzadas, con pérdida acelerada de la función pulmonar. Entre los factores de riesgo destacan el tabaquismo, las exposiciones ambientales, la predisposición genética y la ERGE22,23.
Asociación con ERGE y mecanismos fisiopatológicos propuestos
Diversos estudios han mostrado una alta prevalencia de ERGE en la fibrosis pulmonar idiopática, incluso en pacientes sin síntomas digestivos, con predominio de reflujo no ácido, proximal, y presencia de hernia hiatal. La microaspiración crónica de ácido, pepsina y bilis puede inducir lesión epitelial y señalización profibrótica (factor de crecimiento transformante beta, factor nuclear kappa B, receptor farnesoide X), demostrada en modelos animales y en lavado broncoalveolar. La bidireccionalidad mecánica también es relevante: la baja distensibilidad pulmonar favorece las relajaciones transitorias del esfínter esofágico inferior y el reflujo proximal. Aunque se ha propuesto un papel de Helicobacter pylori, la evidencia es inconsistente. Los datos genéticos sugieren un efecto de la ERGE sobre el riesgo de fibrosis pulmonar idiopática, sin evidencia de causalidad inversa22–24.
Diagnóstico
Se recomienda la aplicación de los criterios de Lyon 2.0 para evitar el sobretratamiento. La pH-metría con impedancia deberá realizarse con comidas habituales y análisis de episodios totales, exposición proximal y asociación sintomática (IS/PAS). Un TEA > 6% es concluyente de ERGE, un TEA del 4-6% se considera zona gris (se apoya con > 80 episodios de reflujo, hallazgos endoscópicos y de IS/PAS positivos), y un TEA < 4% va en contra de ERGE. Sin embargo, como ya se mencionó, hay que recordar que una pH-metría positiva para ERGE no necesariamente explica los síntomas respiratorios, incluso con evidencia de extensión proximal, por lo que se debe integrar con la clínica, la funcionalidad y la discusión multidisciplinaria1,22–24.
Tratamiento
El tratamiento con IBP ofrece resultados contradictorios y conlleva el riesgo de infecciones respiratorias. La cirugía antirreflujo puede considerarse en casos con aspiración documentada y reflujo patológico demostrado. Los P-CAB carecen de evidencia específica, aunque son prometedores por su supresión ácida sostenida1–3,23,24.
Asma refractaria
Epidemiología
Las cohortes poblacionales han mostrado una asociación bidireccional entre la ERGE y el asma: la ERGE aumenta el riesgo de asma (RM: ≈1.46) y el asma aumenta el riesgo de ERGE (RM: ≈1.36)25. Las revisiones sistemáticas destacan la coexistencia con asma de difícil control y EPOC26,27.
Mecanismos
Existen dos vías principales: 1) microaspiración de contenido gástrico con inflamación de la vía aérea y 2) reflejos vagales esófago-bronquio que inducen broncoconstricción. El empeoramiento nocturno y posprandial apoya un componente de reflujo. La hipersensibilidad esofágica puede contribuir a la tos crónica26,27.
Diagnóstico y tratamiento
En el asma refractaria no debe asumirse causalidad; se requiere documentación de reflujo patológico o asociación sintomática (IS > 50%, PAS > 95%) en la pH-metría con impedancia. Los IBP muestran beneficio modesto en algunos pacientes y no sustituyen al tratamiento estándar del asma. La cirugía antirreflujo es excepcional y se reserva para pacientes con ERGE probada y con asociación clínica altamente probable1–3,26,27.
Discusión
Las complicaciones de la ERGE comprenden un espectro que abarca desde lesiones estructurales esofágicas, como la estenosis péptica y el esófago de Barrett, hasta manifestaciones extraesofágicas respiratorias. Todas ellas requieren una evaluación diagnóstica integral basada en endoscopia, pruebas de fisiología esofágica y documentación objetiva de reflujo patológico mediante pH-metría con impedancia y manometría de alta resolución.
La estenosis péptica es una secuela del reflujo ácido crónico no tratado que induce inflamación, fibrosis y formación de tejido cicatricial. Su abordaje debe centrarse en la dilatación endoscópica progresiva, apoyada en terapia antisecretora intensiva con IBP o P-CAB, para reducir las recurrencias y favorecer la cicatrización. En casos refractarios, pueden considerarse inyecciones intralesionales de esteroides o prótesis totalmente cubiertas, mientras que la esofagectomía se reserva para estenosis complejas o recidivantes.
El esófago de Barrett es una metaplasia intestinal adquirida secundaria a la exposición crónica al ácido, con un riesgo de progresión a adenocarcinoma estimado entre el 0.12% y el 0.5% anual. La vigilancia endoscópica sistemática (protocolo de Seattle), el uso de endoscopia de alta definición y las terapias de ablación –especialmente la radiofrecuencia– han modificado el pronóstico, permitiendo la erradicación efectiva de la displasia y la reducción del riesgo de progresión. La integración de biomarcadores y herramientas de inteligencia artificial promete optimizar la detección y la caracterización de lesiones displásicas en el futuro.
En cuanto a las manifestaciones extraesofágicas respiratorias, la evidencia indica que la ERGE contribuye a la patogénesis de trastornos como la CLAD y la BOS posteriores a un trasplante pulmonar, la neumonía por aspiración, la fibrosis pulmonar idiopática y el asma refractaria. Sin embargo, la causalidad directa solo se establece cuando el reflujo patológico es demostrado objetivamente y existe una correlación temporal con los síntomas. La tabla 2 muestra el nivel de evidencia de la asociación de la ERGE con complicaciones respiratorias.
Tabla 2. Resumen de la evidencia clínica para las complicaciones respiratorias
| Complicación | Evidencia clínica | Nivel de certeza |
|---|---|---|
| Trasplante pulmonar | Asociación con CLAD y BOS; ARS puede mejorar la FEV1 y retrasar la disfunción del injerto | Moderada |
| Neumonía por aspiración | Mayor riesgo en pacientes frágiles con disfagia; prevención con IBP o ARS y rehabilitación | Alta |
| Fibrosis pulmonar | Asociación observacional, sin causalidad confirmada; beneficio de antiácidos incierto | Baja |
| Asma refractaria | Asociación frecuente, pero los ensayos con IBP muestran resultados variables | Baja |
ARS: antireflux surgery; BOS: bronquiolitis obliterante; CLAD: disfunción crónica del injerto; FEV1: volumen espiratorio forzado en el primer segundo; IBP: inhibidores de la bomba de protones.
El consenso Lyon 2.0 propone el concepto de «ERGE accionable», centrado en integrar métricas objetivas (TEA, número de episodios de reflujo, asociación sintomática, motilidad y respuesta terapéutica) antes de indicar un tratamiento. La cirugía antirreflujo temprana muestra el beneficio más consistente en el contexto del trasplante pulmonar, al reducir la progresión a CLAD o BOS. En la fibrosis pulmonar idiopática y el asma refractaria, la relación es menos robusta, y debe evitarse el uso indiscriminado de IBP. Se recomiendan un enfoque multidisciplinario y una medicina de precisión basada en la fisiología y los biomarcadores, reservando la cirugía para pacientes con correlación demostrada entre reflujo y síntomas.
Conclusiones
- –Las complicaciones esofágicas (estenosis péptica y esófago de Barrett) y respiratorias son parte del espectro clínico de la ERGE, y su manejo requiere un abordaje integral basado en la fisiología y el control ácido efectivo.
- –En la estenosis péptica, la dilatación endoscópica asociada a antisecreción potente es el pilar del tratamiento; en casos refractarios, pueden emplearse esteroides intralesionales o prótesis.
- –En el esófago de Barrett, la combinación de vigilancia endoscópica estructurada y ablación por radiofrecuencia reduce la progresión a displasia o cáncer.
- –No todas las manifestaciones respiratorias se deben a ERGE; la causalidad debe confirmarse con métricas objetivas (pH-metría con impedancia y manometría).
- –En el trasplante pulmonar debe realizarse una evaluación temprana y considerar la funduplicatura en casos seleccionados.
- –En la neumonía por aspiración se priorizarán la rehabilitación deglutoria, las medidas posturales y los IBP; la cirugía reduce el riesgo, pero no lo elimina.
- –En la fibrosis pulmonar idiopática y el asma refractaria, la evidencia sugiere asociación, pero el beneficio terapéutico es variable; hay que individualizar el manejo y evitar un sobretratamiento.
- –Deben aplicarse las guías Lyon 2.0, AGA 2023 y ACG 2022, fomentando la colaboración entre gastroenterólogos, neumólogos y cirujanos torácicos.
- –Los IBP siguen siendo los principales fármacos antisecretores en estos escenarios de complicaciones de la ERGE, pero los P-CAB son una alternativa prometedora para el control del ácido en casos refractarios y deben ser evaluados en futuros estudios.
Agradecimientos
Los autores agradecen la invitación por parte de la Asociación Mexicana de Gastroenterología y del presidente en turno, Dr. J.M. Remes-Troche.
Financiamiento
Los autores declaran no haber recibido financiamiento para este estudio.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. El estudio no involucra datos personales de pacientes ni requiere aprobación ética. No se aplican las guías SAGER.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no utilizaron ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.
